名校
1 . 下列说法不正确的是
| A.中和热测定实验中,应迅速将NaOH溶液和盐酸在测定装置中混合 |
| B.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 |
| C.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL 5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
| D.已知4H++4I﹣+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除KI溶液、稀硫酸外,还需要用到淀粉溶液 |
您最近一年使用:0次
名校
2 . 合成气的主要成分为一氧化碳和氢气,在工业上用途十分广泛。最近中国科学家成功研究由合成气制备乙醇的新工艺,具体制备路线如下所示:
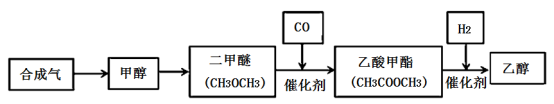
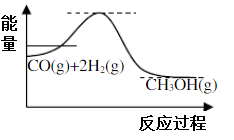
(1)制备甲醇的原理为CO(g)+2H2(g) CH3OH(g),反应过程中物质能量变能化如图所示,生产中为同时提高甲醇的产率和反应速率,可采取措施是
CH3OH(g),反应过程中物质能量变能化如图所示,生产中为同时提高甲醇的产率和反应速率,可采取措施是___________ (写一条即可)。
(2)若该反应加入催化剂,请在答题纸图中画出反应过程中物质能量变化曲线___________ 。
(3)制备二甲醚的原理为2CH3OH(g)= CH3OCH3(g)+H2O(g)。写出该反应的化学平衡常数表达式为___________ 。在2 L容器中发生上述反应,5分钟后,测得甲醇减少16 g,则二甲醛的平均生成速率为___________ 。
(4)CH3COOCH3和H2制备乙醇的反应中,还有另一产物生成,该物质在上述转化路线中循环使用,其分子式为___________ 。 若不考虑生产过程中的损失且每步都反应完全,通过以上制备路线消耗8.4 kgCO时,理论上可制取乙醇的质量为___________ 。
(5)设计实验证明乙醇中是否含有CH3COOCH3____________________ (写出实验的操作步骤、现象和结论)

(1)制备甲醇的原理为CO(g)+2H2(g)
 CH3OH(g),反应过程中物质能量变能化如图所示,生产中为同时提高甲醇的产率和反应速率,可采取措施是
CH3OH(g),反应过程中物质能量变能化如图所示,生产中为同时提高甲醇的产率和反应速率,可采取措施是
(2)若该反应加入催化剂,请在答题纸图中画出反应过程中物质能量变化曲线
(3)制备二甲醚的原理为2CH3OH(g)= CH3OCH3(g)+H2O(g)。写出该反应的化学平衡常数表达式为
(4)CH3COOCH3和H2制备乙醇的反应中,还有另一产物生成,该物质在上述转化路线中循环使用,其分子式为
(5)设计实验证明乙醇中是否含有CH3COOCH3
您最近一年使用:0次
3 . CO2的资源化利用和转化已成为当今科学研究的热点。回答下列问题:
(1)325℃时,水在锰粉表面产生的H2可将CO2转化成甲酸,同时生成MnO。
①由H2O、Mn、CO2制备甲酸的化学方程式为___________ 。
②直接将H2和CO2混合,在325℃条件下难以生成甲酸,而在锰粉表面可以较快生成甲酸的原因是___________ 。
(2)由CO2和H2制备甲醇(CH3OH)的反应原理如下:
反应I.
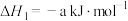 (a>0)
(a>0)
反应I.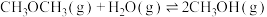
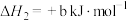 (b>0)
(b>0)
反应Ⅲ. △H3
△H3
恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图所示。其中:CH3OH的选择性=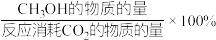 。
。
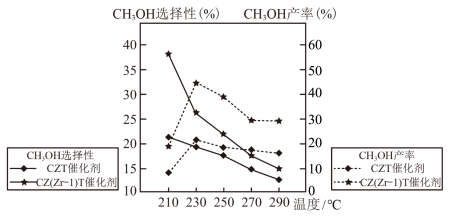
①△H3=_________ kJ∙mol-1,据此判断反应Ⅲ在_________ (填“低温”“高温”或“任意温度”)条件下有利于自发进行。
②在上述条件下,结合图像分析,合成甲醇的最佳温度是________ ,最佳催化剂是________ 。
③温度高于230℃,使用CZT催化剂时CH3OH产率随温度升高而下降的原因是___________ 。
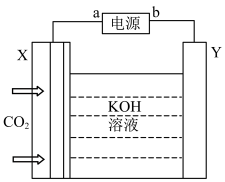
(3)模拟在碱性环境中电催化还原CO2制乙烯(X、Y均为新型电极材料,可减少CO2和碱发生副反应)装置如图所示,装置中b电极为___________ (填“正”或“负”)极,X极上发生反应的电极反应式为___________ 。
(1)325℃时,水在锰粉表面产生的H2可将CO2转化成甲酸,同时生成MnO。
①由H2O、Mn、CO2制备甲酸的化学方程式为
②直接将H2和CO2混合,在325℃条件下难以生成甲酸,而在锰粉表面可以较快生成甲酸的原因是
(2)由CO2和H2制备甲醇(CH3OH)的反应原理如下:
反应I.

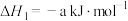 (a>0)
(a>0)反应I.
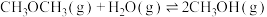
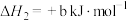 (b>0)
(b>0)反应Ⅲ.
 △H3
△H3恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图所示。其中:CH3OH的选择性=
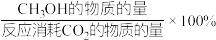 。
。
①△H3=
②在上述条件下,结合图像分析,合成甲醇的最佳温度是
③温度高于230℃,使用CZT催化剂时CH3OH产率随温度升高而下降的原因是
(3)模拟在碱性环境中电催化还原CO2制乙烯(X、Y均为新型电极材料,可减少CO2和碱发生副反应)装置如图所示,装置中b电极为

您最近一年使用:0次
4 . 下列设计方案都正确的是( )
| A.制备绿矾(FeSO4⋅7H2O):将FeSO4溶液在空气中低温蒸发即得绿矾 |
| B.将0.1000mol/L的KMnO4溶液装在碱式滴定管中滴定未知浓度的过氧化氢溶液,读出消耗的高锰酸钾的体积即可求出过氧化氢的浓度 |
| C.探究催化剂对H2O2分解速率影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
| D.用一定浓度的盐酸标准液滴定未知浓度的氨水,可选用酚酞作指示剂 |
您最近一年使用:0次
5 . 尿素[CO(NH2)2]的合成与利用,体现了化学科学与技术的不断进步。
(1) 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为___________ 。
(2)电催化法合成尿素
2021年,科学家设计出一种在 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。


①甲醛和羟胺( )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了___________ 化学键。
②已知在制备和反应过程中,催化剂表面的电子能自发从 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是___________ 。
③实际生产时可忽略步骤Ⅲ可能出现的副产物 和
和 ,原因是
,原因是___________ 。
(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。
①实验测得,烟气中少量 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的___________ 性。
②当无 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为___________ 。
③当无 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是___________ 。
(1)
 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为(2)电催化法合成尿素
2021年,科学家设计出一种在
 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。

①甲醛和羟胺(
 )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了②已知在制备和反应过程中,催化剂表面的电子能自发从
 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是③实际生产时可忽略步骤Ⅲ可能出现的副产物
 和
和 ,原因是
,原因是(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有
 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。①实验测得,烟气中少量
 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的②当无
 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为③当无
 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是
您最近一年使用:0次
2023-10-17更新
|
259次组卷
|
2卷引用:江苏省决胜新高考部分学校2023-2024学年高三上学期10月大联考化学试题
解题方法
6 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
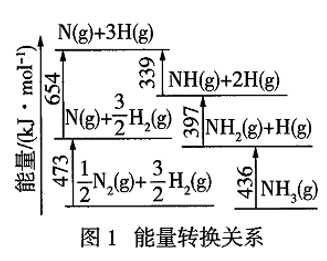
(1)Ⅰ.根据图1数据计算反应
 的
的
 。
。
Ⅱ.在一定温度、催化剂存在的条件下,密闭容器中CO与 转化为
转化为 与
与 ,相关反应如下:
,相关反应如下:
①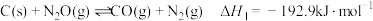
②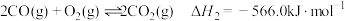
③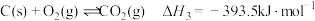
(2)则反应I:
 的
的
(3)合成氨工厂以“水煤气”和
 为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、
为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、 、
、 、
、 的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为
 ,装置如图2。
,装置如图2。
①温度比较:气流a
②气体流速一定,经由催化剂Ⅰ到催化剂Ⅱ,原料转化率有提升,其可能原因是:
③下列说法正确的是
A.合成氨是目前自然固氮最重要的途径
B.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气流速,有利于水煤气生成
C.体系温度升高,可能导致催化剂失活,用热交换器将原料气可预热并使反应体系冷却
D.终端出口2得到的气体,通过液化可分离出
(4)LiH-3d过渡金属复合催化剂也可用于催化合成氨,已知
 先被吸附发生反应
先被吸附发生反应
 ,紧接着
,紧接着 被吸附发生的反应方程式
被吸附发生的反应方程式
您最近一年使用:0次
7 . 催化氢化是一项重要的实验方法,某实验小组制备高活性的雷尼镍,并用于催化氢化反应制备氢化肉桂酸(M=150g/mol)的实验如下:
步骤1:雷尼镍的制备

步骤2:氢化肉桂酸的制备
反应原理和实验装置图如下(夹持和搅拌装置略)。将2.96g肉桂酸溶于45 mL95% 乙醇中,再转移至仪器M中备用。
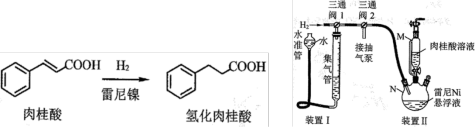
回答下列问题:
(1)装置Ⅱ中仪器N的名称为_______ 。
(2)过程(a)的离子方程式为_______ 。
过程(b)中移除清液的最佳方法为_______ (填字母)。
A.倾析 B.过滤 C.蒸发
雷尼镍相对于普通镍粉有更优的催化活性,原因是_______ 。
(3)步骤2中组装完装置后,需要进行的操作是_______ 。
(4)步骤2中部分实验操作顺序为 c→_______ (填字母)。
a. 向装置I中加水至集气管中充满水
b. 调节三通阀1和2,使装置I 中 H2进入装置Ⅱ
c. 调节三通阀2,抽出装置Ⅱ中空气
d. 调节三通阀1,向装置I中通入H2
若反应中装置I的水准管与集气管液面相平,为使反应继续进行,可进行的操作为_______ 。
(5)氢化肉桂酸粗品纯化的方法为_____ ;纯化得到产品2.5 g,则氢化肉桂酸的产率为___ %(保留小数点后1位)。
步骤1:雷尼镍的制备

步骤2:氢化肉桂酸的制备
反应原理和实验装置图如下(夹持和搅拌装置略)。将2.96g肉桂酸溶于45 mL95% 乙醇中,再转移至仪器M中备用。

回答下列问题:
(1)装置Ⅱ中仪器N的名称为
(2)过程(a)的离子方程式为
过程(b)中移除清液的最佳方法为
A.倾析 B.过滤 C.蒸发
雷尼镍相对于普通镍粉有更优的催化活性,原因是
(3)步骤2中组装完装置后,需要进行的操作是
(4)步骤2中部分实验操作顺序为 c→
a. 向装置I中加水至集气管中充满水
b. 调节三通阀1和2,使装置I 中 H2进入装置Ⅱ
c. 调节三通阀2,抽出装置Ⅱ中空气
d. 调节三通阀1,向装置I中通入H2
若反应中装置I的水准管与集气管液面相平,为使反应继续进行,可进行的操作为
(5)氢化肉桂酸粗品纯化的方法为
您最近一年使用:0次
名校
8 . 重要的化工原料丁烯(C4H8)可由丁烷(C4H10)催化脱氢制备,反应如下:
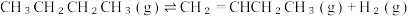 △H
△H
已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
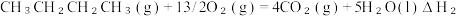
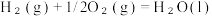 △H3
△H3
(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=_______ 。
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是_______ 。
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
下列说法正确的是_______ (填序号)。[收率=(生成某产物的原料量/投入的原料量)×100%]
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。
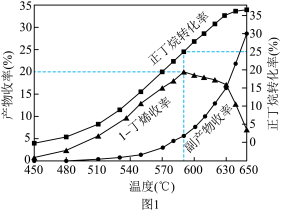
① 实际生产温度选择590℃, 由图1说明其理由是_______ 。
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为_______ mol/(L·min)。
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。
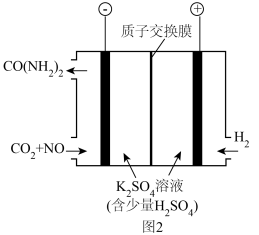
①阴极的电极反应式为_______ 。
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为_______ 。
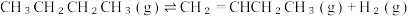 △H
△H已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
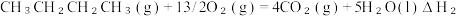
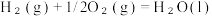 △H3
△H3(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
| 实验组 | 催化剂组成 | 正丁烷转化率 /% | 正丁烯收率 /% |
| 1 | 无催化剂 | 5 | 0.35 |
| 2 | SiO2 | 5 | 0.35 |
| 3 | SiO2+9%CrOx | 25.5 | 18.3 |
| 4 | SiO2+15% CrOx | 27.5 | 20.65 |
| 5 | SiO2+21%CrOx | 24 | 17.87 |
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。

① 实际生产温度选择590℃, 由图1说明其理由是
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。

①阴极的电极反应式为
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为
您最近一年使用:0次
名校
9 . H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
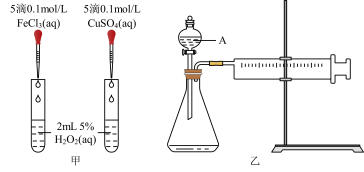
(1)若利用图甲装置,可通过观察__________ 现象,从而定性比较得出结论。
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是________ 。写出H2O2在二氧化锰催化作用下发生反应的化学方程式:___________ 。
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为________ ,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________ 。
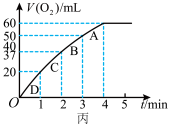
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:________ 。H2O2初始物质的量浓度为_______ (保留两位小数)。

(1)若利用图甲装置,可通过观察
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:

您最近一年使用:0次
2019-09-20更新
|
445次组卷
|
10卷引用:云南省盈江县一中2019-2020学年高二上学期开学考试化学试题
云南省盈江县一中2019-2020学年高二上学期开学考试化学试题人教版高中化学必修二第二单元《化学反应与能量》测试卷2019-2020人教版高中化学必修2第二章《化学反应与能量》测试卷2020年人教版高中化学必修2第二章《化学反应与能量》测试卷12020年春季苏教版高中化学必修2专题二《化学反应与能量转化》测试卷安徽省定远县育才学校2019-2020学年高一下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题云南省石屏县第一中学2021-2022学年高一下学期3月份考试化学试题云南省广南县第一中学校2021-2022学年高一下学期3月份考试化学试题
解题方法
10 . H2O2作为绿色氧化剂应用广泛。氢醌法制备H2O2的原理为:H2+O2 H2O2,装置如图所示。
H2O2,装置如图所示。

已知:①H2O、卤化氢等杂质易使Ni催化剂中毒;②催化剂乙基蒽醌难溶于水,易溶于有机溶剂,熔点107-111°C。下列说法中正确的是
 H2O2,装置如图所示。
H2O2,装置如图所示。
已知:①H2O、卤化氢等杂质易使Ni催化剂中毒;②催化剂乙基蒽醌难溶于水,易溶于有机溶剂,熔点107-111°C。下列说法中正确的是
| A.装置B可选择①或② |
| B.装好试剂后的操作为:打开活塞a、d,关闭活塞b、c |
| C.提纯产品的操作依次为过滤,加水萃取,分液,常压蒸馏 |
| D.若没有F装置三颈烧瓶中的反应速率会减慢 |
您最近一年使用:0次



