名校
1 . Ⅰ.分别取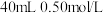 盐酸与
盐酸与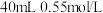 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:
(1)本实验除烧杯、量筒、温度计外还缺少的玻璃仪器名称为________ 。
(2)若某同学通过该实验测定出中和热 偏大,请分析可能的原因是
偏大,请分析可能的原因是________ (填序号)。
A.用量筒量取盐酸时仰视读数
B.分多次将NaOH溶液倒入盛有盐酸的小烧杯中
C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
(3)写出混合溶液中滴入H2O2溶液反应的离子方程式为___________ 。
(4)表中的V=___________ mL,t1、t2、t3由小到大的顺序为___________ 。
(5)某同学研究浓度对化学平衡的影响。他向5mL 0.1mol/L K2Cr2O7溶液中加入1mL 5mol/L NaOH溶液溶液颜色变化为___________ [ (橙色) + H2O
(橙色) + H2O  2H+ + 2
2H+ + 2 (黄色)]。
(黄色)]。
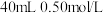 盐酸与
盐酸与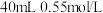 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:(1)本实验除烧杯、量筒、温度计外还缺少的玻璃仪器名称为
(2)若某同学通过该实验测定出中和热
 偏大,请分析可能的原因是
偏大,请分析可能的原因是A.用量筒量取盐酸时仰视读数
B.分多次将NaOH溶液倒入盛有盐酸的小烧杯中
C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知
 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)| 向烧杯中加入的试剂及用量/mL | |||||||
| 0.1mol/L KI溶液 | 0.1mol/L H2O2溶液 | 0.1mol/L H2SO4溶液 | 淀粉溶液 | H2O | 时间/s | ||
| ① | 25℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 | t1 |
| ② | 40℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 | t2 |
| ③ | 25℃ | 20.0 | 5.0 | 5.0 | 1.0 | V | t3 |
(4)表中的V=
(5)某同学研究浓度对化学平衡的影响。他向5mL 0.1mol/L K2Cr2O7溶液中加入1mL 5mol/L NaOH溶液溶液颜色变化为
 (橙色) + H2O
(橙色) + H2O  2H+ + 2
2H+ + 2 (黄色)]。
(黄色)]。
您最近一年使用:0次
名校
2 . 利用传感技术可探究压强对
 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的 和
和 ,当活塞位置不变时,分别在
,当活塞位置不变时,分别在 、
、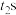 时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是
时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是


 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的 和
和 ,当活塞位置不变时,分别在
,当活塞位置不变时,分别在 、
、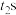 时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是
时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是
| A.E点到F点的变化是压缩注射器所致 |
B.B点到D点 、 、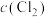 、 、 都减小 都减小 |
C.若容器绝热,则平衡常数 |
| D.C点到D点混合气体颜色由深到浅 |
您最近一年使用:0次
2023-08-20更新
|
291次组卷
|
2卷引用:广东省东莞市东华高级中学2023-2024学年高二上学期10月月考化学试题
3 . 为了研究 的性质,某兴趣小组进行了如下实验。
的性质,某兴趣小组进行了如下实验。
Ⅰ.制备: 易潮解,
易潮解, 能升华。
能升华。
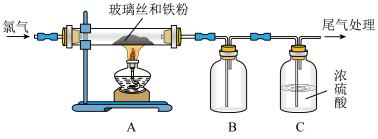
(1)实验开始前先通氯气的目的是_____ 。
(2)若用NaOH溶液处理尾气,发生反应的化学方程式为_____ 。
(3)该装置存在的主要缺点是_____ 。
Ⅱ.溶液的配制:
(4)取 固体溶于浓盐酸,再稀释至指定浓度。配制
固体溶于浓盐酸,再稀释至指定浓度。配制 溶液,需
溶液,需 溶液的体积为
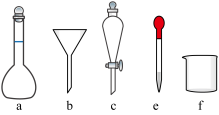
溶液的体积为_____ mL,不需要使用的实验仪器有_____ (填字母)。
Ⅲ. 溶液的性质:
溶液的性质:
(5)向 溶液中通入
溶液中通入 至饱和,充分静置。观察到
至饱和,充分静置。观察到 溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。
溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为_____ 。某同学想检验反应5分钟后的溶液中有 生成,应选用的试剂是
生成,应选用的试剂是_____ 。
(6)为探究实验过程中血红色物质产生的原因,该同学查阅资料发现红色物质可能是 与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:
与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:
假设一:血红色物质的产生与 或
或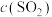 有关
有关
假设二:血红色物质的产生与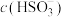 或
或 有关
有关
该同学为验证假设进行以下实验:
①实验一:向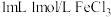 溶液中滴加
溶液中滴加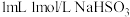 溶液,溶液变成血红色,且颜色比(1)实验深,再加入
溶液,溶液变成血红色,且颜色比(1)实验深,再加入
_____ ,溶液颜色由红色褪成黄色。
②实验二:将 的
的 溶液、
溶液、 溶液、
溶液、 溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。
溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。
表中x=_____ 。
③实验结论:血红色物质是 与
与_____ 形成的配离子。
(7)结合化学平衡解释(1)实验中出现“5分钟后溶液颜色由血红色慢慢变回黄色”现象的原因:_____ 。
 的性质,某兴趣小组进行了如下实验。
的性质,某兴趣小组进行了如下实验。Ⅰ.制备:
 易潮解,
易潮解, 能升华。
能升华。
(1)实验开始前先通氯气的目的是
(2)若用NaOH溶液处理尾气,发生反应的化学方程式为
(3)该装置存在的主要缺点是
Ⅱ.溶液的配制:
(4)取
 固体溶于浓盐酸,再稀释至指定浓度。配制
固体溶于浓盐酸,再稀释至指定浓度。配制 溶液,需
溶液,需 溶液的体积为
溶液的体积为
Ⅲ.
 溶液的性质:
溶液的性质:(5)向
 溶液中通入
溶液中通入 至饱和,充分静置。观察到
至饱和,充分静置。观察到 溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。
溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为 生成,应选用的试剂是
生成,应选用的试剂是(6)为探究实验过程中血红色物质产生的原因,该同学查阅资料发现红色物质可能是
 与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:
与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:假设一:血红色物质的产生与
 或
或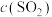 有关
有关假设二:血红色物质的产生与
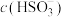 或
或 有关
有关该同学为验证假设进行以下实验:
①实验一:向
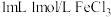 溶液中滴加
溶液中滴加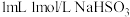 溶液,溶液变成血红色,且颜色比(1)实验深,再加入
溶液,溶液变成血红色,且颜色比(1)实验深,再加入
②实验二:将
 的
的 溶液、
溶液、 溶液、
溶液、 溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。
溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。| 序号 | V/mL | 吸光度 | ||
 |  |  | ||
| 1 | 0.5 | 4.0 | 0.0 | 0.412 |
| 2 | 0.5 | 3.2 | 0.8 | 0.331 |
| 3 | 0.5 | 2.0 | 2.0 | 0.182 |
| 4 | 0.5 | 1.2 | x | 0.085 |
| 5 | 0.5 | 0.0 | 4.0 | 0.018 |
③实验结论:血红色物质是
 与
与(7)结合化学平衡解释(1)实验中出现“5分钟后溶液颜色由血红色慢慢变回黄色”现象的原因:
您最近一年使用:0次
4 . 在一密闭容器中,反应aM(g) bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%,则
bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%,则
 bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%,则
bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%,则| A.平衡向正反应方向移动 | B.物质M的转化率变小 |
| C.反应的化学平衡常数变大 | D.a、b的大小关系是:a>b |
您最近一年使用:0次
2023-07-25更新
|
621次组卷
|
4卷引用:广东省韶关市2022-2023学年高二下学期期末考试化学试题
广东省韶关市2022-2023学年高二下学期期末考试化学试题山东省济宁市泗水县2023-2024学年高二上学期期中考试化学试题(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)山东省临沂市临沭第一中学2023-2024学年高二上学期12月月考化学试题
名校
5 . 在恒温密闭的条件下进行反应:
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.加入高效催化剂,即可增大反应速率,也可增大反应物的平衡转化率 |
| B.若为恒压容器,充入惰性气体,平衡不移动 |
C.达到平衡后,保持 的浓度不变,扩大容器体积,平衡逆向移动 的浓度不变,扩大容器体积,平衡逆向移动 |
| D.若将容器改为绝热恒容,如果反应从正向开始,则到达平衡的时间缩短 |
您最近一年使用:0次
2023-07-10更新
|
338次组卷
|
2卷引用:广东省佛山市顺德区桂洲中学2023-2024学年高一下学期第二次联考化学模拟试题2
6 .  时,向恒容密闭容器中充入
时,向恒容密闭容器中充入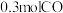 和
和 ,发生反应
,发生反应 。已知
。已知 时反应的平衡常数是1.0。下列说法正确的是
时反应的平衡常数是1.0。下列说法正确的是
 时,向恒容密闭容器中充入
时,向恒容密闭容器中充入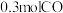 和
和 ,发生反应
,发生反应 。已知
。已知 时反应的平衡常数是1.0。下列说法正确的是
时反应的平衡常数是1.0。下列说法正确的是A. 的平衡转化率为 的平衡转化率为 |
| B.容器内的压强不变时,反应达到平衡状态 |
C.达到平衡后移走 ,平衡向正反应方向移动,化学反应速率加快 ,平衡向正反应方向移动,化学反应速率加快 |
D.其他条件不变,升高温度至 ,若某时刻各气体的浓度均为 ,若某时刻各气体的浓度均为 ,则此时反应向正反应方向进行 ,则此时反应向正反应方向进行 |
您最近一年使用:0次
7 . 用锌片与 稀硫酸反应制取氢气时,下列措施能使氢气生成速率增大的是
稀硫酸反应制取氢气时,下列措施能使氢气生成速率增大的是
 稀硫酸反应制取氢气时,下列措施能使氢气生成速率增大的是
稀硫酸反应制取氢气时,下列措施能使氢气生成速率增大的是| A.降低温度 | B.加入少量 溶液 溶液 | C.不用锌片,改用锌粉 | D.改用 浓硫酸 浓硫酸 |
您最近一年使用:0次
名校
解题方法
8 . 合成氨工业中采用循环操作,主要是为了
| A.增大化学反应速率 | B.提高平衡混合物中氨的含量 |
| C.降低氨的沸点 | D.提高氮气和氢气的利用率 |
您最近一年使用:0次
2023-06-30更新
|
497次组卷
|
16卷引用: 广东实验中学越秀学校2023-2024学年高二上学期期中考试化学试题
广东实验中学越秀学校2023-2024学年高二上学期期中考试化学试题湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷山西省怀仁市2021-2022学年高二上学期期中化学试题人教2019版选择性必修一第二章 第四节 化学反应的调控 课后习题河北省石家庄市2021-2022学年高二上学期期末考试化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)吉林省吉林市2022-2023学年高二上学期期中调研测试化学试题黑龙江省虎林市高级中学2022-2023学年高二上学期期中考试化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题新疆喀什地区疏附县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)化学反应速率与化学平衡——课时7化学反应的调控(已下线)第08讲 化学反应的调控-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)陕西省西安市鄠邑区2022-2023学年高一下学期6月期末考试化学试题四川省遂宁市射洪中学校2023-2024学年高二上学期11月期中化学试题青海省西宁市大通县2023-2024学年高二上学期期末考试化学试题贵州神贵阳市2023-2024学年清镇市博雅实验学校高二上学期第四次月考化学试卷
9 .  -
- 干重整技术(简称“DRM技术”)在转化利用
干重整技术(简称“DRM技术”)在转化利用 的同时可以大量利用
的同时可以大量利用 ,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
主反应:

副反应:

回答下列问题:
(1)已知 、CO和
、CO和 的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
_____ kJ/mol。
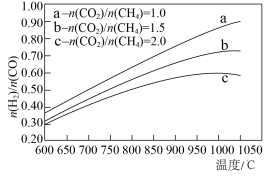
(2)在刚性密闭容器中,反应达到平衡状态时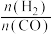 随温度变化的关系如图甲所示,随着进料比
随温度变化的关系如图甲所示,随着进料比 的增加,
的增加,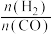 值的变化趋势及原因是
值的变化趋势及原因是_____ 。
(3)在1000℃、压强为P时,按投料比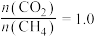 加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为_____ ,副反应的压强平衡常数
_____ (注:对于可逆反应: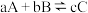 达到化学平衡时,
达到化学平衡时, )
)
(4)DRM技术主反应的催化转化原理的如图乙所示:
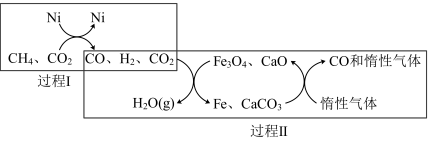
①过程Ⅱ实现了含氢物种与含碳物种的分离。生成 (g)的化学方程式是
(g)的化学方程式是_____ 。
②过程Ⅱ的催化剂是_____ ,只有过程Ⅰ投料比
_____ ,含铁催化剂组成才会保持不变,维持循环使用。
 -
- 干重整技术(简称“DRM技术”)在转化利用
干重整技术(简称“DRM技术”)在转化利用 的同时可以大量利用
的同时可以大量利用 ,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:主反应:


副反应:


回答下列问题:
(1)已知
 、CO和
、CO和 的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
(2)在刚性密闭容器中,反应达到平衡状态时
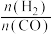 随温度变化的关系如图甲所示,随着进料比
随温度变化的关系如图甲所示,随着进料比 的增加,
的增加,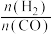 值的变化趋势及原因是
值的变化趋势及原因是
(3)在1000℃、压强为P时,按投料比
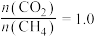 加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
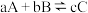 达到化学平衡时,
达到化学平衡时, )
)(4)DRM技术主反应的催化转化原理的如图乙所示:

①过程Ⅱ实现了含氢物种与含碳物种的分离。生成
 (g)的化学方程式是
(g)的化学方程式是②过程Ⅱ的催化剂是

您最近一年使用:0次
名校
10 . 下列现象能用勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②棕红色NO2加压后颜色先变深后变浅
③SO2与O2生成SO3的反应,往往需要使用催化剂
④H2、I2、HI平衡混和气加压后颜色变深
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②棕红色NO2加压后颜色先变深后变浅
③SO2与O2生成SO3的反应,往往需要使用催化剂
④H2、I2、HI平衡混和气加压后颜色变深
| A.①和② | B.①和④ | C.②和③ | D.①②④ |
您最近一年使用:0次
2023-06-26更新
|
347次组卷
|
3卷引用:广东省高州市2020-2021学年高二上学期期末考试化学试题



