1 . 完成汽车尾气中NOx和CO的生成及转化等问题。已知汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) ∆H>0
2NO(g) ∆H>0
(1)汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是______ 。
(2)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的∆H>0,判断该反应在任何温度下能否自发进行______ (填“能”或“不能”)。
(3)目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为_____ 。
(4)若1mol空气含0.8molN2和0.2molO2,1300℃时,在密闭容器内反应N2(g)+O2(g) 2NO(g)达到平衡,测得NO为8×10-4 mol。计算该温度下的平衡常数K=
2NO(g)达到平衡,测得NO为8×10-4 mol。计算该温度下的平衡常数K=______ 。
 2NO(g) ∆H>0
2NO(g) ∆H>0(1)汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是
(2)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的∆H>0,判断该反应在任何温度下能否自发进行
(3)目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
(4)若1mol空气含0.8molN2和0.2molO2,1300℃时,在密闭容器内反应N2(g)+O2(g)
 2NO(g)达到平衡,测得NO为8×10-4 mol。计算该温度下的平衡常数K=
2NO(g)达到平衡,测得NO为8×10-4 mol。计算该温度下的平衡常数K=
您最近一年使用:0次
名校
解题方法
2 . 下列说法中,不正确的是
| A.乙烯聚合为聚乙烯的反应是熵减的过程,∆S<0 |
| B.金属钠和水的反应是熵增、放热、自发进行的反应 |
| C.∆H<0的反应均能够自发进行 |
| D.氯气和消石灰的反应是熵减、自发进行的,一定是放热的反应 |
您最近一年使用:0次
2020-12-01更新
|
458次组卷
|
6卷引用:天津市部分区2020-2021学年高二上学期期中考试化学试题
3 . 下列说法中正确的是
| A.合成氨选择在400~500 ℃进行的重要原因是催化剂在500 ℃左右时的活性最大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.工业合成氨的反应是ΔH<0、ΔS<0的反应,在任何温度下都可自发进行 |
| D.在合成氨中,为增加H2的转化率,充入的N2越多越好 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法中正确的是
| A.合成氨反应选择在400~500℃进行的重要原因是催化剂在500℃左右时的活性最大 |
| B.在工业生产条件优化时,只考虑经济性就行,不用考虑环保 |
| C.工业合成氨的反应是∆H<0、∆S<0的反应,在任何温度下都可自发进行 |
| D.在合成氨中,为增加H2的转化率,充入的N2越多越好 |
您最近一年使用:0次
2020-11-16更新
|
289次组卷
|
5卷引用:天津市滨海新区塘沽第一中学2020-2021学年高二上学期第一次月考化学试题
名校
解题方法
5 . 下列反应在任何温度下都无法自发进行的是
| A.2SO2(g) + O2(g) = 2SO3(g) ΔH= -197.78 kJ/mol |
| B.C(s) + CO2(g) = 2CO(g) ΔH= +172.47 kJ/mol |
| C.AgCl(s) + Br-(aq) = AgBr(s) + Cl-(aq) ΔH= -18.9 kJ/mol |
| D.3O2(g) ⇌ 2O3(g) ΔH= +285.4 kJ/mol |
您最近一年使用:0次
2020-11-07更新
|
563次组卷
|
9卷引用:天津市天津中学2022-2023学年高二上学期期中测试化学试题
天津市天津中学2022-2023学年高二上学期期中测试化学试题天津市实验中学滨海学校2023-2024学年高二上学期期中质量调查化学试题重庆市南开中学2020-2021学年高二上学期期中模拟测试化学试题宁夏青铜峡市高级中学2020-2021学年高二上学期期中考试化学试题北京市一零一中学2020-2021学年高二上学期期中考试化学试题吉林省长春市希望高中2021-2022学年高二上学期期中考试化学试题北京市清华大学附属中学2022-2023学年高二上学期12月月考化学试题湖南省衡阳市衡阳县第五中学2022-2023学年高二上学期期末考试化学试题北京市清华大学附属中学2023-2024学年高二上学期期中考试化学试题
解题方法
6 . 下列反应在任何温度下均能自发进行的是( )
| A.2N2(g)+O2(g)=2N2O(g) △H=+163kJ/mol |
B.H2O2(1)= O2(g)+H2O(l) △H= -98kJ/mol O2(g)+H2O(l) △H= -98kJ/mol |
| C.2HgO(s)=2Hg(1)+O2(g) △H=+182kJ/mol |
D.Fe(s)+ Cl2(g)=FeCl3(s) △H= -138kJ/mol Cl2(g)=FeCl3(s) △H= -138kJ/mol |
您最近一年使用:0次
7 . 反应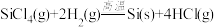 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是
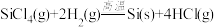 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是A.该反应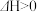 、 、 |
B.该反应的平衡常数 |
C.高温下反应每生成1 mol Si需消耗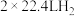 |
D.用E表示键能,该反应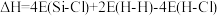 |
您最近一年使用:0次
2020-07-11更新
|
6873次组卷
|
53卷引用:天津市河东区 2022-2023 学年高二上学期期末质量检测化学试题
天津市河东区 2022-2023 学年高二上学期期末质量检测化学试题安徽省宣城二中2020-2021学年高二上学期第一次月考化学试题山东师范大学附属中学2020-2021学年高二上学期期中考试化学试题、黑龙江省大庆实验中学2020-2021学年高二上学期期末考试化学试题河北省祖冲之中学2020-2021学年高二上学期阶段性测试化学试题吉林省长春市第二十九中学2020-2021学年高二下学期期末考试化学试题选择性必修1 专题2 素养检测河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题四川省大竹中学2021-2022学年高二上学期期中达标测化学试题(提高卷)山东省济宁曲阜市第一中学2021-2022学年高二10月月考化学试题江苏省徐州市第三中学2021-2022学年高二上学期10月月考化学试题山东省济南市商河县第三中学2021-2022学年高二10月月考化学试题山东省淄博市高青县第一中学2021-2022学年高二10月月考化学试题宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题安徽省芜湖市2021-2022学年高二上学期期末考试化学试题四川省成都外国语学校2021-2022学年高二上学期12月月考化学试题河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题陕西省西北农林科技大学附属中学2021-2022学年高二上学期期末考试化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(1卷)试题山东省聊城市第二中学2022-2023学年高二上学期第一次月考化学试题广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题湖南省衡阳县第四中学 2022-2023学年高二下学期开学摸底考试(平行班)化学试题陕西省宝鸡市金台区2022-2023学年高二下学期期末考试化学试题吉林省普通高中友好学校联合体2023-2024学年高二上学期第三十七届基础年段期末联考化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题2020年江苏卷化学高考试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编江苏省扬州市邗江区蒋王中学2021届高三上学期第一次质量检测化学试题新疆哈密市第十五中学2021届高三上学期第一次质量检测化学试题(已下线)第24讲 化学平衡常数及转化率的计算 (精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷23 焓变与热化学方程式——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷28 化学平衡及平衡移动——2021年高考化学一轮复习小题必刷(通用版本)(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题(已下线)课时37 化学平衡常数-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第20讲 化学平衡常数及转化率的计算(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)重庆第七中学2021-2022学年高三上学期半期考试化学试题(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)2020年江苏卷化学高考真题变式题1-10陕西省武功县普集高中2021-2022学年高三上学期第四次月考化学试题(已下线)卷07 化学反应速率与化学平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷15 热化学选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)第22讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省汤原县高级中学2021-2022学年高三年级上学期期中考试化学试题贵州省铜仁市第二中学2022-2023学年高三上学期第二次月考化学试题(已下线)选择题6-10广东省湛江市第二中学2023届高三上学期第一次月考化学试题
解题方法
8 . CO2资源化利用的方法之一是合成二甲醚(CH3OCH3)。
(1)CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I: CO2(g) + H2(g) CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
反应II:2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
其中,反应II分以下①、②两步完成,请写出反应①的热化学方程式:①___________
② 2CH3OH(g) CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
(2)二甲醚直接燃料电池具有启动快、效率高等优点。若电解质为碱性,二甲醚直接燃料电池的负极反应式为____________ 。以该电池为电源,用惰性电极电解饱和食盐水的化学方程式为________ 。
(3)反应I产生的CO,有人设想按下列反应除去:2CO(g) = 2C(s) + O2(g),已知该反应的∆H>0,简述该设想能否实现的依据_____________ 。
(4)CO2在自然界循环时可与CaCO3反应,Ksp(CaCO3)=2.8×10−9。 CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10−5mol·L−1,则生成沉淀所需CaCl2溶液的最小浓度为________ 。
(1)CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I: CO2(g) + H2(g)
 CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1反应II:2CO2(g) + 6H2(g)
 CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1其中,反应II分以下①、②两步完成,请写出反应①的热化学方程式:①
② 2CH3OH(g)
 CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1(2)二甲醚直接燃料电池具有启动快、效率高等优点。若电解质为碱性,二甲醚直接燃料电池的负极反应式为
(3)反应I产生的CO,有人设想按下列反应除去:2CO(g) = 2C(s) + O2(g),已知该反应的∆H>0,简述该设想能否实现的依据
(4)CO2在自然界循环时可与CaCO3反应,Ksp(CaCO3)=2.8×10−9。 CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10−5mol·L−1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
解题方法
9 . (1)已知H2S的燃烧热ΔH=-akJ·mol-1,写出表示H2S燃烧反应的热化学方程式__ ,表示H2S燃烧热的热化学方程式__ 。
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是__ (填化学式)。FeCl3水溶液呈__ (填“酸”、“中”、“碱”)性,原因为:__ (用离子方程式表示)。
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是__ 。此时铁锅锈蚀主要是吸氧腐蚀,电极反应方程式为:负极:__ ,正极__ 。
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)__
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)__
臭氧的生成:3O2(g)=2O3(g)__
A.熵增大 B.熵减小 C.熵变很小
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)
臭氧的生成:3O2(g)=2O3(g)
A.熵增大 B.熵减小 C.熵变很小
您最近一年使用:0次
名校
10 . 下列有关化学反应方向及其判据的说法中错误的是( )
| A.1molH2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] |
| B.已知某自发反应A(g)+B(g)=2C(g)△H>0,则△S<0 |
| C.CaCO3(s)=CaO(s)+CO2(g)△H>0能否自发进行与温度有关 |
| D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
您最近一年使用:0次
2020-02-21更新
|
224次组卷
|
5卷引用:天津市第九十五中学益中学校2022-2023学年高二上学期期中考试化学试题



