1 . 下列有关沉淀溶解平衡的说法正确的是
| A.Ksp(AB2)小于Ksp(CD),则AB2的溶解度小于CD的溶解度 |
| B.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,AgCl的Ksp增大 |
| C.在AgI的沉淀溶解平衡体系中,加入K2S固体,AgI沉淀可转化为Ag2S沉淀 |
| D.在CaCO3的沉淀溶解平衡体系中,通入CO2气体,溶解平衡不移动 |
您最近一年使用:0次
2016-12-09更新
|
145次组卷
|
5卷引用:2014-2015江西省奉新县第一中学高二上学期期末化学试卷
2014-2015江西省奉新县第一中学高二上学期期末化学试卷(已下线)2013-2014学年辽宁省大连普通高中高二上学期期末考试理科化学试卷(已下线)2014秋湖北省武汉市部分重点中学高二上学期期中联考化学试卷2014-2015辽宁省沈阳二中高二上学期12月月考化学试卷贵州省毕节市民族中学2019-2020学年高二上学期第二次月考化学试题
12-13高二上·湖南永州·期末
名校
2 . 在2mL NaCl溶液中加入1滴AgNO3溶液,有白色沉淀生成;再加入1滴KI溶液,沉淀转化为黄色,然后再加入1滴Na2S溶液,沉淀又转化为黑色(以上所用的溶液物质的量浓度均相同),下列表示各沉淀物溶解度由大到小的顺序正确的是
| A.Ag2S 、 AgI 、 AgCl | B.AgCl 、 AgI 、 Ag2S |
| C.AgI 、 AgCl、 Ag2S | D.AgCl 、 Ag2S 、 AgI |
您最近一年使用:0次
2016-12-09更新
|
468次组卷
|
7卷引用:江西省赣县第三中学2020-2021学年高二上学期11月强化训练(三)化学试题
14-15高二上·湖南长沙·阶段练习
名校
3 . 已知在25℃时,Ksp(AgCl)=1.8×10—10,Ksp(AgI)=8.3×10—17,下列说法错误的是
| A.在100mL0.01mol/LKCl溶液中,加入1mL0.01mol/LAgNO3溶液,有沉淀析出 |
| B.往氯化银的悬浊液中加硝酸银,c(Cl—)、c(Ag+)均减小 |
| C.由于Ksp(AgCl)>Ksp(AgI),AgCl沉淀在一定条件下可转化为AgI沉淀 |
| D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度减小 |
您最近一年使用:0次
14-15高二上·辽宁沈阳·期中
4 . 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s) 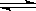 CuS(s)+Mn2+(aq),下列说法正确的是
CuS(s)+Mn2+(aq),下列说法正确的是
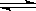 CuS(s)+Mn2+(aq),下列说法正确的是
CuS(s)+Mn2+(aq),下列说法正确的是| A.MnS的Ksp比CuS的Ksp小 |
| B.该反应达平衡时c(Mn2+)=c(Cu2+) |
| C.往平衡体系中加入少量CuSO4固体后,c(Cu2+)减小,c(Mn2+)变大 |
| D.设该反应的平衡常数为K,则该关系成立:K×Ksp(CuS)=Ksp(MnS) |
您最近一年使用:0次
2016-12-09更新
|
702次组卷
|
5卷引用:2014-2015江西省赣州市赣县中学北校区高二1月月考化学试卷
2014-2015江西省赣州市赣县中学北校区高二1月月考化学试卷(已下线)2015届辽宁省沈阳铁路实验中学高二上学期期中考试化学试卷人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡选择性必修1(SJ)专题3第四单元 沉淀溶解平衡3.4.1沉淀溶解平衡原理 课后
13-14高三上·江苏泰州·期末
5 . 下列有关说法正确的是
| A.Hg(l) + H2SO4(aq) = HgSO4(aq) + H2(g)常温下不能自发进行,说明△H<0 |
| B.用惰性电极电解1L1mol/L的CuSO4溶液,当阴极析出3.2 g铜时,加入0.05 molCu(OH)2固体可将溶液恢复至原浓度 |
| C.已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度 |
| D.25℃时,向0.1 mol/L CH3COOH溶液中加入少量CH3COONa固体,该溶液中水的电离程度将增大,且Kw不变 |
您最近一年使用:0次
2016-12-09更新
|
277次组卷
|
5卷引用:2015届江西南昌三中高三11月份月考化学试卷
(已下线)2015届江西南昌三中高三11月份月考化学试卷2016届江西省南昌二中高三上学期第四次模拟化学试卷(已下线)2013届江苏省泰州市高三上学期期末考试化学试卷2020届高三化学选修4二轮专题练——沉淀溶解平衡的影响因素及应用【精编23题】(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)
12-13高二下·江西吉安·期末
名校
6 . 已知25 ℃ 时,AgCl 的溶度积Ksp=1.8×10-10,则下列说法正确的是
| A.向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
| C.温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出. |
| D.将AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,因为AgCl溶解度大于AgI |
您最近一年使用:0次
2016-12-09更新
|
749次组卷
|
9卷引用:2012-2013学年江西省吉安市高二下学期期末考试化学试卷
(已下线)2012-2013学年江西省吉安市高二下学期期末考试化学试卷(已下线)2013-2014湖北省黄石市秋季高二化学期中统考试卷(已下线)2015安徽望江中学同步课时练(人教选修4)3.4难溶电解质的溶解平衡河南省中原名校(即豫南九校)2017-2018学年高二下学期第一次联考化学试题河北省邢台市第八中学2017-2018学年高二上学期期末考试化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题甘肃省张掖市高台县第一中学2022--2023学年高二上学期10月模拟考试化学试题第1课时 沉淀溶解平衡与溶度积
12-13高二上·黑龙江·期末
名校
7 . 以下是25℃时几种难溶电解质的溶解度:
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为__________ (填名称)而除去
(2).①中加入的试剂应该选择__________ 为宜。
(3).②中除去Fe3+时所发生的总反应的离子方程式为__________
(4).下列与方案③相关的叙述中,正确的是( )
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为
(2).①中加入的试剂应该选择
(3).②中除去Fe3+时所发生的总反应的离子方程式为
(4).下列与方案③相关的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
您最近一年使用:0次
2016-12-09更新
|
286次组卷
|
11卷引用:2014届江西省宜春市上高二中高二第六次月考化学试卷
(已下线)2014届江西省宜春市上高二中高二第六次月考化学试卷(已下线)2011-2012学年黑龙江省哈六中高二上学期期末考试化学试卷(已下线)2013届辽宁省鞍山一中上学期期中考试高二年级化学试卷 (已下线)2015安徽望江中学同步课时练(人教选修4)第三章检测试卷2014-2015黑龙江省大庆市铁人中学高二上期末化学试卷2014-2015陕西省西安市一中高二上学期期末化学试卷2015-2016学年湖南省衡阳八中高二上第二次月考化学试卷陕西省西安市第一中学2015-2016学年高二上12月月考化学试卷2015-2016学年内蒙古赤峰市宁城县高二上学期期末考试化学试卷吉林省白城一中2018-2019学年高二上学期期中考试化学试题河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题
8 . 某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是
| A.NaOH | B.ZnO | C.Na2CO3 | D.Fe2O3 |
您最近一年使用:0次
2016-12-09更新
|
573次组卷
|
6卷引用:2013-2014学年江西省新余市高二上学期期末考试化学试卷
(已下线)2013-2014学年江西省新余市高二上学期期末考试化学试卷(已下线)2010年吉林省长春十一中高二上学期期中考试化学试卷2018学年上海市控江中学高二第一学期第一次月考化学考试内蒙古自治区巴彦淖尔市临河区第三中学2019-2020学年高二上学期期末考试化学试题宁夏银川市唐徕中学2022-2023学年高二下学期3月月考化学试题第2课时 沉淀溶解平衡的应用
2013·河南开封·二模
名校
9 . 已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是( )
| A.除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
| B.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 |
| C.因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生 |
| D.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L |
您最近一年使用:0次
2016-12-09更新
|
821次组卷
|
6卷引用:2013-2014学年江西赣州市四所重点中学高二上学期期末联考化学试卷
(已下线)2013-2014学年江西赣州市四所重点中学高二上学期期末联考化学试卷江西省赣州市2021-2022学高二上学期期末考试化学试题(已下线)2013届河南省开封市高三第二次质量检测理综化学试卷步步为赢 高二化学寒假作业:作业十一 难溶电解质的溶解平衡黑龙江省哈尔滨市第六中学2022-2023学年高三8月月考化学试题内蒙古乌兰浩特第一中学2022-2023学年高二上学期第三次月考化学试题
10 . 下列实验操作与预期目的或所得结论一致的是
| A.用铂丝蘸取某溶液进行焰色反应,火焰星黄色,证明该溶液中一定不含有K+ |
| B.向浓度均为0.1mol/L的NaCl和NaI混合溶液中滴加少量AgNO3溶液,出现黄色沉淀,说明Ksp(AgCl)>Ksp(AgI) |
| C.向某溶液中加入硝酸酸化的BaCl溶液,出现白色沉淀,说明该溶液中一定含有SO42- |
| D.在乙酸、乙醇与乙酸乙酯的混合物中加入适量饱和烧碱溶液充分混合后分液,可得到较纯净的乙酸乙酯 |
您最近一年使用:0次
2016-12-09更新
|
231次组卷
|
4卷引用:江西省金溪一中、余江一中等五市八校2018届高三上学期第一次联考化学试题
江西省金溪一中、余江一中等五市八校2018届高三上学期第一次联考化学试题(已下线)2014届江苏省苏北四市高三上期末统考化学试卷(已下线)【艺体生文化课百题突围系列-基础练测】专题2.15 物质的制备及实验方案设计与评价江苏省南京市大厂高级中学2020-2021学年高二下学期3月学情调研化学试题



