2007·广东·高考真题
真题
解题方法
1 . 羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料。其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
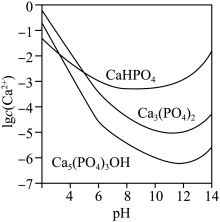
3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O=Ca5(PO4)3OH↓+________ +________
②5Ca(OH)2+3H3PO4=________________________________________________
(2)与方法A相比,方法B的优点是______________________________________ 。
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是
___________________________________________________________________________ 。
(4)图中所示3种钙盐在人体中最稳定的存在形式是______________ (填化学式)。
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因________________________________________________________ 。
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。

3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O=Ca5(PO4)3OH↓+
②5Ca(OH)2+3H3PO4=
(2)与方法A相比,方法B的优点是
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是
(4)图中所示3种钙盐在人体中最稳定的存在形式是
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因
您最近一年使用:0次
解题方法
2 . 选考[化学—选修化学与技术]
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作制冷剂,这一做法对环境的积极意义是___________________________ 。
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:
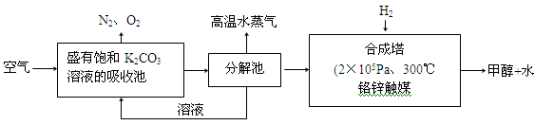
①分解池中反应的化学方程式为:___________________ 。
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式:______________________________ 。
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的__________ 溶液,实验时除测定温度、压强和空气的体积外,还需测定__________________ 。
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作制冷剂,这一做法对环境的积极意义是
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:

①分解池中反应的化学方程式为:
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式:
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的
您最近一年使用:0次
2016-12-09更新
|
449次组卷
|
3卷引用:2015届江西省六校高三3月联考化学试卷
3 . 已知:25°C时, ,
, 。下列说法正确的是
。下列说法正确的是
 ,
, 。下列说法正确的是
。下列说法正确的是A.25°C时,饱和 溶液与饱和 溶液与饱和 溶液相比,前者的 溶液相比,前者的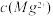 大 大 |
B.25°C时,在 的悬浊液加入少量的 的悬浊液加入少量的 固体, 固体,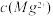 增大 增大 |
C.25°C时, 固体在20ml0.01 mol· 固体在20ml0.01 mol·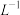 氨水中的 氨水中的 比在20mL0.01mol· 比在20mL0.01mol·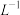  溶液中的 溶液中的 小 小 |
D.25°C时,在 的悬浊液加入 的悬浊液加入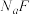 溶液后, 溶液后, 不可能转化成为 不可能转化成为 |
您最近一年使用:0次
2016-12-09更新
|
1385次组卷
|
78卷引用:2011-2012学年江西省白鹭洲中学高二下学期第三次月考化学试卷
(已下线)2011-2012学年江西省白鹭洲中学高二下学期第三次月考化学试卷2015-2016学年江西吉安一中高二下第二次段考化学试卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷江西省靖安中学2020-2021学年高二上学期第二次月考化学试题2009年普通高等学校招生统一考试理综试题化学部分(浙江卷)(已下线)2010年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2011届安徽省阜阳三中高三上学期期末考试化学试卷(已下线)2010—2011学年江苏省盐城中学高二第二学期期末考试化学试卷(已下线)2011-2012学年黑龙江省大庆铁人中学高二上学期第二阶段测试化学试卷(已下线)2011-2012学年吉林省东北师大附中高二上学期期末考试化学试卷(已下线)2011-2012学年河北唐山市第一中学高二年级调研考试化学试卷(已下线)2011-2012学年吉林省长春市十一高中高二上学期期末考试化学试卷(已下线)2011-2012年陕西宁强天津中学高二下学期期中考试化学试卷(已下线)2011-2012学年浙江省浙东北三校高二下学期期中联考化学试卷(已下线)2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(已下线)2014年高二化学人教版选修四 17难溶电解质的溶解平衡练习卷(已下线)2012届吉林东北师大附中高二上学期期末考试化学试卷 (已下线)2014届山东济南外国语学校高三上学期质量检测化学试卷 (已下线)2014~2015学年黑龙江省哈六中高二上学期期中化学试卷2014-2015辽宁省沈阳二中高二上学期12月月考化学试卷2014-2015河南省陕州中学高二下学期第二次精英对抗赛化学试卷2015届新疆乌鲁木齐地区高三第一次诊断性测验化学试卷2015-2016学年吉林省吉林一中高二上期中考试化学试卷2015-2016学年甘肃省天水一中高二上学期第一次段中考试化学试卷2015-2016学年山西省怀仁一中高二上11月月考化学试卷2015-2016学年贵州遵义航天中学高二上第三次月考化学卷2015-2016学年山东省枣庄三中高二上学情调查化学试卷2016届河北省冀州中学高三上学期第四次月考化学试卷2015-2016学年山西省曲沃中学高二上学期12月月考化学试卷2015-2016学年湖南省张家界民族中学高二上学期12月月考化学试卷2015-2016学年河南省南阳市高二上学期期终质量评估化学试卷2015-2016学年黑龙江大庆一中高二下假期验收化学试卷2015-2016学年山西省临汾一中高二5月月考化学试卷2016-2017学年陕西省西安长安区一中高二上期中化学卷2016-2017学年河北省邢台市高二上学期第四次月考化学卷广西桂林市桂林中学2016-2017学年高二下学期期中考试化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第二次月考化学试题吉林省延边第二中学2017-2018学年高二上学期第二次月考化学试题宁夏育才中学勤行校区2017-2018学年高二12月月考化学试题重庆市第一中学2017-2018学年高二上学期期中考试化学试题湖南省师范大学附属中学2017-2018学年高二上学期期末考试化学(理)试题【全国市级联考】黑龙江省齐齐哈尔市2017-2018学年高二下学期期末考试化学试题1【全国市级联考】黑龙江省齐齐哈尔市2017-2018学年高二下学期期末考试化学试题2(已下线)2018年11月19日 《每日一题》人教选修4-沉淀的转化河南省上蔡县第二高级中学2018-2019学年高二上学期期中考试化学试题河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题山东省菏泽市第一中学老校区2018-2019学年高二上学期期末模拟化学试题安徽省滁州市明光中学2019-2020学年高二上学期第一次月考化学试题黑龙江省伊春市第二中学2019-2020学年高二上学期期中考试化学(理)试题苏教版选修四化学反应原理专题3第四单元 难溶电解质的沉淀溶解平衡 同步检测试卷安徽省合肥市肥东县第二中学2019-2020学年高二上学期第二次月考化学试题(普通班)宁夏回族自治区吴忠市青铜峡市高级中学2019-2020学年高二上学期第二次月考化学试题安徽省涡阳县第一中学2019-2020学年高二12月月考化学试题重庆市黔江新华中学校2019-2020学年高二12月月考化学试题云南省丽江市宁蒗县第一中学2019—2020学年高二上学期期末考试化学试题2020年安徽省全省教学质量检测统一考试(练习检测一)河南省焦作市沁阳市第一中学2019-2020高二月考考试化学试题黑龙江省伊春林业管理局第二中学2019-2020学年高二下学期期中质量检测化学试题江苏省常熟市2019-2020学年高二下学期期中考试化学试题福建省福州福清市2017-2018学年高二上学期期末考试化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二下学期期末考试化学试题(已下线)第21讲 难溶电解质的溶解平衡-2021年高考化学一轮复习名师精讲练黑龙江省大兴安岭漠河县高级中学2019-2020学年高二上学期期中考试化学试题甘肃省兰州市第一中学2019-2020学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡(已下线)清远市2016-2017学年度第一学期期末教学质量检测高二化学试题(已下线)3.4.2 沉淀溶解平衡原理的应用(基础练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)黑龙江省实验中学2020-2021学年高三上学期期中考试化学试题陕西省榆林市第十二中学2020-2021学年高二下学期第一次月考化学试题江苏省宜兴市张渚高级中学2020-2021学年高二下学期期中考试化学试题(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)3.4.1 难溶电解质的沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.4.1 沉淀溶解平衡原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)内蒙古彦淖尔市临河区第三中学2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高二上学期期中考试化学试题(已下线)题型139 沉淀溶解平衡及其影响因素上海市上海中学2023-2024学年高二上学期期中考试化学试题
11-12高二上·江西·期中
名校
4 . 硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
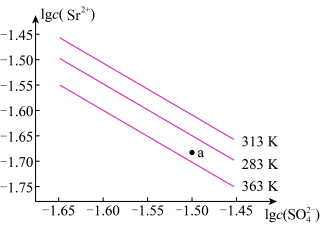

| A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 |
| B.三个不同温度中,363K时Ksp(SrSO4)最大 |
| C.283K时,图中a点对应的溶液是不饱和溶液 |
| D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
您最近一年使用:0次
2016-12-08更新
|
588次组卷
|
14卷引用:2011-2012学年江西省白鹭洲中学高二上学期期中考试化学(理)试卷
(已下线)2011-2012学年江西省白鹭洲中学高二上学期期中考试化学(理)试卷(已下线)2014秋江西省吉安市白鹭洲中学高二上学期期中化学试卷(已下线)2011-2012学年广东省深圳高级中学高二下学期期中化学试卷(已下线)2012-2013学年山东省聊城市某重点中学高二第四次模块检测化学试卷(已下线)2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷2016届山东省枣庄八中南校区高三上学期10月阶段测化学试卷2016届湖南长沙市长郡中学三上学期第四次月考化学试卷2016-2017学年广西柳州铁路一中高二上段考理化学卷黑龙江省齐齐哈尔市第八中学2017-2018学年高二12月月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】广东省深圳市耀华实验学校2018届高三上学期期末考试化学试题云南省会泽县茚旺高级中学2018-2019学年高二上学期12月月考化学试题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期1月月考化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
5 . 下列说法正确的是
| A.用冰醋酸、蒸馏水和容量瓶等可以配制pH=1的醋酸溶液 |
| B.在氨水中加入少量的水或氯化铵固体后,都会使溶液中的c(H+)增大 |
| C.反应SiO2(s)+ 3C(s)="SiC(s)" + 2CO(g)室温下不能自发进行,则该反应的△H<0 |
| D.对于Ca(OH)2的沉淀溶解平衡,升高温度,Ca(OH)2的溶解速率增大,Ksp减小 |
您最近一年使用:0次
2016-05-30更新
|
166次组卷
|
3卷引用:江西省高安二中2018-2019学年高二上学期期中考试化学试题
6 . 下列叙述正确的是( )
| A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B.25 ℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7 |
| C.25 ℃时,0.1 mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
| D.0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中c(Cl-)=c(I-) |
您最近一年使用:0次
2016-04-13更新
|
1965次组卷
|
42卷引用:2015-2016学年江西省临川十中高二上学期12月月考化学试卷
2015-2016学年江西省临川十中高二上学期12月月考化学试卷2015年全国普通高等学校招生统一考试化学(重庆卷)2016届西藏拉萨中学高三上学期第二次月考化学试卷2016届江苏省淮安市四星级高中高三上学期10月阶段测化学试卷2015-2016学年湖南省株洲二中高二上学期期末化学试卷2015-2016学年四川省双流中学高二下3月月考化学试卷2016届山西省平遥中学高三第二轮训练三化学试卷2017届河北省沧州一中高三上10.6周测化学试卷2017届西藏自治区拉萨中学高三上第一次月考化学卷2016-2017学年河北省冀州中学高二上期中化学卷河南省濮阳市2016-2017学年高二下学期升级(期末)考试(A卷)化学试题河北省鸡泽县第一中学2017-2018学年高二上学期期中考试化学试题福建省福州市2016-2017学年高二上学期期中考试化学试题陕西师范大学附中2017-2018第一学期高二年级化学期中考试化学试题辽宁省辽阳2017-2018学年高二化学上学期期末考试题河南省安阳县第一高级中学2017-2018学年高二上学期第三次月考化学试卷辽宁省营口中学2017-2018学年高二上学期期末考试化学试题2018-2019学年鲁科版高中化学选修四:模块综合检测题(一)四川省内江铁路中学2019届高三上学期入学考试化学试题【全国百强校】西藏自治区拉萨中学2019届高三上学期第五次月考理科综合化学试题【全国百强校】黑龙江省大庆实验中学2017-2018学年高二上学期期末考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期末考试化学试题河北省秦皇岛市北戴河区树人中学2019-2020学年高二上学期第二次月考化学试题甘肃省张掖市高台县第一中学2018-2019学年高二上学期期末考试理科化学试题山东省济南外国语学校2019-2020学年高二下学期3月份“空中课堂”阶段性测试化学试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训湖南省怀化市辰溪县辰溪县第一中学2019-2020学年高二12月月考化学试题2020年北京高二下学期 复习模拟试题二(选修4人教版)湖南省长沙市雨花区2019-2020学年高二上学期期末考试化学(选考)试题湖北省宜昌市长阳土家族自治县第一高级中学2020-2021学年高二上学期期中考试化学试题重庆市云阳江口中学校2020-2021学年高二上学期第三次月考化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第三次月考化学试题山西省运城市临猗县临晋中学2020-2021学年高二上学期12月月考化学试题吉林省长春市第二十九中学2020-2021学年高二上学期期末考试化学试题吉林省梅河口市朝鲜族中学2020-2021学年高二下学期第一次月考化学试题(已下线)综合复习与测试(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)福建省莆田第二十五中学2021-2022学年高二上学期期末考试化学试题重庆市天星桥中学2021-2022学年高二上学期第二次月考化学试题天津市实验中学2022-2023学年高二上学期末考试化学试题 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷重庆市荣昌永荣中学校2021-2022学年高二上学期期末考试化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 下列实验操作及现象能够达到对应实验目的是
| 选项 | 实验操作及现象 | 实验目的 |
| A | 将SO2通入品红溶液中,品红溶液褪色;加热褪色后的品红溶液,溶液恢复红色 | 验证亚硫酸的不稳定性 |
| B | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下 Ksp(BaCO3)>Ksp(BaSO4) |
| C | 常温下,测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水溶液中HCl电离程度大于CH3COOH |
| D | 将浓硫酸与碳混合加热,直接将生成的气体通入足量的石灰水,石灰水变浑浊 | 检验气体产物CO2的存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-03-02更新
|
246次组卷
|
5卷引用:2016届江西师范大学附属中学高三上学期期末化学试卷
2016届江西师范大学附属中学高三上学期期末化学试卷(已下线)2013届山东省济南市高三3月模拟考试理综化学试卷2017届陕西省西安一中高三上期中化学试卷四川省雅安中学2018届高三下学期第一次月考化学试题2020届高三化学选修4二轮专题练——沉淀溶解平衡的影响因素及应用【精编23题】
名校
解题方法
8 . 下列实验能达到预期目的的是 ( )
| 编号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp: Mg(OH)2 >Fe(OH)3 |
| D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2015-09-30更新
|
434次组卷
|
11卷引用:2016届江西省吉水中学三校高三上第一次联考化学试卷
2016届江西省吉水中学三校高三上第一次联考化学试卷2016届江西省九江市七校高三第一次联考化学试卷(已下线)2013-2014四川绵阳中学实验学校高考冲刺理综化学试卷2015-2016学年湖南省浏阳一中高二上第三次月考化学试卷2015-2016学年安徽省安庆市怀宁县高河中学高二上期末化学试卷2016届湖南省株洲市高三3月高考模拟理综化学试卷2016届安徽省六安一中高三下学期适应性考试理综化学试卷2017届河北省沧州一中高三上10.6周测化学试卷2016-2017学年辽宁省盘锦高中高二上期中化学卷【懂做原理题】2020届高三化学选修4二轮专题练——盐类水解平衡及其影响因素【精编25题】福建省泰宁第一中学2020届高三上学期第二次阶段考试化学试题
名校
解题方法
9 . 下列实验现象与结论不一致的是
| 实验操作(或设计) | 实验现象 | 结论 | |
| A | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | 酸性:HB > HA |
| B | 以镁、铝、氢氧化钠溶液构成原电池 | 镁表面有气泡 | 镁作原电池的负极 |
| C | 相同温度下,等质量的大理石与等体积等浓度的盐酸反应 | 粉状大理石产生气泡更快 | 反应速率: 粉状大理石>块状大理石 |
| D | 向盛有10滴0.1 mol·L-1AgNO3溶液的试管中滴加0.1 mol·L-1NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol·L-1NaI溶液 | 先有白色沉淀,后转成黄色沉淀 | Ksp(AgCl )> Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2015-08-27更新
|
349次组卷
|
4卷引用:2016届江西省赣中南五校高三下学期第二次段考化学试卷
名校
10 . 相关物质的溶度积常数见下表(25℃):
下列有关说法中不正确的是
物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
Ksp(单位略) | 1.1×10—11 | 2.3×10﹣3 | 1.8×10﹣10 | 1.9×10﹣12 |
| A.浓度均为0.2 mol•L﹣1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.将0.001 mol•L﹣1的AgNO3溶液滴入0.001 mol•L﹣1的KCl和0.001 mol•L﹣1 的K2CrO4混合溶液中.先产生Ag2CrO4沉淀 |
| C.0.11 mol•L﹣1的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 |
| D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
您最近一年使用:0次
2015-07-03更新
|
523次组卷
|
2卷引用:江西省南昌市第二中学2017-2018学年高二上学期第三次月考化学试题



