13-14高一·全国·课时练习
名校
解题方法
1 . 结合元素周期表回答下列问题:
(1)下图中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界___________ 。

(2)周期表中所列元素 ,属于短周期元素的有
,属于短周期元素的有__________ 种,属于主族元素的有__________ 种;g元素位于第__________ 周期第__________ 族;i元素位于第__________ 周期第__________ 族。
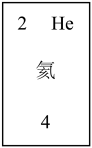
(3)f元素位于第__________ 周期第__________ 族,原子结构示意图为__________ 请在下图方框中按氦元素的式样写出该元素的原子序数,元素符号、元素名称、相对原子质量__________ 。

(1)下图中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界

(2)周期表中所列元素
 ,属于短周期元素的有
,属于短周期元素的有(3)f元素位于第


您最近一年使用:0次
2020-10-02更新
|
581次组卷
|
13卷引用:河北深州市长江中学2019-2020学年高一下学期第一次月考化学试题
河北深州市长江中学2019-2020学年高一下学期第一次月考化学试题(已下线)2014学年高一化学人教版必修2 1.1.1元素周期表练习卷山东峨山一中2018年3月高一月考(化学试卷)峨山县第一中学2017-2018学年第二学期3月份月考卷(高二化学)2017-2018学年鲁科版高一化学必修二第一章第二节基础题2019—2020学年人教版必修2第一章 第一节《元素周期表》第1课时 《元素周期表》(跟踪训练)苏教版高一化学必修2专题一第一单元第三课时《元素周期表》课时训练(夯实基础)(已下线)4.1.1 原子结构 元素周期表 核素练习(2)——《高中新教材同步备课》(人教版 必修第一册)人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第一节 原子结构与元素周期表 教材帮广东省东莞市光明中学2020-2021学年高二上学期期初考试化学试题(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)4.1.2 元素周期表(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.1.2 元素周期表-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
名校
2 . 下表是元素周期表的一部分,其中甲~戊共五种元素,回答下列问题:
(1)五种元素最高价氧化物对应的水化物中酸性最强的是______ 填化学式,下同),显两性的是_____ 。
(2)乙与丙按原子数 1:1 形成的一种化合物,其电子式为_____ ,该化合物固态时所属晶体类型为_____ ,所含化学键类型有_________ 。
(3)乙、丙、丁三种元素分别形成简单离子,按离子半径从大到小的顺序排列为_____ (用离子符号表示)。
(4)有人认为,元素甲还可以排在第ⅦA族,理由是它们的负化合价都是_____ ;也有人认为,根据元素甲的正、负化合价代数和为零,也可以将元素甲排在第_________ 族。
(5)甲与丙两种元素形成的化合物与水反应,生成—种可燃性气体单质,该反应的化学方程式为_____ 。
(6)通常状况下,1g甲的单质在戊的单质中燃烧放热92kJ,写出该反应的热化学方程式_____
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | 甲 | ||||||
| 2 | 乙 | ||||||
| 3 | 丙 | 丁 | 戊 |
(1)五种元素最高价氧化物对应的水化物中酸性最强的是
(2)乙与丙按原子数 1:1 形成的一种化合物,其电子式为
(3)乙、丙、丁三种元素分别形成简单离子,按离子半径从大到小的顺序排列为
(4)有人认为,元素甲还可以排在第ⅦA族,理由是它们的负化合价都是
(5)甲与丙两种元素形成的化合物与水反应,生成—种可燃性气体单质,该反应的化学方程式为
(6)通常状况下,1g甲的单质在戊的单质中燃烧放热92kJ,写出该反应的热化学方程式
您最近一年使用:0次
名校
3 . 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力,2016年IUPAC确认了4种新元素,其中一种为115号元素锁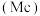 ,它与氮
,它与氮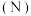 、磷
、磷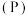 为同族元素。回答下列问题:
为同族元素。回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为______ ;Mc元素的一种核素X可由反应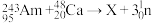 得到,X原子核内的中子数为
得到,X原子核内的中子数为______ 。
(2) 和
和 的结构与性质相似,
的结构与性质相似, 的电子式为
的电子式为______ ; 与HCl反应所得产物中含有的化学键类型为
与HCl反应所得产物中含有的化学键类型为______ 。下列性质的比较中,不能说明N的非金属性强于P的是______  填序号
填序号 。
。
a.熔点: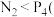 白磷
白磷
b.稳定性:
c.酸性:
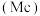 ,它与氮
,它与氮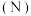 、磷
、磷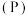 为同族元素。回答下列问题:
为同族元素。回答下列问题:(1)
 元素在周期表中的位置为
元素在周期表中的位置为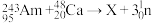 得到,X原子核内的中子数为
得到,X原子核内的中子数为(2)
 和
和 的结构与性质相似,
的结构与性质相似, 的电子式为
的电子式为 与HCl反应所得产物中含有的化学键类型为
与HCl反应所得产物中含有的化学键类型为 填序号
填序号 。
。a.熔点:
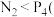 白磷
白磷
b.稳定性:

c.酸性:

您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分,回答有关问题。

(1)写出元素符号:①___ ,⑥___ 。
(2)在这些元素中,最活泼的金属元素的原子结构示意图为___ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为___ 。
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为___ (填离子符号)。
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有___ 。
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:___ 。

(1)写出元素符号:①
(2)在这些元素中,最活泼的金属元素的原子结构示意图为
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
2020-07-12更新
|
259次组卷
|
5卷引用:河北省重点中学2019-2020学年高一下学期期末考试化学试题
解题方法
5 . 下表为元素周期表的一部分
回答下列问题:
(1)Z元素在周期表中的位置为____ ,其氢化物的化学式____ ,其水溶液是___ 酸(填强或弱)
(2)表中元素原子半径最大的是(写元素符号)______ ,其氧化物化学式_____
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是____ 。
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol Y单质比1mol S得电子多
C.Y和S两元素的简单氢化物受热分解,前者的分解温度高
| 碳 | 氮 | Y | |
| X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为
(2)表中元素原子半径最大的是(写元素符号)
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol Y单质比1mol S得电子多
C.Y和S两元素的简单氢化物受热分解,前者的分解温度高
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分,用化学用语回答下列问题:
(1)③的元素符号为___ ,元素④与⑦形成化合物的电子式为___ 。
(2)比较元素①和⑥的原子半径大小:①___ (填“>”或“<”)⑥
(3)元素⑥的离子结构示意图为___ 。
(4)元素①和⑧形成的化合物中含有的化学键为___ 。
(5)元素②、⑤的最高价氧化物对应的水化物之间反应的离子方程式为___ 。
(6)工业上冶炼元素⑥的单质的化学方程式为___ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③的元素符号为
(2)比较元素①和⑥的原子半径大小:①
(3)元素⑥的离子结构示意图为
(4)元素①和⑧形成的化合物中含有的化学键为
(5)元素②、⑤的最高价氧化物对应的水化物之间反应的离子方程式为
(6)工业上冶炼元素⑥的单质的化学方程式为
您最近一年使用:0次
名校
7 . 下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
解题方法
8 . 如图是元素周期表的框架图,请回答下列问题:
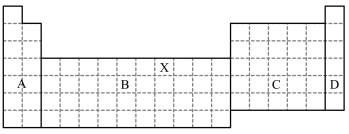
(1)写出元素X在周期表中位置___ 。
(2)若将此元素周期表分为A、B、C、D区,其中全部是金属元素的区域为___ 区。
(3)所含元素最多的周期是__ ,所含元素最多的族是__ 。
(4)硬度最大的单质是__ ,密度最小的金属是___ 。(用物质的名称填写)
(5)在原子序数为1~18号元素中,请用化学式填写。
与水反应最剧烈的金属元素是__ ;与酸、碱都反应的金属是__ ;最高价氧化物对应水化物酸性最强的酸是__ ;具有四核18个电子且含有非极性键的一种化合物是____ 。

(1)写出元素X在周期表中位置
(2)若将此元素周期表分为A、B、C、D区,其中全部是金属元素的区域为
(3)所含元素最多的周期是
(4)硬度最大的单质是
(5)在原子序数为1~18号元素中,请用化学式填写。
与水反应最剧烈的金属元素是
您最近一年使用:0次
名校
解题方法
9 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。

回答下列问题:
(1)写出元素f的基态原子核外电子排布式:__ 。
(2)写出元素h的基态原子核外电子轨道表示式:__ 。
(3)ci2分子的电子式为__ 。
(4)第一电离能:h__ (填“>”“<”或“=”,下同)i;电负性:g__ b。
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的叙述正确的是__ (填字母)。
A.j位于元素周期表中第4周期ⅠB族,属于ds区元素
B.d的基态原子中,2p轨道为半充满,属于p区元素
C.最外层电子排布式为4s1,该元素一定属于第ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是第ⅢA族或ⅢB族

回答下列问题:
(1)写出元素f的基态原子核外电子排布式:
(2)写出元素h的基态原子核外电子轨道表示式:
(3)ci2分子的电子式为
(4)第一电离能:h
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的叙述正确的是
A.j位于元素周期表中第4周期ⅠB族,属于ds区元素
B.d的基态原子中,2p轨道为半充满,属于p区元素
C.最外层电子排布式为4s1,该元素一定属于第ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是第ⅢA族或ⅢB族
您最近一年使用:0次
2020-05-05更新
|
182次组卷
|
2卷引用:河北省保定市崇德实验中学2020-2021学年度高二下学期期中考试化学试题
名校
解题方法
10 . 下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____ ,金属性最强的元素的名称是____ 。
(2)③、④、⑥三种元素中的原子半径最小的是_____________ (填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是________ (用离子符号填写)。
(4)④与⑥形成的化合物的电子式为_____________ 。
(5)④与氢形成含氢量最高的化合物的结构式____________ 。
(6)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是
(2)③、④、⑥三种元素中的原子半径最小的是
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是
(4)④与⑥形成的化合物的电子式为
(5)④与氢形成含氢量最高的化合物的结构式
(6)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次



