1 . (1)第ⅢB族有__ 种元素,第117号元素属于__ 元素(填“金属”或“非金属”);
(2)第5周期第ⅤA族元素的元素名称为__ ,原子序数为__ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为__ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
您最近一年使用:0次
解题方法
2 . 根据元素周期表回答下列问题:
(1)自然界稳定存在的元素中,金属性最强的元素是__ ,非金属性最强的元素是__ 。
(2)在稳定存在的碱金属元素中,最高价氧化物对应水化物的碱性最强的是__ 。
(3)卤族元素中,氢化物热稳定性最强的是__ 。
(1)自然界稳定存在的元素中,金属性最强的元素是
(2)在稳定存在的碱金属元素中,最高价氧化物对应水化物的碱性最强的是
(3)卤族元素中,氢化物热稳定性最强的是
您最近一年使用:0次
名校
解题方法
3 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在③~⑦元素中,原子半径最大的是__________ (填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________ ;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________ 。
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是________ (填离子符号)
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________ (填物质化学式);呈两性的氢氧化物是_________ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________ 。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)用电子式表示元素③与⑨形成化合物的过程
您最近一年使用:0次
2020-04-13更新
|
1066次组卷
|
6卷引用:黑龙江省鹤岗市第一中学2019-2020学年高一下学期4月月考化学试题
4 . 下表为元素周期表中的一部分,表中列出了11种元素在周期表中的位置,按要求完成下列各小题。
I. (1)化学性质最不活泼的元素是_____ (填元素符号,下同),非金属性最强的元素是_____ 。金属性最强的单质与水反应的离子方程式是________ 。
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式是____ 。
(3)①②③三种元素的原子半径由大到小的顺序是____ >____ >_____ 。
(4)某元素的最高价氧化物对应的水化物既能与酸反应生成盐和水又能和碱反应生成盐和水,该元素为_____ 。在这两种盐中该元素的化合价为_____ ,该元素的最高价氧化物和盐酸反应的离子方程式为_______ 。向该元素和⑧号元素形成的化合物的溶液中,缓慢滴加氢氧化钠溶液至过量,产生的实验现象是_______ ,有关反应的化学方程式为_______ 。
II.下列物质:①N2②CO2③NH3④Na2O⑤Na2O2⑥ NaOH ⑦CaBr2⑧H2O2⑨NH4Cl⑩Ar
(1)既含有极性键又含有非极性键的是_______ ;(填序号,下同)
(2)含有非极性键的离子化合物是___________
(3)不含化学键的是___________
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑪ | |||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式是
(3)①②③三种元素的原子半径由大到小的顺序是
(4)某元素的最高价氧化物对应的水化物既能与酸反应生成盐和水又能和碱反应生成盐和水,该元素为
II.下列物质:①N2②CO2③NH3④Na2O⑤Na2O2⑥ NaOH ⑦CaBr2⑧H2O2⑨NH4Cl⑩Ar
(1)既含有极性键又含有非极性键的是
(2)含有非极性键的离子化合物是
(3)不含化学键的是
您最近一年使用:0次
名校
5 . 下表是元素周期表短周期的一部分:
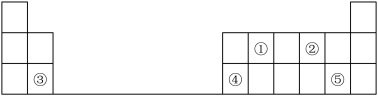
(1)①表示的元素名称是_________ ②对应简单离子结构示意图_______ 。
(2)③位于元素周期表中第________ 周期,第__________ 族。
(3)④的单质与 NaOH 溶液反应的离子方程式____________ 。
(4)⑤在自然界中有质量数为35和37的两种核素,该元素的相对原子质量为35.5,则两核素在自然界中的原子个数之比约为_______ 。

(1)①表示的元素名称是
(2)③位于元素周期表中第
(3)④的单质与 NaOH 溶液反应的离子方程式
(4)⑤在自然界中有质量数为35和37的两种核素,该元素的相对原子质量为35.5,则两核素在自然界中的原子个数之比约为
您最近一年使用:0次
2019-04-26更新
|
54次组卷
|
2卷引用:黑龙江省鹤岗市第一中学2020-2021学年高一上学期12月月考化学试题
名校
6 . 下图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼 的是___________________ (填元素符号),其⑤的离子结构示意图为____________________ 。
(2)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为____________ (填物质的化学式),酸性最强的化合物为________________ (填物质的化学式)。
(3)在②和③两种元素中,非金属性较强的是______ (填元素名称),②的某种单质可以和③的最高价氧化物的水化物反应,请写出有关化学方程式______________________________ 。
| 族/周期 | IA | IIA | III A | IVA | VA | VIA | VIIA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
(3)在②和③两种元素中,非金属性较强的是
您最近一年使用:0次
名校
7 . (1).短周期元素中,最外层电子数是次外层电子数3倍的元素是 ______ (填元素名称),某元素R的最高价氧化物的水化物的化学式为H2RO4,则其气态氢化物的化学式为 ________ ,等质量的H2O、D2O所含质子数之比为 ________ 。
(2)有下列物质:①O2、②SO3、③NaOH、④MgBr2、⑤HCl、⑥CF4、⑦NH4Cl
完全由第二周期元素形成的化合物为_____ (填序号,下同)。 由同主族元素形成的化合物是_____ 。 只含离子键的物质是_____ 。
(3) 用<、或>填空 稳定性比较 H2S_____ HF 还原性比较HBr_______ HI
(2)有下列物质:①O2、②SO3、③NaOH、④MgBr2、⑤HCl、⑥CF4、⑦NH4Cl
完全由第二周期元素形成的化合物为
(3) 用<、或>填空 稳定性比较 H2S
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分,回答下列有关问题:
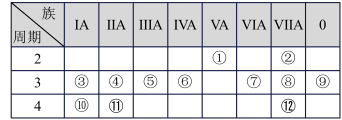
(1)画出原子的结构示意图:④______________
(2)在①~12元素中,金属性最强的元素是______ ,非金属性最强的元素是____ ,最不活泼的元素是_____ 。(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)元素⑤的最高价氧化物的水化物分别与元素③⑧的最高价氧化物的水化物反应的离子方程式_________ , _________
(5)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程:__________ 。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:______________________

(1)画出原子的结构示意图:④
(2)在①~12元素中,金属性最强的元素是
(3)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)元素⑤的最高价氧化物的水化物分别与元素③⑧的最高价氧化物的水化物反应的离子方程式
(5)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程:
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次
名校
9 . 按要求完成下列各题:
(1)微粒铵根14N2H4+中的中子数是___________________ ,核外电子数是_____ 。
(2)写出 N2的电子式_________________ ,画出HClO分子的结构式_________________
CO2的电子式________________ ;Na2O2的电子式为___________________
(3)如图是元素周期表的一个方格 ,其中19.00的意义是
,其中19.00的意义是______________
(4) 25℃,101 kPa,1g C2H2气体充分燃烧生成气体CO2和液态H2O,放出125kJ的热量,写出C2H2燃烧热的热化学方程式_________________
(1)微粒铵根14N2H4+中的中子数是
(2)写出 N2的电子式
CO2的电子式
(3)如图是元素周期表的一个方格
 ,其中19.00的意义是
,其中19.00的意义是(4) 25℃,101 kPa,1g C2H2气体充分燃烧生成气体CO2和液态H2O,放出125kJ的热量,写出C2H2燃烧热的热化学方程式
您最近一年使用:0次
名校
10 . 下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号或化学式 回答下列问题:
(1)化学性质最不活泼的元素是___________ ,氧化性最强的单质是_______ ,用一个化学反应证明H单质的氧化性强于G单质____________________________ 。
(2)D的最高价氧化物与I的最高价氧化物对应的水化物反应的离子方程式为_____________ 。
(3)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_______________ 。
(4)B、C、D、G、I离子半径由大到小的顺序是_______________________ 。
(5)用电子式表示化合物MgCl2的形成过程_________________________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | A | |||||||
2 | E | F | G | H | J | |||
3 | B | C | D | I |
根据A—J在周期表中的位置,用
(1)化学性质最不活泼的元素是
(2)D的最高价氧化物与I的最高价氧化物对应的水化物反应的离子方程式为
(3)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(4)B、C、D、G、I离子半径由大到小的顺序是
(5)用电子式表示化合物MgCl2的形成过程
您最近一年使用:0次



