解题方法
1 . 镁铝合金与钢在生产生活中有广泛的应用。
(1)地壳中含量最高的金属元素是___________ ,其单质的还原性比Na___________ (填“强”或“弱”)。
(2)镁铝合金比铝___________ (填“硬”或“软”),用足量的氢氧化钠溶液溶解镁铝合金,剩余的金属主要是___________ 。
(3)钢中含有的主要金属元素是___________ ,(填元素符号)该元素的单质粉末(过量)在氯气中加热,发生反应的化学方程式为___________ 。
(1)地壳中含量最高的金属元素是
(2)镁铝合金比铝
(3)钢中含有的主要金属元素是
您最近一年使用:0次
2022-10-07更新
|
144次组卷
|
2卷引用:黑龙江省佳木斯市第八中学2021-2022学年高一上学期期末考试化学试题
解题方法
2 . 完成下列问题
(1)写出Ni的元素名称_______ , 该元素在周期表的位置为第_______ 周期,第_______ 族。
(2)基态Si原子的电子排布式为_______ ,基态S原子的电子排布式为_______ 。
(3)写出基态Fe原子的价层电子排布式:_______ 。
(1)写出Ni的元素名称
(2)基态Si原子的电子排布式为
(3)写出基态Fe原子的价层电子排布式:
您最近一年使用:0次
解题方法
3 . 请根据构造原理,按要求写出下列电子排布式或原子结构示意图:
(1)16S的电子排布式___________ 。
(2)26Fe的简化电子排布式___________ 。
(3)某元素原子的电子排布式为[Ar]3d104s24p1,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第___________ 周期。
②该元素处于元素周期表的第___________ 族。
③试推测该元素处于元素周期表的___________ 区。
(1)16S的电子排布式
(2)26Fe的简化电子排布式
(3)某元素原子的电子排布式为[Ar]3d104s24p1,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第
②该元素处于元素周期表的第
③试推测该元素处于元素周期表的
您最近一年使用:0次
解题方法
4 . Ⅰ.回答下列问题
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是_______ 。
(2)已知某粒子的结构示意图为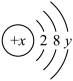 。
。
①当x-y=10时,该粒子为_______ (填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称)_______ 、_______ 、_______ 、_______ 、_______ 。
Ⅱ.结合元素周期表回答下列问题:
(3)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。_______
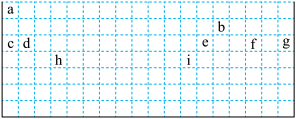
(4)表中所列元素,属于短周期元素的有_______ ,属于主族元素的有_______ 。
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是
(2)已知某粒子的结构示意图为
 。
。①当x-y=10时,该粒子为
②当y=8时,粒子可能为(填名称)
Ⅱ.结合元素周期表回答下列问题:
(3)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。

(4)表中所列元素,属于短周期元素的有
您最近一年使用:0次
5 . 已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
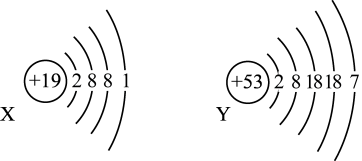
X:_______ ,Y:_______ 。

X:
您最近一年使用:0次
2022-04-28更新
|
561次组卷
|
2卷引用:黑龙江省七台河市第六中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
6 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第_______ 周期。
(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积_______ L。
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。_______
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为_______ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
您最近一年使用:0次
2022-04-20更新
|
384次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学2021-2022学年高一上学期期末考试化学试题
名校
7 . 下表是元素周期表的一部分,回答下列关问题:
(1)下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是_______ (填元素符号),简单离子半径最小的是_______ (填化学式)。
(3)④与⑧可以形成_______ (填离子或共价)化合物,请用电子式表示其形成过程:_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)第三周期中,原子半径最大的元素是
(3)④与⑧可以形成
您最近一年使用:0次
名校
8 . 下表为元素周期表的一部分,表中序号各代表某一元素。请回答下列问题。
(1)③的原子结构示意图是___________ 。
(2)①~⑨中非金属性最强的元素是___________ (填化学式)。
(3)①和⑨两种元素组成的化合物的电子式___________
(4)元素⑦和⑨组成的化合物中含有的化学键是___________ (填“共价键”或“离子键”)。
(5)元素①的名称为___________ 。
(6)元素⑤的最高价氧化物的水化物为___________ (填化学式)
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①~⑨中非金属性最强的元素是
(3)①和⑨两种元素组成的化合物的电子式
(4)元素⑦和⑨组成的化合物中含有的化学键是
(5)元素①的名称为
(6)元素⑤的最高价氧化物的水化物为
您最近一年使用:0次
2022-03-20更新
|
442次组卷
|
2卷引用:黑龙江省鸡西市英桥高级中学2021-2022学年高一下学期期中考试化学试题
名校
9 . 下表是元素周期表的一部分,根据表中给出10种元素(其中X、Y分别代表某种化学元素),按要求作答。
(1)X、Y两种元素符号分别是_______ 和_______ ;
(2)最外层电子数为4的原子,其元素符号是_______ ;
(3)保存在煤油中的金属是_______ ;
(4)化学性质最不活泼的单质是_______ ;
(5)HF与HCl热稳定性较强的是_______ ;
(6)NaOH与 碱性较强的是
碱性较强的是_______ ;
族 周期 | IA | IIA | ⅢA | IVA | VA | ⅥA | ⅦA | O |
| 2 | C | N | X | F | Ne | |||
| 3 | Na | Mg | Y | S | Cl |
(1)X、Y两种元素符号分别是
(2)最外层电子数为4的原子,其元素符号是
(3)保存在煤油中的金属是
(4)化学性质最不活泼的单质是
(5)HF与HCl热稳定性较强的是
(6)NaOH与
 碱性较强的是
碱性较强的是
您最近一年使用:0次
名校
解题方法
10 . 下表是元素周期表的一部分,①~⑦代表七种元素,它们在元素周期表中的位置如下。
请回答下列问题:
(1)元素⑥的原子结构示意图为___________ 。
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(3)②、③、④三种元素中,原子半径最小的是___________ (填元素符号)。
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为_______ 。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ |
请回答下列问题:
(1)元素⑥的原子结构示意图为
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是
(3)②、③、④三种元素中,原子半径最小的是
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为
您最近一年使用:0次



