名校
1 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第____ 周期第_____ 族,A、B、C三种元素原子半径从大到小的顺序是_________________ ;
(2)D简单离子的结构示意图为_____________ ,D、E中金属性较强的元素是________ 。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
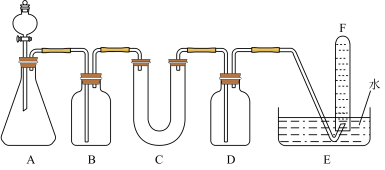
(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________ ;
(4)装置C中X与CO2反应的化学方程式是_____________________ ,装置D盛放NaOH溶液的作用是除去____________ ;
(5)为检验试管F收集的气体,进行____________ 操作,出现_________ 现象,即证明X可作供氧剂。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第
(2)D简单离子的结构示意图为

(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去
(4)装置C中X与CO2反应的化学方程式是
(5)为检验试管F收集的气体,进行
您最近一年使用:0次
2019-03-25更新
|
2348次组卷
|
8卷引用:黑龙江省哈尔滨市第三十二中学2021-2022学年高一上学期期末考试化学试题
2 . 下表是元素周期表的一部分,其中列出了①一⑥六种元素在周期表中的位置。
请回答下列问题:
(1)①的元素符号为_____________ ;④的元素符号为_____________ ;
(2)②的原子半径______ ⑤的原子半径(选填“>”、“<”或“=”);
(3)③和⑥两元素形成的化合物的化学式为_________ ;
(4)⑤的最高价氧化物对应的水化物的化学式为_________ ;
(5)③的单质与水反应的化学方程式为___________ 。
族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA |
2 | ① | ② | |||||
3 | ③ | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①的元素符号为
(2)②的原子半径
(3)③和⑥两元素形成的化合物的化学式为
(4)⑤的最高价氧化物对应的水化物的化学式为
(5)③的单质与水反应的化学方程式为
您最近一年使用:0次
名校
3 . 下表为元素周期表的一部分,请回答有关问题:
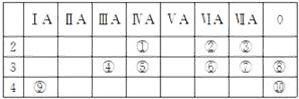
(1)⑤和⑧的元素符号是________ 和________ (填写元素符号,下同);
(2)表中最活泼的金属是________ ,非金属最强的元素是________ ;
(3)⑥的最高正价是________ 。
(4)⑦和⑩单质氧化性________ 强(填写元素符号);

(1)⑤和⑧的元素符号是
(2)表中最活泼的金属是
(3)⑥的最高正价是
(4)⑦和⑩单质氧化性
您最近一年使用:0次
名校
解题方法
4 . 下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白。
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___ 。
(2)④与⑤两种元素相比较,原子半径较大的是___ (填元素符号);在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是___ (填化学式)。在金属元素氧化物所对应的水化物中,碱性最强的化合物是___ (填化学式),具有两性的化合物是___ (填化学式)。
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为___ (填化学式)。
(4)元素①和元素⑦形成化合物属于___ 化合物(填“离子”或者“共价”)。请用电子式表示⑥和④组成化合物的形成过程:________ 。
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:______________ 。
| 主族\周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)④与⑤两种元素相比较,原子半径较大的是
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为
(4)元素①和元素⑦形成化合物属于
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:
您最近一年使用:0次
名校
5 . 如图是元素周期表的一部分,回答下列问题:
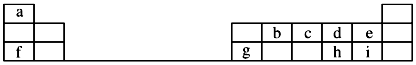
 元素e的负一价离子的结构示意图为
元素e的负一价离子的结构示意图为 ______ ,f、g、h、i对应简单离子的半径由大到小的顺序为 ______  用具体微粒符号表示
用具体微粒符号表示 .
.
 元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为
元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为 ______ .
 、c、d三种原子的第一电离能大小顺为
、c、d三种原子的第一电离能大小顺为 ______  用具体微粒符号表示
用具体微粒符号表示 .
.

 元素e的负一价离子的结构示意图为
元素e的负一价离子的结构示意图为  用具体微粒符号表示
用具体微粒符号表示 .
. 元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为
元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为 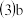 、c、d三种原子的第一电离能大小顺为
、c、d三种原子的第一电离能大小顺为  用具体微粒符号表示
用具体微粒符号表示 .
.
您最近一年使用:0次
名校
6 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)9种元素中,化学性质最不活泼的是______ ,原子结构示意图为____________ 。
(2)这些元素中,最高价氧化物的水化物中碱性最强的碱是__________ ,写出元素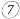 的单质与其反应的离子方程式:
的单质与其反应的离子方程式:___________________________________ 。
(3)最高价氧化物是两性氧化物的元素是______ ,写出它的氧化物与NaOH溶液反应的化学反应方程式: ____________________________________ 。
(4)用电子式表示元素 和
和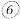 组成的化合物的形成过程
组成的化合物的形成过程 _____________________________ ,该化合物属于 ______ (填“共价”或“离子” 化合物。
化合物。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 |  |  | ||||||
| 三 |  |  | 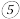 | 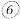 | 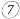 |  | ||
| 四 | 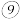 |
(1)9种元素中,化学性质最不活泼的是
(2)这些元素中,最高价氧化物的水化物中碱性最强的碱是
 的单质与其反应的离子方程式:
的单质与其反应的离子方程式:(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素
 和
和 组成的化合物的形成过程
组成的化合物的形成过程  化合物。
化合物。
您最近一年使用:0次
2018-05-22更新
|
181次组卷
|
2卷引用:【全国百强校】黑龙江省大庆中学2017-2018学年高一下学期期中考试化学试题
名校
7 . (1)第ⅢB族有_____ 种元素,第117号元素属于_________ 元素(填“金属”或“非金属”);
(2)第5周期第ⅤA族元素的元素名称为_________ ,原子序数为_______ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为_______ ;
(4)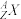 和
和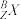 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则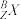 的相对原子质量为
的相对原子质量为___________ ,元素X的近似相对原子质量为______________________ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
(4)
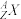 和
和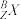 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则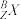 的相对原子质量为
的相对原子质量为
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分,针对表中的①~⑩中10种元素回答以下问题:

Ⅰ.填写下列空白:
(1)写出⑧元素在周期表的位置______________________ ;
(2)实验室制取②氢化物的化学方程式_______________________________________ ;
②的氢化物与其最高价氧化物水化物反应生成的物质是________________ (填名称)
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是________ (填“共价化合物”或“离子化合物”),可以证明你判断正确的实验依据为:_____________________________________________________________________ 。
(4)用电子式表示④、⑥两元素结合成化合物的形成过程____________________________ 。
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂;X是一种氢化物,常温下为液体,则:
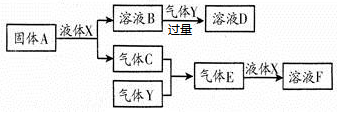
(1)A的电子式为_________________ ;
(2)气体Y是一种大气污染物,无色有刺激性气味,直接排放会形成酸雨。写出溶液D与酸性高锰酸钾溶液反应的离子方程式:_________________________________________ ;
(3)在含2molF的浓溶液中加入1mol锌片加热使之充分反应,产生气体的体积为_____ L(标准状况下)

Ⅰ.填写下列空白:
(1)写出⑧元素在周期表的位置
(2)实验室制取②氢化物的化学方程式
②的氢化物与其最高价氧化物水化物反应生成的物质是
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是
(4)用电子式表示④、⑥两元素结合成化合物的形成过程
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂;X是一种氢化物,常温下为液体,则:

(1)A的电子式为
(2)气体Y是一种大气污染物,无色有刺激性气味,直接排放会形成酸雨。写出溶液D与酸性高锰酸钾溶液反应的离子方程式:
(3)在含2molF的浓溶液中加入1mol锌片加热使之充分反应,产生气体的体积为
您最近一年使用:0次
名校
9 . (1)下图所示元素周期表中全部是金属元素的区域为___________
A.A B.B C.C D.D
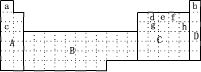
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。______________
②甲、乙两元素相比较,金属性较强的是_________ (填名称),可以验证该结论的实验是_______ 。
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出B的电子式:______ ,比较C、B、D结合氢离子的能力由强到弱的顺序为_________________ (用化学式表示)。
(4)上表中c、h元素形成的简单离子半径之比________ 1(填〉或〈或 =)。
A.A B.B C.C D.D

(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出B的电子式:
(4)上表中c、h元素形成的简单离子半径之比
您最近一年使用:0次
2018-04-13更新
|
505次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2017-2018学年高一4月月考化学试题1
名校
10 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________ 周期________ 族。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为_______________ 。
(3)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:________________ 。
(4)写出3p轨道上有2个未成对电子的元素的符号:____________ 。
(5)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为
(3)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(4)写出3p轨道上有2个未成对电子的元素的符号:
(5)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
您最近一年使用:0次



