解题方法
1 . 下图是元素周期表的一部分。按要求填写下列空白:
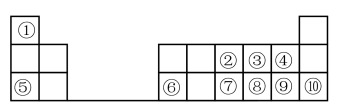
(1)元素⑦在周期表中的位置可表示为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物的电子式为_______ ;⑧的氢化物的结构式为_______
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置可表示为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物的电子式为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2022-12-21更新
|
351次组卷
|
2卷引用:山东省临沂滨河高级中学2022-2023学年高一上学期线上期末考试化学试题
解题方法
2 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:_______ 周期_______ 族。
(2)X原子在第二电子层上只有一个空轨道,则X是_______ ;其轨道表示式为_______ 。
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:_______ 。
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_______ 。
(5)写出3p轨道上有2个未成对电子的元素符号:_______ 。
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:_______ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)X原子在第二电子层上只有一个空轨道,则X是
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:
(5)写出3p轨道上有2个未成对电子的元素符号:
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:
您最近一年使用:0次
2022-12-20更新
|
290次组卷
|
2卷引用:山东省威海市文登新一中2021-2022学年高二上学期期中考试化学试题
解题方法
3 . I. 下面是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:
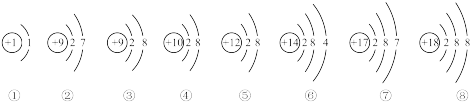
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是_______ ;在化学反应中容易得到电子的是_______ ;属于阳离子的是_______ ;表示F-离子的是_______ ;属于同一种元素的是_______ ;属于非金属元素的是_______ ;电子层数相同,最外层电子数也相同的粒子有_______ ;能与①形成AB4型分子的是_______ 。
II.某微粒的结构示意图可表示为
(2)当x=10+y时,该粒子为_______ (填“原子”、“阳粒子”或“阴离子”),当x<10+y时,该粒子为_______ 。
(3)当y=2时x=_______ 。该元素能形成的离子符号为_______ 。
(4)若该结构示意图表示的粒子是R-,则x=_______ ,y=_______ 。
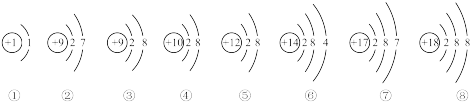
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是
II.某微粒的结构示意图可表示为

(2)当x=10+y时,该粒子为
(3)当y=2时x=
(4)若该结构示意图表示的粒子是R-,则x=
您最近一年使用:0次
4 . 某学习小组探究B及其化合物的性质。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。
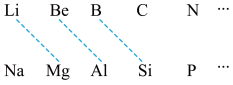
B在元素周期表中的位置是_______ 。其最高价氧化物的化学式为_______ ,与氢氧化钠溶液反应的化学方程式为_______ 。
(2)某科研团队研究发现硼氢化钠( )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
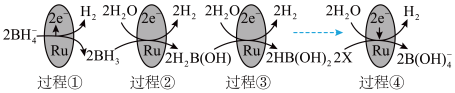
①上图中X的化学式为_______ 。
② 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用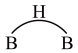 表示,则二聚物结构式为
表示,则二聚物结构式为_______ 。
③图中反应的总化学方程式为_______ 。
④_______ g 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。

B在元素周期表中的位置是
(2)某科研团队研究发现硼氢化钠(
 )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
①上图中X的化学式为
②
 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用 表示,则二聚物结构式为
表示,则二聚物结构式为③图中反应的总化学方程式为
④
 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
您最近一年使用:0次
名校
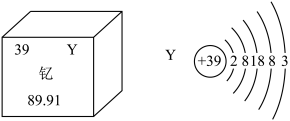
5 . 新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:_______ 个质子,左图中89.91表示的是_______ ;
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据_______ 个电子层;
(3)钇元素形成氧化物的化学式是_______ 。
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据
(3)钇元素形成氧化物的化学式是
您最近一年使用:0次
2022-10-08更新
|
327次组卷
|
3卷引用:山东省滨州惠民文昌中学2023-2024学年高一下学期第一次月考化学试题
6 .  、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,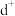 中各层电子数都是
中各层电子数都是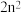 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物_______ 。
 、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,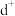 中各层电子数都是
中各层电子数都是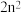 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物
您最近一年使用:0次
名校
7 . 近年来,我国航空航天事业成果显著,“北斗三号”导航卫星搭载了精密计时的铷(Rb)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图1)。回答下列问题:

(1)下列说法错误的是_______(填字母)。
(2)Rb原子第一电子层上电子的能量比最外层上电子的能量_______ (填“低”或“高”)。
(3)如图2中 所示粒子共表示
所示粒子共表示_______ 种元素,铷元素原子的化学性质与如图中_______ (填字母)的化学性质相似。


(1)下列说法错误的是_______(填字母)。
A.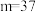 , ,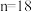 | B.铷是金属元素 |
| C.铷的相对原子质量是85.47 | D.铷原子有5个电子层,最外层有1个电子 |
(3)如图2中
 所示粒子共表示
所示粒子共表示
您最近一年使用:0次
2022-09-07更新
|
378次组卷
|
3卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题
名校
8 . 回答下列问题:
(1)鉴于 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(2)甲元素 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
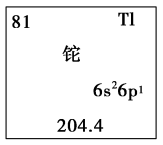
(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。
(1)鉴于
 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的(2)甲元素
 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。

| A.铊元素在元素周期表中的位置是第六周期第ⅡA族 |
B.铊原子的中子数为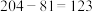 |
| C.铊原子有6个电子层,最外电子层上有3个电子 |
| D.铊元素的金属性比铝元素的强 |
您最近一年使用:0次
9 . 废旧太阳能电池具有较高的回收利用价值,其主要组成CIGS的化学式可写为CuIn0.5Ga05Se2;回答下列问题:
(1)Cu在元素周期表中属于_______ 分区。同周期元素基态原子中与其未成对电子数相同的原子还有_______ (写元素名称)。
(2)Ga、In与Al同主族,写出Ga基态原子电子排布式_______ 。
(3)Ga、Se与As同周期,推测这三种元素第一电离能由大到小的顺序_______ (用元素符号表示),推测的理由是_______ 。
(4)CIGS含有的四种元素中电负性最强的是_______ (用元素符号表示),Cu的化合价为_______ 。
(1)Cu在元素周期表中属于
(2)Ga、In与Al同主族,写出Ga基态原子电子排布式
(3)Ga、Se与As同周期,推测这三种元素第一电离能由大到小的顺序
(4)CIGS含有的四种元素中电负性最强的是
您最近一年使用:0次
10 . 在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
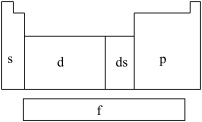
(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为___________ ,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近一年使用:0次
2021-12-04更新
|
555次组卷
|
9卷引用:山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题
山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)同步君 选修3 第一章 第二节 原子结构与元素周期表高中化学人教版 选修三 第1章 原子结构与性质 原子结构与元素周期表(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)1.2.1 原子结构与元素周期表(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第1课时 原子核外电子排布的周期性2.2.1原子核外电子排布的周期性 课后



