1 . 根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有________ 种,金属性最强的元素与氧反应生成的化合物有(填两种化合物的化学式)________ 、___________ 。
(2)属于稀有气体元素的是(填元素符号,下同)_____________ 。
(3)形成化合物种类最多的两种元素是_________ 、_________ 。
(4)推测Si、N最简单氢化物的稳定性:________ 大于________ (填化学式)。
(1)属于金属元素的有
(2)属于稀有气体元素的是(填元素符号,下同)
(3)形成化合物种类最多的两种元素是
(4)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次
解题方法
2 . 下表是元素周期表短周期的一部分,请参照元素①~⑨在表中的位置,回答下列问题。

(1)元素②在周期表中的位置是______________ 。
(2)元素⑤和⑨形成的化合物的电子式为__________________ 。
(3)元素④、⑤、⑥形成的简单离子的半径依次__________________ (填“增大”“减小”或“不变”)。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是_____________ (填化学式)。
(5)元素⑥形成的单质可与⑤的最高价氧化物对应的水化物发生反应,其反应的离子方程式为___________
(6)在一定条件下,①与③可形成一种化合物X,其相对分子质量与O2相同,且X可在纯氧中燃烧,所得产物对环境均无污染,则X燃烧的化学方程式为________________

(1)元素②在周期表中的位置是
(2)元素⑤和⑨形成的化合物的电子式为
(3)元素④、⑤、⑥形成的简单离子的半径依次
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(5)元素⑥形成的单质可与⑤的最高价氧化物对应的水化物发生反应,其反应的离子方程式为
(6)在一定条件下,①与③可形成一种化合物X,其相对分子质量与O2相同,且X可在纯氧中燃烧,所得产物对环境均无污染,则X燃烧的化学方程式为
您最近一年使用:0次
2020-07-14更新
|
122次组卷
|
2卷引用:河南省郑州市2019-2020学年高一下学期期末考试化学试题
名校
3 . 2019年是化学元素周期表问世150周年,联合国宣布此年为“国际化学元素周期表年”。元素周期表在学习、研究中有很重要的作用,下表是元素周期表的一部分。
(1)e的元素符号是___ 。
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是___ 。
(3)c的金属性强于d的金属性,用原子结构解释原因:___ ,失电子能力c大于d。
(4)下列对于a及其化合物的推断中,正确的是___ (填序号)。
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g |
(1)e的元素符号是
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是
(3)c的金属性强于d的金属性,用原子结构解释原因:
(4)下列对于a及其化合物的推断中,正确的是
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
您最近一年使用:0次
2020-06-03更新
|
290次组卷
|
3卷引用:河南省范县第一中学等学校2021-2022学年高一上学期联考检测化学(A卷)试题
解题方法
4 . 元素周期表的形式多种多样,下图是扇形元素周期表的一部分,扇面的18折相当于中学化学常见长式元素周期表的18列,1、2、3、4相当于周期,针对表中所给元素,对照中学化学常见长式元素周期表,回答下列问题:
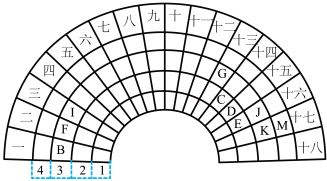
(1)表中金属性最强的元素在长式元素周期表中的位置是___________ ,该元素单质与水反应的化学方程式为______________ 。
(2)表中最高价氧化物对应的水化物酸性最强的是__________ (填酸的化学式)。
(3)元素F与K形成化合物的电子式为__________ 。
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式_________ 。
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式________ 。

(1)表中金属性最强的元素在长式元素周期表中的位置是
(2)表中最高价氧化物对应的水化物酸性最强的是
(3)元素F与K形成化合物的电子式为
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 下表中阿拉伯数字(1、2…)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)B、C两元素中非金属性较强的是____ (写出元素名称),I元素在周期表中的位置是_____ 。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式_______ 。
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式_____ ,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M,用电子式表示M的形成过程:____ 。
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式_______ 。
| 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)B、C两元素中非金属性较强的是
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,请写出Y的电子式
(4)表中某两种元素的气态单质可以形成燃料电池,其产物清洁无污染,请写出碱性环境中负极反应式
您最近一年使用:0次
6 . 如图是元素周期表的一部分,表中的①~⑩中元素,填空回答:
用元素符号 或化学式 回答下列问题:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______________ 。
(2)氧化性最强的单质是_____________ 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是_____________ ,碱性最强的是_____________ ,呈两性的氢氧化物是_____________ 。
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是_____________ ,
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
用
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)氧化性最强的单质是
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是
您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在③~⑦元素中,原子半径最大的是__________ (填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________ ;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________ 。
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是________ (填离子符号)
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________ (填物质化学式);呈两性的氢氧化物是_________ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________ 。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)用电子式表示元素③与⑨形成化合物的过程
您最近一年使用:0次
2020-04-13更新
|
1066次组卷
|
6卷引用:河南省新乡市辉县市第二高级中学2019-2020学年高二下学期期中考试化学试题
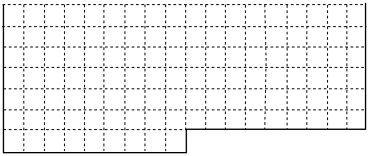
8 . (1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________ 。
(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)
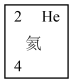
写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________ >________ (用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________
(4)元素周期表体现了元素周期律,即元素的性质随着_________ 的递增呈现____ 的变化。

(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)

写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:
(4)元素周期表体现了元素周期律,即元素的性质随着
您最近一年使用:0次
名校
解题方法
9 . 补充完成下表:(请把序号①~⑦的答案填在相应的位置上)
元素 | 甲 | 乙 | 丙 |
元素符号 | ① | ② | O |
原子结构示意图 |
| ③ | ④ |
周期 | 三 | 三 | ⑤ |
族 | ⑥ | ⅦA | ⑦ |
您最近一年使用:0次
10 . (1)原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
①A和B所属周期数之差为___________
②A和B的核电荷数之差为____________ (用含m、n的代数式表示)
③B和A的族序数之差为______________ (用含m、n的代数式表示)
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。回答下列问题:
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________ ;当B在A的下一周期时,B的原子序数为______________ ;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ 当B在A的下一周期时,B的原子序数为______________ 。
(3)某粒子的结构示意图为: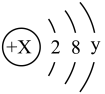 试回答:
试回答:
①当x-y=10时,该粒子为________ (填“原子”或“阳离子”“阴离子”)
②当y=8时,该粒子可能是(写名称):_______ 、________ 、_______ 、_______ 、_______ 。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式________________ 。
①A和B所属周期数之差为
②A和B的核电荷数之差为
③B和A的族序数之差为
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。回答下列问题:
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
(3)某粒子的结构示意图为:
 试回答:
试回答:①当x-y=10时,该粒子为
②当y=8时,该粒子可能是(写名称):
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式
您最近一年使用:0次
2020-02-19更新
|
180次组卷
|
2卷引用:河南省驻马店市正阳县高级中学2019-2020高二下学期第一次素质检测化学试题




