1 . 海水占地球总蓄水量的97.2%,若把海水的淡化和化工生产结合起来,就可充分利用海洋资源来解决淡水资源缺乏的问题。
(1)氯化钠中的金属元素在周期表中的位置是_________ ;
(2)目前常用的“海水淡化”主要技术之一是蒸馏法,蒸馏法属于________ (填“物理变化”或“化学变化”)。
(1)氯化钠中的金属元素在周期表中的位置是
(2)目前常用的“海水淡化”主要技术之一是蒸馏法,蒸馏法属于
您最近一年使用:0次
名校
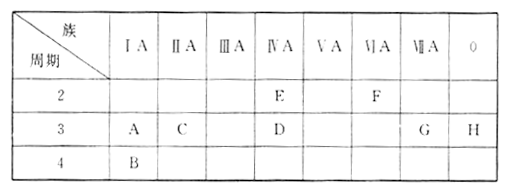
2 . 下表列出了 A〜H八种元素在周期表中的位置。
(1)这八种元素中化学性质最不活泼的是____________ (填元素符号)。
(2)A、B、G 种元素对应的简单离子半径由大到小的顺序为______________ (用离子符号表示)。
(3)F元素与氢元素能形成18电子的化合物,该化合物的化学式为_______________ 。 (4) C元素与G元素形成化合物的电子式是____________________ 。
(5)A、D两元素最高价氧化物对应的水化物之间发生反应的离子方程式为________________ 。
(1)这八种元素中化学性质最不活泼的是
(2)A、B、G 种元素对应的简单离子半径由大到小的顺序为
(3)F元素与氢元素能形成18电子的化合物,该化合物的化学式为
(5)A、D两元素最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
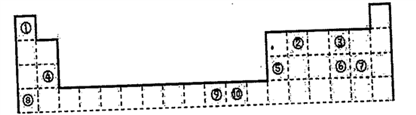
3 . 下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出元素⑤的原子轨道表示式______________ 。
(2)写出元素⑨的基态原子的价电子排布式_________ 。
(3)表中属于ds区的元素是_________ (填编号)
(4)元素⑩形成的单质是由____ 键形成的晶体,该晶体采取的堆积方式是_______ ,晶体中⑩元素原子的配位数是_________ 。
(5)元素④、⑤、⑥、⑦的离子半径由小到大的顺序是_______ (用离子符号表示)
(6)写出元素①和元素⑧形成化合物的电子式_________________ 。
(7)元素⑨与⑩的第二电离能分别为:I⑨=1753kJ/mol,I⑩=1959kJ/mol,第二电离能I⑨⑩的原因是____________________________ 。
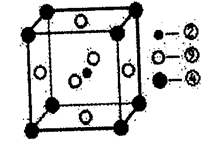
(8)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如下图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为______ (用对应的元素符号表示)。
(1)写出元素⑤的原子轨道表示式
(2)写出元素⑨的基态原子的价电子排布式
(3)表中属于ds区的元素是
(4)元素⑩形成的单质是由
(5)元素④、⑤、⑥、⑦的离子半径由小到大的顺序是
(6)写出元素①和元素⑧形成化合物的电子式
(7)元素⑨与⑩的第二电离能分别为:I⑨=1753kJ/mol,I⑩=1959kJ/mol,第二电离能I⑨⑩的原因是
(8)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如下图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为
您最近一年使用:0次
2017-04-26更新
|
363次组卷
|
2卷引用:河南省郑州市八校2016-2017学年高二下学期期中联考化学试题
4 . A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的﹣1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题:
(1)B元素在元素周期表中的位置是第______ 周期______ 族;
(2)画出C元素的原子结构示意图______ ;
(3)与E的氢化物分子所含电子总数相等的分子是______ (举一例,填化学式,下同)、阳离子是______ ;
(4)A与D形成的化合物中含有化学键的类型是_____ 。
(1)B元素在元素周期表中的位置是第
(2)画出C元素的原子结构示意图
(3)与E的氢化物分子所含电子总数相等的分子是
(4)A与D形成的化合物中含有化学键的类型是
您最近一年使用:0次
2017-04-26更新
|
395次组卷
|
2卷引用:河南省焦作市济源市第六中学2019-2020学年高二下学期第二次月考化学试题
5 . A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
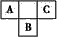
(1)A、B、C三种元素的名称分别为_______ 、_______ 、_______ 。
(2)B位于元素周期表中第_______ 周期,第_______ 族。
(3)C的单质与H2反应的化学方程式为_______
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式_______

(1)A、B、C三种元素的名称分别为
(2)B位于元素周期表中第
(3)C的单质与H2反应的化学方程式为
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分元素,用元素符号或化学式回答下列问题:
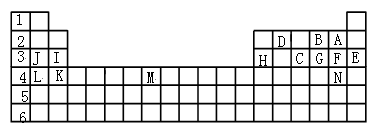
① 表中用字母标出的14种元素中,化学性质最不活泼的是________ ,主族元素中金属性最强的是_______ ,常温下单质为液态的非金属元素是_______ ;属于过渡元素的是_________ 。
②C、G、F气态氢化物的稳定性顺序是______________________ 。
③第三周期中原子半径最小的元素是_______ 。

① 表中用字母标出的14种元素中,化学性质最不活泼的是
②C、G、F气态氢化物的稳定性顺序是
③第三周期中原子半径最小的元素是
您最近一年使用:0次
名校
7 . 某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
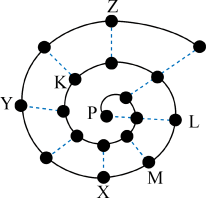
(1)X元素符号为__________________ 。
(2)M与Z两种元素形成的化合物含有的化学键为________________ 。
(3)下列说法正确的是__________________ 。
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键

(1)X元素符号为
(2)M与Z两种元素形成的化合物含有的化学键为
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键
您最近一年使用:0次
2017-03-27更新
|
223次组卷
|
2卷引用:河南省洛阳市第一高级中学2022-2023学年高一下学期3月月考化学试题
11-12高一下·河北邢台·阶段练习
名校
8 . 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
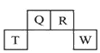
(1)T的原子结构示意图为______________________ 。
(2)元素的非金属性(原子的得电子能力):Q_______________ W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为__________________________________ 。
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________________________________________________ 。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是______________ 。

(1)T的原子结构示意图为
(2)元素的非金属性(原子的得电子能力):Q
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是
您最近一年使用:0次
2016-12-09更新
|
241次组卷
|
10卷引用:2016-2017学年河南省林州市第一中学高一3月调研考试化学试卷
2016-2017学年河南省林州市第一中学高一3月调研考试化学试卷(已下线)2011-2012学年河北省邢台一中高一下学期第二次月考化学试卷2014-2015福建省福州市第八中学高一下学期期中化学试卷2015-2016学年海南琼海市嘉积中学高一下期中理科化学卷2016-2017学年河北省邯郸市大名县第一中学高一3月月考化学试卷江西省南昌市八一中学、洪都中学、麻丘中学、十七中、桑海中学2016-2017学年高一下学期期中考试化学试题江苏省泰州中学2016-2017学年高一5月月度检测化学试题山东省潍坊市临朐县实验中学2022届高三9月摸底考试化学试题四川省南充市白塔中学2021-2022学年高一下学期期中考试化学试题安徽省砀山县第四中学2021-2022学年高一下学期第一阶段教学质量检测 化学试题
9-10高二下·河南郑州·期末
9 . 右表是元素周期表的一部分。
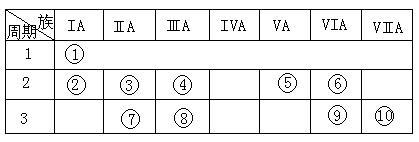
(1)表中元素⑩的氢化物的化学式为__________ ,此氢化物的还原性比元素⑨的氢化物的还原性_____________ (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,其单质的电子式为________________ 。
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式____________________ ;又如表中与元素⑦的性质相似的不同族元素是___________ (填元素符号)

(1)表中元素⑩的氢化物的化学式为
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
您最近一年使用:0次
9-10高一下·河南·期中
10 . 已知aAn+、bB(n+1)+、cCn-、dD(n+1)─具有相同的核外电子排布,则a、b、c、d由大到小的顺序是_______ ,这四种离子的半径由大到小的顺序是_______ 。
您最近一年使用:0次



