名校
1 . 已知:A~H均为短周期元素,它们的最高(或最低)化化合价与原子序数的关系如图。
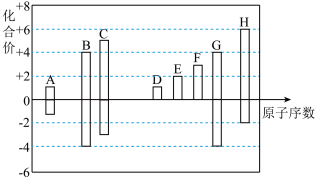
(1)G在周期表中的位置:___________ ,元素C、D、H的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(2)C元素的简单气态氢化物与其最高价氧化物对应的水化物反应生成的化合物与D的最高价氧化物对应的水化物反应的离子方程式:___________ 。G的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式:___________ 。
(3)请写出F的最高价氧化物溶于D的最高价氧化物对应水化物的溶液的离子方程式:___________ 。
(4)上述元素中的三种元素的最高价氧化物的水化物之间两两皆能反应,且三种元素原子的最外层共有9个电子,请写出其中的非金属元素的名称:___________ 。
(5)元素C与元素G相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
a.常温下C的单质和G的单质状态不同
b.C的最高价氧化物对应水化物滴入G的最高价氧化物对应水化物的钠盐溶液中有白色沉淀生成
c.G原子的电子层数比C原子的电子层数多

(1)G在周期表中的位置:
(2)C元素的简单气态氢化物与其最高价氧化物对应的水化物反应生成的化合物与D的最高价氧化物对应的水化物反应的离子方程式:
(3)请写出F的最高价氧化物溶于D的最高价氧化物对应水化物的溶液的离子方程式:
(4)上述元素中的三种元素的最高价氧化物的水化物之间两两皆能反应,且三种元素原子的最外层共有9个电子,请写出其中的非金属元素的名称:
(5)元素C与元素G相比,非金属性较强的是
a.常温下C的单质和G的单质状态不同
b.C的最高价氧化物对应水化物滴入G的最高价氧化物对应水化物的钠盐溶液中有白色沉淀生成
c.G原子的电子层数比C原子的电子层数多
您最近半年使用:0次
名校
2 . A,B,C,D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A,B,C形成电子总数相等的分子X、Y、Z。下列叙述正确的是
| A.X、Y、Z的稳定性逐渐减弱 |
| B.自然界中存在多种由A、B、C、D四种元素组成的化合物 |
| C.Y、X、Z三种化合物的熔、沸点逐渐升高 |
| D.A,B,C,D只能形成5种单质 |
您最近半年使用:0次
解题方法
3 . 化合物 可作阻燃剂,其中W、X、Y、Z均为短周期主族元素,Y在地壳中含量最多,X的基态原子价层p轨道半充满,Y只与Z同周期,Y与W的价电子数之和等于Z的价电子数,W为金属元素。下列说法正确的是
可作阻燃剂,其中W、X、Y、Z均为短周期主族元素,Y在地壳中含量最多,X的基态原子价层p轨道半充满,Y只与Z同周期,Y与W的价电子数之和等于Z的价电子数,W为金属元素。下列说法正确的是
 可作阻燃剂,其中W、X、Y、Z均为短周期主族元素,Y在地壳中含量最多,X的基态原子价层p轨道半充满,Y只与Z同周期,Y与W的价电子数之和等于Z的价电子数,W为金属元素。下列说法正确的是
可作阻燃剂,其中W、X、Y、Z均为短周期主族元素,Y在地壳中含量最多,X的基态原子价层p轨道半充满,Y只与Z同周期,Y与W的价电子数之和等于Z的价电子数,W为金属元素。下列说法正确的是A.第一电离能: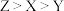 | B.简单氢化物沸点: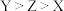 |
C.简单离子半径: | D.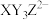 中心原子的价层电子对数为5 中心原子的价层电子对数为5 |
您最近半年使用:0次
名校
4 . 短周期主族元素X、Y、Z、W、M的原子半径依次增大,与元素有关的信息如表所示:
回答下列问题:
(1) 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为___________ ,写出其简单氢化物的一种用途:___________ 。
(2)由 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为___________ 。
(3)上述元素对应的简单离子中半径最大的为___________ (填离子符号)。
(4) 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为___________ 。
(5) 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程___________ 。
(6) 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为___________ 。
(7)下列关于 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。
| 元素 | 相关信息 |
 | 简单氢化物的水溶液可以刻蚀玻璃 |
 | 最外层电子数比次外层多3 |
 | 最高正价和最低负价的代数和为4 |
 | 地壳中含量最高的金属元素 |
 | 最高价氧化物对应水化物属于强碱 |
(1)
 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为(2)由
 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为(3)上述元素对应的简单离子中半径最大的为
(4)
 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为(5)
 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程(6)
 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为(7)下列关于
 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。A.将 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 |
| B.随着原子序数递增,该主族元素对应单质的沸点逐渐升高 |
C.该主族元素中最高价氧化物对应水化物酸性最强的元素为 |
D. 的简单氢化物可与强碱溶液反应 的简单氢化物可与强碱溶液反应 |
您最近半年使用:0次
5 . 甲、乙、丙为原子序数依次增大的不同短周期的主族元素。甲、丙形成的单核离子所带电荷数相同;乙和丙的原子最外层电子数之和为10。下列说法错误的是
| A.丙位于第三周期第ⅦA族 |
| B.甲、丙形成的化合物熔融态不导电 |
| C.最高价含氧酸酸性:乙<丙 |
| D.乙、丙形成的单中心分子中各原子满足8电子结构 |
您最近半年使用:0次
6 . 已知W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y、Z分别处于不同周期,W、X、Y、Z形成的化合物 是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
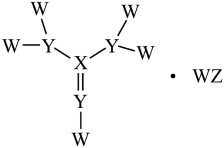
 是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
| A.W、X、Y、Z的单质在常温下均为气体 |
| B.W分别与X、Y、Z结合均可以形成含有相同电子数的分子 |
| C.Y的氧化物对应的水化物为强酸 |
| D.元素的第一电离能:X>Y>W |
您最近半年使用:0次
名校
7 . 已知 为短周期主族元素,
为短周期主族元素, 、
、 为第四周期元素,它们的原子序数依次增大。
为第四周期元素,它们的原子序数依次增大。
(1)已知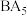 为离子化合物,写出其电子式
为离子化合物,写出其电子式___________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(3)实验室制备 的单质的离子反应方程式为
的单质的离子反应方程式为___________ 。
(4)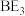 在常温下是一种淡黄色的液体,其遇水即发生反应可生成一种具有漂白性的物质,写出反应的化学方程式
在常温下是一种淡黄色的液体,其遇水即发生反应可生成一种具有漂白性的物质,写出反应的化学方程式___________ ;该反应说明其中B和 中非金属性较强的是
中非金属性较强的是___________ (填元素的符号)。
(5)C与D的第一电离能大小为___________ 。D与 的最高价氧化物对应水化物相互反应的离子方程式为
的最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(6) 价电子排布图为
价电子排布图为___________ ,位于___________ 区。 元素的原子结构示意图为
元素的原子结构示意图为___________ ,前四周期中未成对电子数最多的元素在周期表中位置为___________ 。
 为短周期主族元素,
为短周期主族元素, 、
、 为第四周期元素,它们的原子序数依次增大。
为第四周期元素,它们的原子序数依次增大。| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B元素原子的核外 电子数比 电子数比 电子数少1 电子数少1 |
C原子的第一至第四电离能分别是: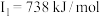 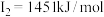 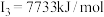 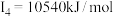 |
| D元素简单离子半径是该周期中最小的 |
| E元素是该周期电负性最大的元素 |
| F所在族的元素种类是周期表中最多的 |
| G在周期表的第十一列 |
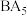 为离子化合物,写出其电子式
为离子化合物,写出其电子式(2)B基态原子中能量最高的电子,其电子云在空间有
(3)实验室制备
 的单质的离子反应方程式为
的单质的离子反应方程式为(4)
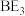 在常温下是一种淡黄色的液体,其遇水即发生反应可生成一种具有漂白性的物质,写出反应的化学方程式
在常温下是一种淡黄色的液体,其遇水即发生反应可生成一种具有漂白性的物质,写出反应的化学方程式 中非金属性较强的是
中非金属性较强的是(5)C与D的第一电离能大小为
 的最高价氧化物对应水化物相互反应的离子方程式为
的最高价氧化物对应水化物相互反应的离子方程式为(6)
 价电子排布图为
价电子排布图为 元素的原子结构示意图为
元素的原子结构示意图为
您最近半年使用:0次
解题方法
8 . 已知A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。
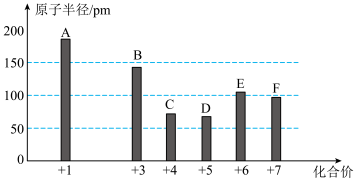
请回答下列问题:
(1)B元素在周期表中的位置为__________ ;D元素能与氢元素组成18电子分子,该分子含有的共价键类型为__________ (填“极性键”或“非极性键”)。
(2)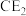 属于严禁携带的易燃易爆液体,其电子式为
属于严禁携带的易燃易爆液体,其电子式为__________ ;A、E、F三种元素形成的简单离子,半径由大到小的顺序是__________ (用离子符号表示)。
(3)写出元素A、B的最高价氧化物的水化物相互反应的离子方程式__________ 。
(4)用C元素的最简单氢化物和 在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的
在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的__________ 极,若线路中转移2mol电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为__________ 。
(5)化合物 在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向
在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向 溶液中滴加酸性
溶液中滴加酸性 溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式__________ 。

请回答下列问题:
(1)B元素在周期表中的位置为
(2)
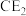 属于严禁携带的易燃易爆液体,其电子式为
属于严禁携带的易燃易爆液体,其电子式为(3)写出元素A、B的最高价氧化物的水化物相互反应的离子方程式
(4)用C元素的最简单氢化物和
 在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的
在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的 在标准状况下的体积为
在标准状况下的体积为(5)化合物
 在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向
在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向 溶液中滴加酸性
溶液中滴加酸性 溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
您最近半年使用:0次
9 . 回答下列问题
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是_______ (填元素符号,下同);
②B、C、D、E的第一电离能由小到大的顺序是_______ ;
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是_______ 。
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
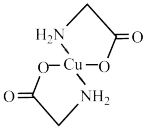
①硅原子电子占据的最高能级电子云形状为_______ ;
②Fe3+的价电子排布图为_______ ;
③铜位于周期表中_______ 区,铜原子的电子排布式为_______ 。试从核外电子排布角度比较,高温下Cu2O和CuO的稳定性更高的原因是_______ 。
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是
②B、C、D、E的第一电离能由小到大的顺序是
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:

①硅原子电子占据的最高能级电子云形状为
②Fe3+的价电子排布图为
③铜位于周期表中
您最近半年使用:0次
解题方法
10 . 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种新型超分子,其分子结构如下图所示(Y和Y之间重复单元的W、X未全部标出),W、X、Z分别位于不同周期,Z是同周期中金属性最强的元素,下列说法正确的是


A.简单气态氢化物的沸点: |
B.第一电离能: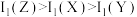 |
C. 只含有离子键 只含有离子键 |
D.原子半径: |
您最近半年使用:0次



