名校
1 . 离子液体在电化学研究中应用广泛,某离子液体M由W、X、Y、Z四种原子半径依次增大的短周期元素组成,其结构如图所示。下列说法正确的是
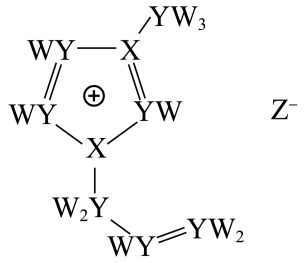

| A.X和Y均能与W形成18电子分子,且前者的沸点相对较高 |
| B.元素Z位于第2周期ⅦA族,属于p区元素 |
| C.物质M的晶体中含有离子键、σ键、π键和氢键 |
| D.若用石墨电极电解M,阴极产生黄绿色气体 |
您最近半年使用:0次
2024-04-09更新
|
129次组卷
|
3卷引用:河北省沧州市泊头市八县联考2023-2024学年高三下学期3月月考化学试题
2 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A形成的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。回答下列问题:
(1)E元素在周期表中的位置为_______ 。
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:_______ 。
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:_______ 。
(4)若要比较D和E的失电子能力强弱,下列实验方法可行的是_______ (填字母)。
a.将D形成的单质置于E的盐溶液中,若D形成的单质不能置换出E形成的单质,说明D的失电子能力比E的弱
b.在常温下,将少量D、E形成的单质分别投入到水中,若D形成的单质和水反应而E形成的单质不和水反应,说明D的失电子能力比E的强
c.比较相同条件下D和E的最高价氧化物对应的水化物的溶解性,若前者比后者的溶解度大,说明D的失电子能力比E的强
(1)E元素在周期表中的位置为
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:
(4)若要比较D和E的失电子能力强弱,下列实验方法可行的是
a.将D形成的单质置于E的盐溶液中,若D形成的单质不能置换出E形成的单质,说明D的失电子能力比E的弱
b.在常温下,将少量D、E形成的单质分别投入到水中,若D形成的单质和水反应而E形成的单质不和水反应,说明D的失电子能力比E的强
c.比较相同条件下D和E的最高价氧化物对应的水化物的溶解性,若前者比后者的溶解度大,说明D的失电子能力比E的强
您最近半年使用:0次
名校
解题方法
3 . 化合物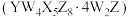 可用于电讯器材、高级玻璃的制造。
可用于电讯器材、高级玻璃的制造。 为短周期元素,原子序数依次增加,且加和为21。
为短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在
分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
以下热分解时无刺激性气体逸出。下列叙述正确的是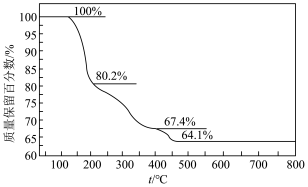
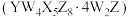 可用于电讯器材、高级玻璃的制造。
可用于电讯器材、高级玻璃的制造。 为短周期元素,原子序数依次增加,且加和为21。
为短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在
分子的总电子数为奇数,常温下为气体。该化合物的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
以下热分解时无刺激性气体逸出。下列叙述正确的是
A. 的氢化物稳定性一定强于 的氢化物稳定性一定强于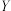 的氢化物 的氢化物 | B.简单气态氢化物的沸点: |
C.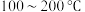 阶段热分解失去4个 阶段热分解失去4个 | D. 热分解后生成固体化合物 热分解后生成固体化合物 |
您最近半年使用:0次
2024-04-08更新
|
71次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
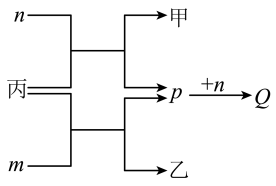
4 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W与X的原子序数之和是Y的一半,m、n、p均是这些元素组成的常见二元气态化合物,常温下0.01 mol·L-1 p溶液中氢离子浓度为0.01 mol·L-1;X、Y、Z的单质分别为甲、乙、丙,其中乙能存在于火山喷口附近,它们之间的转化关系如图所示。下列说法正确的是

| A.元素X、Y的氧化物对应水化物的浓溶液常温下都能使铁、铝钝化 |
| B.Y元素的氢化物能与其某种氧化物反应生成Y的单质 |
| C.实验室中可利用Q受热分解来制备n |
| D.工业上用甲作原料来制备元素X的最高价含氧酸 |
您最近半年使用:0次
2024-04-08更新
|
90次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
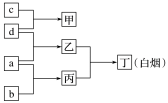
5 . R、X、Y、Z是原子序数依次增大的短周期元素,a、b、c、d分别是这4种元素的单质。已知:Y是地壳中含量最高的金属元素。向甲的溶液中通入丙气体,产生白色沉淀,它们之间的转化关系如图所示。下列说法正确的是

| A.元素对应的简单离子的半径:Y>Z>X |
| B.元素非金属性:Z>R>X |
| C.Y的最高价氧化物对应的水化物是强碱 |
| D.元素最高化合价:Z>X>Y>R |
您最近半年使用:0次
2024-04-08更新
|
70次组卷
|
2卷引用:河南省实验中学2023-2024学年高一下学期月考化学试卷
名校
解题方法
6 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如下:X最外层电子数是内层电子数的2倍,Y其单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强
(1)元素Y在元素周期表中的位置是_______ 。
(2)Z在氧气中完全燃烧所得产物的电子式为_______ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
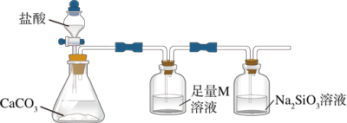
①盛放盐酸的仪器名称是:_______ ;试剂M名称为_______ ,其作用是_______ 。
②能说明X元素的非金属性比硅元素强的实验现象是_______ 。
(5)元素Z与W相比,金属性较弱的是_______ (填元素名称),请写出能证明这一结论的实验事实_______ (列举一条)。
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧所得产物的电子式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

①盛放盐酸的仪器名称是:
②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近半年使用:0次
名校
解题方法
7 . 有机金属氯化物由原子序数依次增大的短周期主族元素X、Y、Z、M、N组成,部分结构如图所示,基态原子M核外电子所占据原子轨道全充满,N元素的价层电子排布式为 ,下列说法
,下列说法不正确 的是
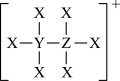
 ,下列说法
,下列说法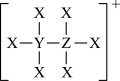
A.Z与N可形成化合物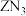 、 、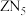 |
B.最简单氢化物的沸点: |
| C.M元素的第一电离能比同周期相邻元素的大 |
D. 离子中Y发生 离子中Y发生 杂化 杂化 |
您最近半年使用:0次
解题方法
8 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同主族,Y原子的最外层电子数等于X原子的电子总数,Z原子的电子总数等于W、X、Y三种原子的电子数之和,Z的最高价氧化物对应水化物的化学式为HnZO2n+2。W、X、Y三种元素形成的一种化合物的结构如图所示。下列说法正确的是


| A.X常用来制造电池 |
| B.Y、Z形成的化合物常用于制取单质Y |
| C.W的简单离子半径一定大于X的简单离子半径 |
| D.Z的单质需保存在棕色试剂瓶中 |
您最近半年使用:0次
名校
解题方法
9 . X、Y、Z、W为原子序数依次增大的短周期主族元素,由这四种元素形成的某化合物的结构如图所示,该化合物中元素W的化合价为其最高化合价,下列说法正确的是


| A.X、Y、Z、W中Z的第一电离能最大 | B.由这四种元素不能形成离子化合物 |
| C.X与Y、Z、W均能形成18电子分子 | D.四种元素形成的四种单质中,两两间均能化合 |
您最近半年使用:0次
名校
解题方法
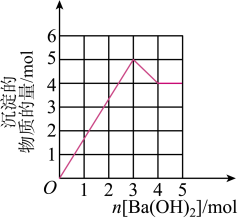
10 . 元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R和Y位于同主族,X的简单离子半径在同周期元素中最小。由这四种元素组成一种化合物Q,在Q的溶液中滴加 溶液。产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是
溶液。产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是
 溶液。产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是
溶液。产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是
| A.R的最高价氧化物水化物酸性大于Y的最高价氧化物水化物 |
| B.Z的离子半径是同周期离子半径最小的 |
| C.Q的水溶液显酸性,可作为净水剂 |
D.当加入3mol 时,沉淀物有2种,且物质的量之比为4:1或1:4 时,沉淀物有2种,且物质的量之比为4:1或1:4 |
您最近半年使用:0次



