名校
解题方法
1 . 4种短周期主族元素X、Y、Z和Q的原子序数依次增大,相关信息如下表:
下列说法正确的是
| 元素 | 相关信息 |
| X | 最外层电子数等于次外层电子数 |
| Y | 与X在同一主族 |
| Z | 单质为淡黄色固体,难溶于水,微溶于酒精,易溶于二硫化碳 |
| Q | 同周期主族元素中原子半径最小 |
| A.X的金属性比Y强 |
| B.Y的原子半径是同周期中最大的 |
| C.Z的单质在空气燃烧和在充满氧气的集气瓶中燃烧产物相同 |
| D.Q的含氧酸与Z的含氧酸都可以混合,不发生反应 |
您最近半年使用:0次
名校
2 . 根据以下短周期元素的性质或原子结构特点推测元素并回答问题:
(1)元素乙的一种核素可用于测定文物年代,这种核素的符号是____________________ 。
(2)元素丁形成的负一价阴离子的离子符号是__________ ,写出某溶液中含该微粒的检验方法:取该溶液少许于试管中,______________________________ 。
(3)元素丁与元素甲相比,原子得电子能力较强的是__________ (填元素名称),下列表述中能证明这一事实的是__________ (填序号)。
①常温下丁的单质和甲的单质状态不同;
②丁的氢化物比甲的氢化物稳定;
③一定条件下丁和甲的单质都能与氢氧化钠溶液反应;
(4)探寻物质的性质差异性是学习的重要方法之一。甲、乙、丙、丁四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是__________ (填化学式),理由是______________________________ 。
元素 | 元素的性质或原子结构 |
甲 | M层上有6个电子 |
乙 | 最外层电子数是次外层电子数的2倍 |
丙 | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
丁 | 元素的最高正化合价是+7价 |
(2)元素丁形成的负一价阴离子的离子符号是
(3)元素丁与元素甲相比,原子得电子能力较强的是
①常温下丁的单质和甲的单质状态不同;
②丁的氢化物比甲的氢化物稳定;
③一定条件下丁和甲的单质都能与氢氧化钠溶液反应;
(4)探寻物质的性质差异性是学习的重要方法之一。甲、乙、丙、丁四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是
您最近半年使用:0次
名校
解题方法
3 . X、Y、Z、M是原子序数依次递增的短周期主族元素。其中X、M同主族;X、Y、Z均为非金属元素,且X与Y的质子数之和比Z的质子数小1,Y与Z的质子数之和比M的质子数大3.下列说法错误的是
| A.电负性:Z>Y>X |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.X、Y形成的化合物中一定既含极性键又含非极性键 |
| D.M单质在Z2中燃烧生成淡黄色固体 |
您最近半年使用:0次
名校
解题方法
4 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如表。
(1)元素Y在元素周期表中的位置是_____ 。
(2)Z在氧气中完全燃烧所得产物的电子式为_____ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是_____ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
①M为_____ (填化学式),其作用是_____ 。
②能说明X元素的非金属性比硅元素强的实验现象是_____ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是内层电子数的2倍 |
| Y | 其单质与氢气在暗处能剧烈化合并发生爆炸 |
| Z | 短周期元素中原子半径最大 |
| W | 其氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(2)Z在氧气中完全燃烧所得产物的电子式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
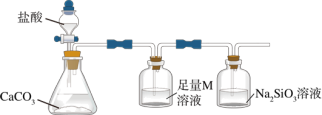
①M为
②能说明X元素的非金属性比硅元素强的实验现象是
您最近半年使用:0次
名校
解题方法
5 . 现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别对应X、Y、Z元素组成的单质)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种高能燃料,分子中含有18个电子,其组成元素与丙相同。________ ,元素X的最高价氧化物的水化物和NaOH溶液反应的离子方程式为________ 。
(2)丙的结构式为________ ,丙的水溶液中浓度最高的阳离子的电子式为________ 。
(3)乙中所含的化学键类型有________ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)丁的结构式为________ 。
(5)反应②中,74.5gNaClO参加反应时转移2mol电子,该反应的化学方程式为________ 。
(6)A与 、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为________ 。
元素编号 | 元素性质或原子结构信息 |
X | 第三周期元素中简单离子半径最小的元素 |
Y | 其最简单氢化物的水溶液呈碱性 |
Z | 原子核外电子数和所在周期数相等 |
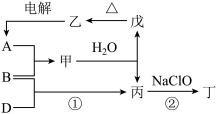
(2)丙的结构式为
(3)乙中所含的化学键类型有
a.离子键 b.极性共价键 c.非极性共价键
(4)丁的结构式为
(5)反应②中,74.5gNaClO参加反应时转移2mol电子,该反应的化学方程式为
(6)A与
 、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
、C(石墨)在高温下反应只生成乙和碳化钛(TiC),该反应的化学方程式为
您最近半年使用:0次
名校
6 . 根据表中八种短周期元素的有关信息判断,下列说法错误的是
元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A.元素②⑥形成的化合物具有两性 |
| B.元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 |
| C.⑧最高价氧化物对应的水化物的碱性为同周期中最强 |
| D.元素④位于周期表中的P区 |
您最近半年使用:0次
名校
解题方法
7 . 现有A、B、C、D、E五种元素,它们的核电荷数依次增多。
①A的核电荷数大于2,可形成氢化物 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;
②A和B两元素可形成化合物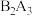 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
③ 比
比 多8个电子;
多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为 。
。
试回答下列问题:
(1)A是_____ (写元素符号,下同), 分子的空间结构为
分子的空间结构为_____________ 。
(2)B的离子结构示意图为_______ ,C元素最高价氧化物对应的水化物的电子式为_________ ,D的原子的电子排布式为___________ 。
(3)用电子式表示 的形成过程:
的形成过程:______________ 。
(4)写出CD的溶液中通入氯气的离子方程式:_____________ 。
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):_____________ 。
①A的核电荷数大于2,可形成氢化物
 ,该氢化物在常温下是液体;
,该氢化物在常温下是液体;②A和B两元素可形成化合物
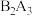 ,该化合物既能溶于强酸溶液,又能溶于强碱溶液;
,该化合物既能溶于强酸溶液,又能溶于强碱溶液;③
 比
比 多8个电子;
多8个电子;④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为
 。
。试回答下列问题:
(1)A是
 分子的空间结构为
分子的空间结构为(2)B的离子结构示意图为
(3)用电子式表示
 的形成过程:
的形成过程:(4)写出CD的溶液中通入氯气的离子方程式:
(5)比较B、C、E三种元素形成的简单离子半径由小到大的顺序(B、C、E离子用实际离子符号表示):
您最近半年使用:0次
名校
解题方法
8 . 短周期主族元素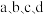 的原子序数依次增大。四种元素形成的单质依次为
的原子序数依次增大。四种元素形成的单质依次为 。而
。而 是这些元素组成的二元化合物,其中
是这些元素组成的二元化合物,其中 为形成酸雨的主要物质之一,
为形成酸雨的主要物质之一,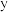 为淡黄色固体,
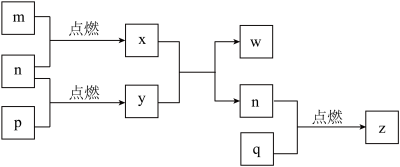
为淡黄色固体,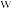 水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
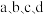 的原子序数依次增大。四种元素形成的单质依次为
的原子序数依次增大。四种元素形成的单质依次为 。而
。而 是这些元素组成的二元化合物,其中
是这些元素组成的二元化合物,其中 为形成酸雨的主要物质之一,
为形成酸雨的主要物质之一,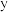 为淡黄色固体,
为淡黄色固体,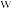 水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
水溶液可使酚酞溶液变红。上述物质转化关系如图所示。下列说法正确的是
A.原子半径的大小: |
B. 的电子式一定是: 的电子式一定是: 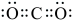 |
C.简单氢化物的沸点: |
D.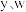 溶于水,破坏的化学键类型完全相同 溶于水,破坏的化学键类型完全相同 |
您最近半年使用:0次
名校
解题方法
9 . 五种短周期元素 的原子序数依次增大,A和C同族,
的原子序数依次增大,A和C同族, 和D同族,C离子和B离子有相同的电子层结构。
和D同族,C离子和B离子有相同的电子层结构。 和
和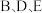 分别形成共价型化合物
分别形成共价型化合物 。
。 和
和 形成的气态化合物
形成的气态化合物 在水中呈碱性,
在水中呈碱性, 和
和 形成化合物
形成化合物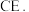 下列说法正确的是
下列说法正确的是
 的原子序数依次增大,A和C同族,
的原子序数依次增大,A和C同族, 和D同族,C离子和B离子有相同的电子层结构。
和D同族,C离子和B离子有相同的电子层结构。 和
和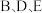 分别形成共价型化合物
分别形成共价型化合物 。
。 和
和 形成的气态化合物
形成的气态化合物 在水中呈碱性,
在水中呈碱性, 和
和 形成化合物
形成化合物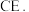 下列说法正确的是
下列说法正确的是A.气态氢化物 中热稳定性最弱的是 中热稳定性最弱的是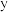 |
B.五种元素中原子半径最大的是 |
C. 最高价氧化物对应水化物的化学式为 最高价氧化物对应水化物的化学式为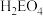 |
D.C的单质在空气中燃烧产物的化学式为 |
您最近半年使用:0次
解题方法
10 . 已知A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和F分别为同一主族元素,B原子的最外层电子数比次外层多3,E的最高价氧化物的水化物既可以和强酸反应也可以和强碱溶液反应,F的单质常出现在火山口。
(1)C在元素周期表中的位置是______ 。
(2)C、D分别形成的简单离子中,半径较大的是______ (填离子符号)。
(3)F和G的最高价氧化物的水化物酸性较强的是______ (填化学式)。
(4)由A、C、D形成的化合物中化学键的类型为______ 。
(5)由C、D形成摩尔质量为78g/mol化合物的电子式为:______ 。
(6)D、E的最高价氧化物的水化物相互反应的化学方程式为:______ 。
(1)C在元素周期表中的位置是
(2)C、D分别形成的简单离子中,半径较大的是
(3)F和G的最高价氧化物的水化物酸性较强的是
(4)由A、C、D形成的化合物中化学键的类型为
(5)由C、D形成摩尔质量为78g/mol化合物的电子式为:
(6)D、E的最高价氧化物的水化物相互反应的化学方程式为:
您最近半年使用:0次



