1 . 原子序数依次增大的三种前四周期元素X、Y、Z组成的某天然矿石的晶体结构如图所示。其中Y元素的一种氧化物具有磁性,Z元素的价电子数为11,下列说法正确的是
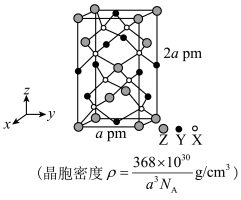

| A.Y、Z均位于元素周期表的d区 | B.第三电离能 |
C.电负性: | D.键角: |
您最近一年使用:0次
名校
2 . 中山大学化学学院廖培钦教授利用HAB合成了有机金属框架(Cu-HAB),为开发催化 制乙醇的催化剂取得突破,合成过程如图所示。
制乙醇的催化剂取得突破,合成过程如图所示。

下列叙述错误的是
 制乙醇的催化剂取得突破,合成过程如图所示。
制乙醇的催化剂取得突破,合成过程如图所示。
下列叙述错误的是
| A.1molHAB最多能消耗6molHCl |
B.上述变化中N原子由 杂化变为 杂化变为 杂化 杂化 |
C.Cu-HAB中N原子提供孤电子对与 形成配位键 形成配位键 |
| D.在Cu-HAB中氮元素电负性最大 |
您最近一年使用:0次
解题方法
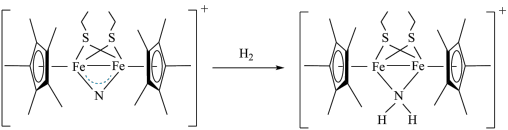
3 . 科学家近期合成了一种配合物,该物质可以在温和条件下活化 ,将
,将 转化为
转化为 ,反应过程如图所示。下列说法错误的是
,反应过程如图所示。下列说法错误的是
 ,将
,将 转化为
转化为 ,反应过程如图所示。下列说法错误的是
,反应过程如图所示。下列说法错误的是
| A.如图,反应过程中N元素的价态发生了变化 |
B. 的VSEPR模型为V形 的VSEPR模型为V形 |
C.电负性大小: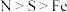 |
D.键角: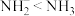 |
您最近一年使用:0次
4 . 化合物 可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为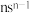 ,Z在地壳中含量最多。下列说法不正确的是
,Z在地壳中含量最多。下列说法不正确的是
 可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为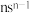 ,Z在地壳中含量最多。下列说法不正确的是
,Z在地壳中含量最多。下列说法不正确的是| A.元素电负性:Z>Y>X | B.最简单氢化物沸点:Z>Y>N |
| C.第一电离能:Y>Z>M | D. 和 和 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
2024-02-14更新
|
670次组卷
|
3卷引用:2024届江西省上饶市高三下学期第二次高考模拟考试化学试卷
2024届江西省上饶市高三下学期第二次高考模拟考试化学试卷2024届湖南省岳阳市高三教学质量监测考试一模化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
5 . 叠氮化钠( )可用于汽车安全气囊的制造,
)可用于汽车安全气囊的制造, 与
与 发生反应可以生成
发生反应可以生成 ,反应方程式为
,反应方程式为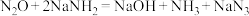 。下列有关说法错误的是
。下列有关说法错误的是
 )可用于汽车安全气囊的制造,
)可用于汽车安全气囊的制造, 与
与 发生反应可以生成
发生反应可以生成 ,反应方程式为
,反应方程式为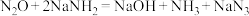 。下列有关说法错误的是
。下列有关说法错误的是A.键角: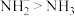 | B.电负性: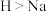 |
C. 溶液显碱性 溶液显碱性 | D.1 mol  中含2 mol σ键 中含2 mol σ键 |
您最近一年使用:0次
2024-02-01更新
|
446次组卷
|
3卷引用:江西省宜春市第一中学2023-2024学年高三上学期1月质量检测化学试题
23-24高二上·四川遂宁·阶段练习
名校
解题方法
6 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为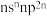 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
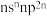 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:B>C>A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
| C.B、C、E形成的简单离子半径大小顺序:E离子>C离子>B离子 |
D.F离子的核外电子排布式为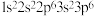 |
您最近一年使用:0次
名校
解题方法
7 . 含有多个配位原子的配体与同一中心离子(或原子)通过整合配位成环而形成的配合物为整合物。一种Cd2+配合物的结构如图所示,下列说法不正确的是
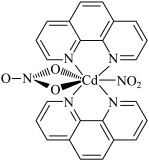
A.结构图右边 与O3互为等电子体 与O3互为等电子体 |
| B.N所形成的六元环中N的杂化方式为sp2 |
| C.该配合物分子中Cd2+的配位数为7 |
| D.图中所涉及元素的电负性由大到小顺序为:O>N>C>H>Cd |
您最近一年使用:0次
名校
解题方法
8 . 前四周期元素X、Y、Z、M原子序数依次增大,由这四种元素形成的一种常见的血红色配离子的结构如图所示,该离子中X、Y、Z都满足8电子结构。下列说法错误的是


| A.电负性:Y>Z>X>M | B.该配离子中M的配位数为6 |
C.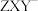 离子中X为sp杂化 离子中X为sp杂化 | D.该配离子中所有键角都为180° |
您最近一年使用:0次
名校
9 . 三氯甲硅烷((SiHCl₃)是制取高纯硅的重要原料,常温下为无色液体,沸点为31.8℃,熔点为-126.5℃,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:

(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为______ ;判断制备反应结束的实验现象是______ 。图示装置存在的两处缺陷,请提出相应改进建议______ 。
(2)已知电负性Cl>H>Si, 在浓NaOH溶液中发生反应的化学方程式为
在浓NaOH溶液中发生反应的化学方程式为______ 。
(3)采用如下方法测定溶有少量HCl的 纯度。
纯度。
 g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①______ ,②______ (填操作名称),③称量等操作,测得所得固体氧化物质量为 g,从下列仪器中选出①、②中需使用的仪器,依次为
g,从下列仪器中选出①、②中需使用的仪器,依次为______ (填标号)。测得样品纯度为______ (用含 、
、 的代数式表示)。
的代数式表示)。

 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为(2)已知电负性Cl>H>Si,
 在浓NaOH溶液中发生反应的化学方程式为
在浓NaOH溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量HCl的
 纯度。
纯度。 g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① g,从下列仪器中选出①、②中需使用的仪器,依次为
g,从下列仪器中选出①、②中需使用的仪器,依次为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
10 . 铜及其化合物具有广泛的应用。请回答:
(1)Cu元素位于周期表___________ 区。
(2)下列说法不正确 的是___________。
(3)高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是___________ 。(已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)
(4) 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、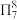 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是___________ (填标号);1mol配合物中含配位键个数为___________ 。___________ 个。
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为___________  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
(1)Cu元素位于周期表
(2)下列说法
| A.基态铜原子的核外电子有29种不同的空间运动状态 |
B.铜催化烯烃硝化反应时会产生 , , 的键角比 的键角比 大 大 |
C. 中非金属元素电负性: 中非金属元素电负性: |
D.配位键的强度: 大于 大于 |
(3)高温下固体中
 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)(4)
 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、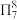 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是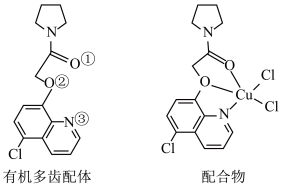
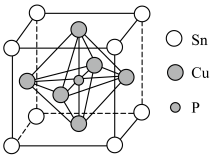
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为
 (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
您最近一年使用:0次
2023-11-26更新
|
320次组卷
|
3卷引用:江西省上饶市婺源县天佑中学2023-2024学年高三上学期期中考试化学试卷
江西省上饶市婺源县天佑中学2023-2024学年高三上学期期中考试化学试卷浙江省9+1高中联盟2023-2024学年高三上学期期中考试化学试题 (已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)



