1 . 钨(W)广泛用于国防军事、航空航天、信息制造等领域。实验室以硬质合金废料(含WC、Fe和少量C、Co)为原料制备炼钨中间体 ,并提取有价金属的一种工艺流程如图所示:
,并提取有价金属的一种工艺流程如图所示:
回答下列问题:
(1)“酸浸”的目的为___________ ;“沉铁”时调节pH的范围为___________ ;“还原”反应同时生成一种参与大气循环的气体,该离子方程式为___________ 。
(2)其他条件相同时,“焙烧”过程中 流速与钨氧化率的关系如图所示,其中
流速与钨氧化率的关系如图所示,其中 流速大于0.15 m3/h时钨氧化率降低的原因为
流速大于0.15 m3/h时钨氧化率降低的原因为___________ 。 ,其原因为
,其原因为___________ 。
(4)“酸浸”工序可用电解法代替。则进行电解时,WC进入___________ (填“阳极泥”或“阴极泥”)。
(5)尾气1与尾气3的反应是汽车尾气处理的原理之一,该反应的化学方程式为___________ 。
(6) 、
、 ,
, 、
、 ,NaOH,Co中,熔点主要取决于氢键的是
,NaOH,Co中,熔点主要取决于氢键的是___________ ;H、O、Cl、Co的电负性由大到小的顺序为___________ 。
 ,并提取有价金属的一种工艺流程如图所示:
,并提取有价金属的一种工艺流程如图所示: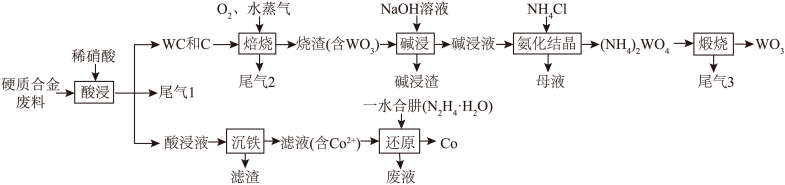
| 金属离子 |  |  |  |  |
| 开始沉定pH | 0.2 | 1.5 | 6.5 | 7.0 |
| 沉淀完全pH | 1.1 | 4.1 | 9.7 | 9.2 |
(1)“酸浸”的目的为
(2)其他条件相同时,“焙烧”过程中
 流速与钨氧化率的关系如图所示,其中
流速与钨氧化率的关系如图所示,其中 流速大于0.15 m3/h时钨氧化率降低的原因为
流速大于0.15 m3/h时钨氧化率降低的原因为
 ,其原因为
,其原因为(4)“酸浸”工序可用电解法代替。则进行电解时,WC进入
(5)尾气1与尾气3的反应是汽车尾气处理的原理之一,该反应的化学方程式为
(6)
 、
、 ,
, 、
、 ,NaOH,Co中,熔点主要取决于氢键的是
,NaOH,Co中,熔点主要取决于氢键的是
您最近一年使用:0次
名校
2 . 三氯甲硅烷((SiHCl₃)是制取高纯硅的重要原料,常温下为无色液体,沸点为31.8℃,熔点为-126.5℃,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:

(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为______ ;判断制备反应结束的实验现象是______ 。图示装置存在的两处缺陷,请提出相应改进建议______ 。
(2)已知电负性Cl>H>Si, 在浓NaOH溶液中发生反应的化学方程式为
在浓NaOH溶液中发生反应的化学方程式为______ 。
(3)采用如下方法测定溶有少量HCl的 纯度。
纯度。
 g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①______ ,②______ (填操作名称),③称量等操作,测得所得固体氧化物质量为 g,从下列仪器中选出①、②中需使用的仪器,依次为
g,从下列仪器中选出①、②中需使用的仪器,依次为______ (填标号)。测得样品纯度为______ (用含 、
、 的代数式表示)。
的代数式表示)。

 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为(2)已知电负性Cl>H>Si,
 在浓NaOH溶液中发生反应的化学方程式为
在浓NaOH溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量HCl的
 纯度。
纯度。 g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① g,从下列仪器中选出①、②中需使用的仪器,依次为
g,从下列仪器中选出①、②中需使用的仪器,依次为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
3 . 铜及其化合物具有广泛的应用。请回答:
(1)Cu元素位于周期表___________ 区。
(2)下列说法不正确 的是___________。
(3)高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是___________ 。(已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)
(4) 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、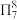 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是___________ (填标号);1mol配合物中含配位键个数为___________ 。___________ 个。
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为___________  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
(1)Cu元素位于周期表
(2)下列说法
| A.基态铜原子的核外电子有29种不同的空间运动状态 |
B.铜催化烯烃硝化反应时会产生 , , 的键角比 的键角比 大 大 |
C. 中非金属元素电负性: 中非金属元素电负性: |
D.配位键的强度: 大于 大于 |
(3)高温下固体中
 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)(4)
 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是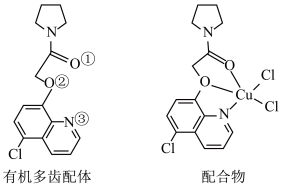
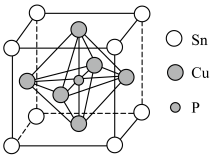
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为
 (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
您最近一年使用:0次
2023-11-26更新
|
320次组卷
|
3卷引用:江西省上饶市婺源县天佑中学2023-2024学年高三上学期期中考试化学试卷
江西省上饶市婺源县天佑中学2023-2024学年高三上学期期中考试化学试卷浙江省9+1高中联盟2023-2024学年高三上学期期中考试化学试题 (已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
4 . 化合物M由两种短周期主族元素组成,在一定条件下可以发生下列转化:
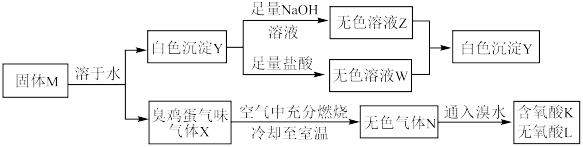
请回答下列问题:
(1)固体M的化学式为___________ 。
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为___________ ,其基态原子中电子的空间运动状态有___________ 种。
(3)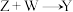 的化学方程式为
的化学方程式为___________ 。
(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为___________ 。
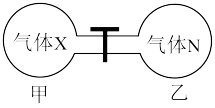
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。
①反应前两容器中的气体密度: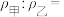
___________ 。
②打开活塞,使气体充分反应,则反应前后的压强: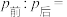
___________ 。
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=___________ 。

请回答下列问题:
(1)固体M的化学式为
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为
(3)
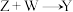 的化学方程式为
的化学方程式为(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。

①反应前两容器中的气体密度:
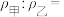
②打开活塞,使气体充分反应,则反应前后的压强:
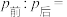
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=
您最近一年使用:0次
2023-11-22更新
|
86次组卷
|
2卷引用:江西省2024届高三上学期11 月一轮总复习调研测试化学试题
名校
5 . 第ⅢA和第ⅤA元素可形成多种化合物。请回答:
(1)基态B原子核外电子占据的最高能级符号是___________ ,基态As原子的价层电子排布式是___________ 。
(2)①固体储氢材料氨硼烷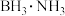 ,其结构和乙烷相似,下列有关说法正确的是
,其结构和乙烷相似,下列有关说法正确的是______ 。
A.氨硼烷中B原子的杂化方式为
B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素 形成的化合物中配位键的强度:
形成的化合物中配位键的强度:
________ 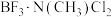 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是________ 。
(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为___________ ,每个N原子周围距离最近的N原子数目为________ 。
(1)基态B原子核外电子占据的最高能级符号是
(2)①固体储氢材料氨硼烷
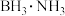 ,其结构和乙烷相似,下列有关说法正确的是
,其结构和乙烷相似,下列有关说法正确的是A.氨硼烷中B原子的杂化方式为

B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素
D. 是硼原子能量最低的激发态
是硼原子能量最低的激发态
 形成的化合物中配位键的强度:
形成的化合物中配位键的强度:
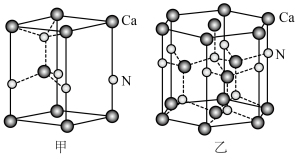
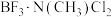 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为
您最近一年使用:0次
2023-11-15更新
|
578次组卷
|
3卷引用:江西省抚州市黎川县第二中学2023-2024学年高三上学期11月期中化学试题
江西省抚州市黎川县第二中学2023-2024学年高三上学期11月期中化学试题浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
6 . CuO、Cu2S等含铜化合物可以催化合成HCOOH.回答下列问题:
(1)基态铜原子的价电子排布式为___________ 。
(2)HCOOH中碳原子的轨道杂化类型为___________ ,元素电负性从大到小的顺序为___________ 。
(3)催化过程中可能产生 ,
, 的空间构型为
的空间构型为___________ ,碳氧键的平均键长 比CH3OH要
比CH3OH要___________ (填“长”或“短”)。
(4)在有机溶剂中,H2SO4的电离平衡常数Ka1(H2SO4)比H2CO3的电离平衡常数Ka1(H2CO3)大,除S的非金属性比C强外,在分子结构上还存在的原因是___________ 。
(5)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。
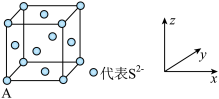
S2-配位数为______________________ ;已知图中A处(S2-)的原子分数坐标为(0,0,0),则晶胞中与A距离最近的为Cu+原子分数坐标为___________ ;若晶胞参数anm,晶体的密度为dg·cm-3),则阿伏加德罗常数的值为___________ (用含a和d的式子表示)。
(1)基态铜原子的价电子排布式为
(2)HCOOH中碳原子的轨道杂化类型为
(3)催化过程中可能产生
 ,
, 的空间构型为
的空间构型为 比CH3OH要
比CH3OH要(4)在有机溶剂中,H2SO4的电离平衡常数Ka1(H2SO4)比H2CO3的电离平衡常数Ka1(H2CO3)大,除S的非金属性比C强外,在分子结构上还存在的原因是
(5)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。

S2-配位数为
您最近一年使用:0次
解题方法
7 . 硫、锌分别是人体必须的常量元素和微量元素,在生产中有着广泛应用。回答下列问题。
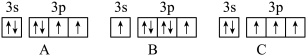
(1)基态硫原子的价电子排布式为___________ ,共有___________ 个未成对电子。下列状态的硫原子中,电离最外层1个电子所需能量最低的是___________ (填标号)。
(2)S与O同族,H2S与H2O空间构型相同,都是2对孤电子对,但H2O分子中的键角比H2S分子中的键角大,请从成键电子对之间相互排斥的角度解释其原因___________ 。
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有___________ ,下表是2种二烃基锌的沸点数据,则烃基R1是___________ ,推断的依据,是___________ 。
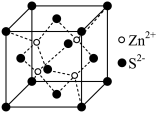
(4)闪锌矿硫化锌的晶胞结构如图所示。硫离子呈立方最密堆积,Zn2+填入S2-组成___________ 空隙中(填“正四面体”或“正八面体”);NA为阿伏加德罗常数,若晶体的密度为ρg/cm3,则S2-离子之间最短核间距离为___________ pm(用含ρ、NA的代数式表示)。
(1)基态硫原子的价电子排布式为

(2)S与O同族,H2S与H2O空间构型相同,都是2对孤电子对,但H2O分子中的键角比H2S分子中的键角大,请从成键电子对之间相互排斥的角度解释其原因
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有
| 物质 | R1-Zn-R1 | C2H5-Zn-C2H5 |
| 沸点(°C) | 46 | 118 |

您最近一年使用:0次
2023-03-14更新
|
772次组卷
|
3卷引用:江西省景德镇市2023届高三下学期第二次综合模拟考试理综化学试题
解题方法
8 . 如图甲,铜离子与有机物HA可形成一种螯合物 ,从而萃取水中的铜离子。
,从而萃取水中的铜离子。
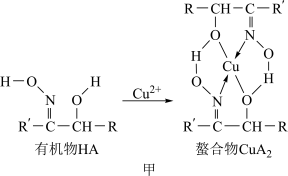
图中的R、R′均为烷烃基,该萃取反应可简单表示为2HA+Cu2+ CuA2+2H+
CuA2+2H+
回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)有机物HA中,C、N、O三种元素电负性由大到小的顺序是_______ 。
(3)螯合物 中的氮原子杂化方式为
中的氮原子杂化方式为_______ ,氧原子的杂化方式为_______ 。
(4)下列关于螯合物 的说法中,正确的是
的说法中,正确的是_______ (填序号)。
① 中O的配位能力比N强
中O的配位能力比N强
②与 配位的4个原子可能呈平面构型
配位的4个原子可能呈平面构型
③ 既溶于水又溶于有机溶剂
既溶于水又溶于有机溶剂
④每个 分子中含2个氢键、2个π键
分子中含2个氢键、2个π键
(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是_______ 。
(6)金属铜与铝可形成多种不同的合金,其中一种合金的晶胞如图乙所示,晶胞参数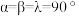 ,
, ,
,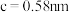 ,按图乙中阴影面进行投影得到图丙。
,按图乙中阴影面进行投影得到图丙。
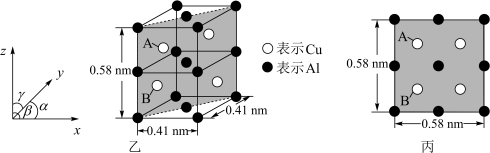
该晶体的化学式为_______ ,密度为_______  (结果保留两位有效数字)。
(结果保留两位有效数字)。
 ,从而萃取水中的铜离子。
,从而萃取水中的铜离子。
图中的R、R′均为烷烃基,该萃取反应可简单表示为2HA+Cu2+
 CuA2+2H+
CuA2+2H+回答下列问题:
(1)基态铜原子的价电子排布式为
(2)有机物HA中,C、N、O三种元素电负性由大到小的顺序是
(3)螯合物
 中的氮原子杂化方式为
中的氮原子杂化方式为(4)下列关于螯合物
 的说法中,正确的是
的说法中,正确的是①
 中O的配位能力比N强
中O的配位能力比N强②与
 配位的4个原子可能呈平面构型
配位的4个原子可能呈平面构型③
 既溶于水又溶于有机溶剂
既溶于水又溶于有机溶剂④每个
 分子中含2个氢键、2个π键
分子中含2个氢键、2个π键(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子的富集及提纯,则反萃取时常加入的试剂是
(6)金属铜与铝可形成多种不同的合金,其中一种合金的晶胞如图乙所示,晶胞参数
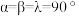 ,
, ,
,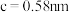 ,按图乙中阴影面进行投影得到图丙。
,按图乙中阴影面进行投影得到图丙。
该晶体的化学式为
 (结果保留两位有效数字)。
(结果保留两位有效数字)。
您最近一年使用:0次
9 . 砷化镓( )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: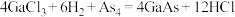 或
或 。
。
(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
(2) 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为_______ , 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是_______ ,写出一种与甲烷互为等电子体的离子的化学式:_______ 。
(3)上述反应涉及的几种元素中,电负性最大的元素是_______ ,砷可形成多种卤化物,其中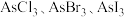 的沸点由低到高的原因为
的沸点由低到高的原因为_______ 。
(4) 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
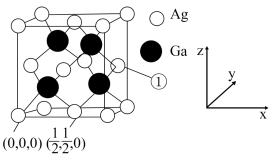
则①处原子的分数坐标为_______ ,已知紧邻的 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的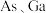 原子之间的距离为
原子之间的距离为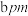 ,则
,则
_______ b,该晶胞的密度为_______  (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
 )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: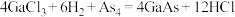 或
或 。
。(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
A.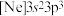 | B. | C.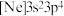 | D.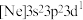 |
 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是(3)上述反应涉及的几种元素中,电负性最大的元素是
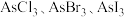 的沸点由低到高的原因为
的沸点由低到高的原因为(4)
 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
则①处原子的分数坐标为
 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的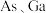 原子之间的距离为
原子之间的距离为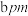 ,则
,则
 (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
您最近一年使用:0次
解题方法
10 . 有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。A、B、C、D、E五种元素的电负性分别为2.1,3.5,1.5,2.5,0.8,请回答下列问题:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ ,E是_______ (用化学符号填空,下同)。
(2)由电负性判断,以上五种元素中金属性最强的是_______ ,非金属性最强的是_______ 。
(3)当B与A、C、D分别形成化合物时,B显_______ 价(填“正”或“负”或“零”,下同),其他元素显_______ 价。
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是_______ (填化学式)。
(1)A是
(2)由电负性判断,以上五种元素中金属性最强的是
(3)当B与A、C、D分别形成化合物时,B显
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是
您最近一年使用:0次



