1 . 超导材料具有广阔的应用前景,某研究团队利用前驱体 {该物质的晶胞中存在
{该物质的晶胞中存在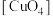 平面结构}在高温高压下合成钙基富氢材料,为寻找高温超导富氢化物提供了新的思路和途径。
平面结构}在高温高压下合成钙基富氢材料,为寻找高温超导富氢化物提供了新的思路和途径。
回答下列问题:
(1)基态钙原子的价层电子轨道表示式为______ 。第二电离能:
______  (选填“>”或“<”),理由是
(选填“>”或“<”),理由是______ 。
(2)下列说法错误的是______(填字母)。
(3)某富氢化物的晶胞结构及该晶胞沿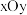 、
、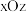 、
、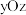 三个平面的投影(沿三个平面的投影相同)如图所示,该晶胞中,
三个平面的投影(沿三个平面的投影相同)如图所示,该晶胞中, 之间相互连接形成笼状结构。
之间相互连接形成笼状结构。 之间以
之间以______ (选填“离子键”“共价键”或“分子间作用力”)相连接。
②已知晶胞可以平移,原子分数坐标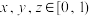 (原子分数坐标为1时记为0)。该晶胞中A原子的分数坐标为
(原子分数坐标为1时记为0)。该晶胞中A原子的分数坐标为 ,
, 原子的分数坐标为
原子的分数坐标为 ,则
,则 原子的分数坐标为
原子的分数坐标为______ 。
③该晶胞中,两个氢原子之间的最近距离为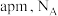 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为______  。
。
 {该物质的晶胞中存在
{该物质的晶胞中存在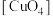 平面结构}在高温高压下合成钙基富氢材料,为寻找高温超导富氢化物提供了新的思路和途径。
平面结构}在高温高压下合成钙基富氢材料,为寻找高温超导富氢化物提供了新的思路和途径。回答下列问题:
(1)基态钙原子的价层电子轨道表示式为

 (选填“>”或“<”),理由是
(选填“>”或“<”),理由是(2)下列说法错误的是______(填字母)。
A.电负性: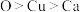 |
B.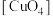 平面结构中,铜原子的杂化方式为 平面结构中,铜原子的杂化方式为 |
C.化学键中离子键成分的百分数: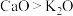 |
D.键角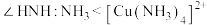 |
(3)某富氢化物的晶胞结构及该晶胞沿
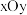 、
、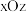 、
、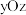 三个平面的投影(沿三个平面的投影相同)如图所示,该晶胞中,
三个平面的投影(沿三个平面的投影相同)如图所示,该晶胞中, 之间相互连接形成笼状结构。
之间相互连接形成笼状结构。
 之间以
之间以②已知晶胞可以平移,原子分数坐标
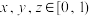 (原子分数坐标为1时记为0)。该晶胞中A原子的分数坐标为
(原子分数坐标为1时记为0)。该晶胞中A原子的分数坐标为 ,
, 原子的分数坐标为
原子的分数坐标为 ,则
,则 原子的分数坐标为
原子的分数坐标为③该晶胞中,两个氢原子之间的最近距离为
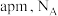 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
2 . 一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:_______ ,基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为_______ 。
(2)均为平面结构的吡咯( )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为_______ ,原因是_______ 。
(3) 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角_______  中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。
(4) (
( )中
)中 比
比 中的更
中的更_______ (填“难”或“易”)断裂。其原因是_______ 。
元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(5)在浓 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为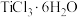 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为_______ 。
(6)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的 层与带负电的
层与带负电的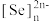 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为_______ 。晶胞棱边夹角均为 ,则晶体密度的计算式为
,则晶体密度的计算式为_______  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为(3)
 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角 中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。(4)
 (
( )中
)中 比
比 中的更
中的更元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(5)在浓
 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为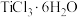 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为(6)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
 层与带负电的
层与带负电的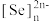 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为 ,则晶体密度的计算式为
,则晶体密度的计算式为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
3 .  、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有___________ 种;O、S、Cl电负性由大到小的顺序是___________ 。
(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是___________ (填化学式);键长 最长的是
最长的是___________ (填化学式)。已知:配离子的颜色与 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为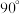 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为___________ 。若阿伏加德罗常数的值为 ,化合物
,化合物 的密度
的密度
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: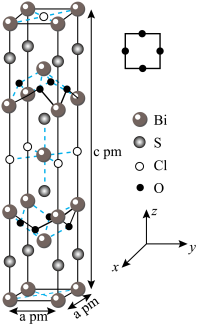
 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是
 最长的是
最长的是 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
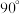 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
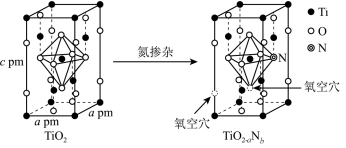
4 . 氮、磷化合物在科研和生产中有许多重要用途。回答下列问题:
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为_________ ,H、B、N的电负性由大到小的顺序为____ 。与氨硼烷互为等电子体的分子是_______ (写名称),其熔点比NH3BH3低,原因是__________ 。
(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状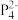 结构与苯相似,
结构与苯相似,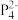 中的大π键可表示为
中的大π键可表示为___________ 。
___ 种,TiO2晶胞的密度为_________ g/cm3,TiO2-aNb 晶体中a:b=_________ 。
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H
 +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状
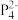 结构与苯相似,
结构与苯相似,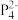 中的大π键可表示为
中的大π键可表示为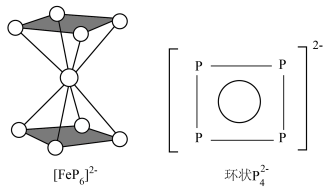
您最近一年使用:0次
名校
解题方法
5 . 氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是______ 。
(2)叠氮酸(HN3)常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
______ 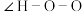 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: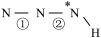 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①______ ②。
(3)乙胺( )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是______ 。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是______ 。

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是______ ,n原子的分数坐标是______ ,若阿伏加德罗常数值为 ,该晶体密度是
,该晶体密度是______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态As原子的价电子的轨道表示式是
(2)叠氮酸(HN3)常用于引爆剂,可用联氨(
 )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
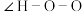 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: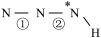 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①(3)乙胺(
 )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为
 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是 ,该晶体密度是
,该晶体密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-05-21更新
|
526次组卷
|
2卷引用:山东省潍坊市2024届高三下学期二模化学试题
解题方法
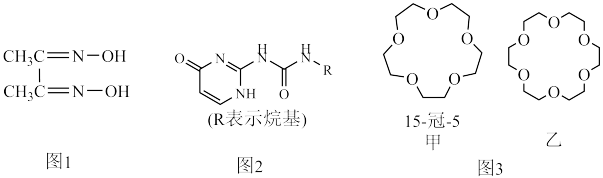
6 . 配合物和超分子广泛应用于新材料合成、物质的鉴别和分离。如丁二酮肟(如图1)可用于鉴别 Ni2+,嘧啶衍生物(如图2)是形成高韧性超分子的单体,冠醚(如图3)是皇冠状分子,可有大小不同的空穴适配不同大小的碱金属离子。
(1)基态 Ni2+核外未成对电子的数目为______ 。
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为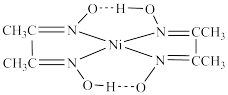 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为_______ 。
(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=_______ 。
(4)图2所示分子所含元素电负性由小到大的顺序为______ 。
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为________ ;乙的名称为______ 。
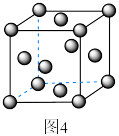
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为________ (用含π的代式表示)。
(1)基态 Ni2+核外未成对电子的数目为
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为
 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=
(4)图2所示分子所含元素电负性由小到大的顺序为
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为
您最近一年使用:0次
解题方法
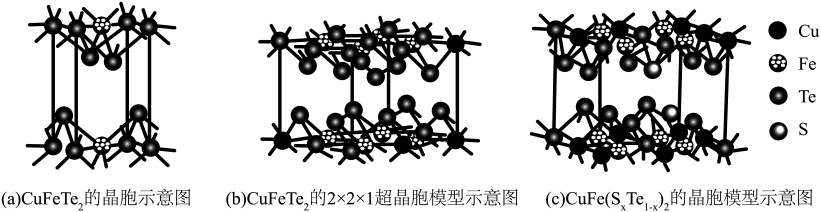
7 . 四方晶系CuFeTe2晶体是一种p型半导体,在太阳能半导体薄膜中具有巨大的潜在应用价值,其晶胞示意图如图a、图b所示。
(1)基态Cu原子的价电子排布式为___________ ;
(2)H2S中S的杂化方式为___________ ;H2O、H2Te、H2S沸点依次降低的原因是___________ 。
(3)CuFeTe2中元素的电负性由大到小的顺序为___________ ;Te的配位数为___________ 。
(4)向CuFeTe2中掺杂S原子会改善半导体性能。由图(c)可知x=___________ ;掺杂后晶胞参数分别为apm,apm,cpm,设NA为阿伏加德罗常数的值。晶体CuFe(SxTe1-x)的密度为___________ g/cm3(用含a、c和NA的代数式表示)。
(1)基态Cu原子的价电子排布式为
(2)H2S中S的杂化方式为
(3)CuFeTe2中元素的电负性由大到小的顺序为
(4)向CuFeTe2中掺杂S原子会改善半导体性能。由图(c)可知x=
您最近一年使用:0次
8 . Fe、Co、Ni、Cu均为第四周期元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为___________ 。在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是___________ 。
(2) 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有___________ 个;C、N、B的电负性由小到大的顺序为___________ 。
(3)基态 的核外电子排布式为
的核外电子排布式为___________ ; 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式___________ 、___________ 。
(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点、B点原子的分数坐标分别为 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为___________ ;晶胞中C、D间距离d=___________ pm。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为
 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是(2)
 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有(3)基态
 的核外电子排布式为
的核外电子排布式为 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为
您最近一年使用:0次
9 . 短周期元素可形成许多结构和性质不同的化合物,回答下列问题:

(1) 是一种甲基化试剂,能发生水解反应
是一种甲基化试剂,能发生水解反应 ;
; 的水解产物为
的水解产物为_____ (填化学式)。
(2) 是共价化合物,可以形成二聚体和多聚体
是共价化合物,可以形成二聚体和多聚体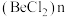 ,二聚体中
,二聚体中 的杂化方式为
的杂化方式为 ,二聚体的结构式为
,二聚体的结构式为_____ 。
(3) 分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成
分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成 的方向上时斥力最大,判断
的方向上时斥力最大,判断 应采用结构
应采用结构_____ (填“a”或“b”)。
(4) 在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了
在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了_____ (填化学式),比较它与 的稳定性并说明理由
的稳定性并说明理由_____ 。
(5)在超高压下,金属钠和氦可形成化合物。结构中的钠离子按简单立方排布,形成 立方体空隙如图,电子对
立方体空隙如图,电子对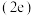 和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对
和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对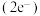 在该晶胞中的所有分数坐标除了
在该晶胞中的所有分数坐标除了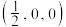 、
、 ,还有
,还有_____ ;若晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞的边长
,晶胞的边长
_____  (用含
(用含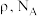 的代数式表示)。
的代数式表示)。


(1)
 是一种甲基化试剂,能发生水解反应
是一种甲基化试剂,能发生水解反应 ;
; 的水解产物为
的水解产物为(2)
 是共价化合物,可以形成二聚体和多聚体
是共价化合物,可以形成二聚体和多聚体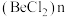 ,二聚体中
,二聚体中 的杂化方式为
的杂化方式为 ,二聚体的结构式为
,二聚体的结构式为(3)
 分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成
分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成 的方向上时斥力最大,判断
的方向上时斥力最大,判断 应采用结构
应采用结构(4)
 在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了
在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了 的稳定性并说明理由
的稳定性并说明理由(5)在超高压下,金属钠和氦可形成化合物。结构中的钠离子按简单立方排布,形成
 立方体空隙如图,电子对
立方体空隙如图,电子对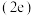 和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对
和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对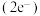 在该晶胞中的所有分数坐标除了
在该晶胞中的所有分数坐标除了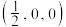 、
、 ,还有
,还有 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞的边长
,晶胞的边长
 (用含
(用含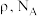 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
10 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知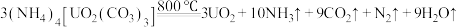 。
。
①基态U原子的外围电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________ (填标号)。
A. B.
B. 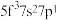 C.
C. 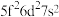 D.
D. 
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式___________ 。
(2)一个配体中有两个配位原子的配体叫双齿配体,C2O 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为___________
(3)四羰基镍 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是___________ 。
(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为___________ (保留三位小数)。

(1)已知
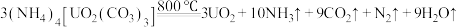 。
。①基态U原子的外围电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是A.
 B.
B. 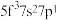 C.
C. 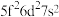 D.
D. 
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式(2)一个配体中有两个配位原子的配体叫双齿配体,C2O
 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为(3)四羰基镍
 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为

您最近一年使用:0次
2024-04-03更新
|
277次组卷
|
2卷引用:山东省济宁市第一中学2023-2024学年高三下学期3月月考化学试题



