解题方法
1 . 氯元素可形成多种含氧酸,下列含氧酸或含氧酸根离子中,键角最大的是
| A.HClO | B. | C. | D. |
您最近一年使用:0次
解题方法
2 . 下列说法错误的是
| A.SO2和CO2的价层电子对互斥模型相同 |
| B.NH3和CH4的中心原子杂化方式相同 |
| C.C2H6和C2H4的化学键类型不同,可用溴水除去C2H6中混有的C2H4 |
| D.水和苯分子极性不同,可用分液法分离 |
您最近一年使用:0次
2024-03-23更新
|
393次组卷
|
2卷引用:河北省唐山市2023-2024学年高三一模化学试题
名校
解题方法
3 . 硫在不同温度下的状态和分子结构不同,单质硫S8环状分子的结构如图。隔绝空气,717.6K时硫变为蒸气,蒸气中存在3S8 4S6
4S6 6S4
6S4 12S2,温度越高,蒸气的平均相对分子质量越小。下列说法正确的是
12S2,温度越高,蒸气的平均相对分子质量越小。下列说法正确的是
 4S6
4S6 6S4
6S4 12S2,温度越高,蒸气的平均相对分子质量越小。下列说法正确的是
12S2,温度越高,蒸气的平均相对分子质量越小。下列说法正确的是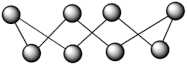
A.对于3S8 4S6 4S6 6S4 6S4 12S2,△H<0 12S2,△H<0 |
| B.S8分子中,原子数与共价键数之比为1:2 |
| C.S8分子中S-S-S的键角为109°28′ |
| D.S8、S6、S4、S2互为同素异形体,其相互转化为化学变化 |
您最近一年使用:0次
2024-03-21更新
|
50次组卷
|
4卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
河北正定中学本部2023-2024学年高二上学期期末考试化学试题河北省石家庄市河北正定中学2023-2024年高二上学期期末考试化学试题江苏省常州市联盟校2023-2024学年高二下学期3月阶段调研化学试题(已下线)2.1.2 键参数——键能、键长与键角课堂例题
名校
解题方法
4 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:乙醇(78.3℃)高于二甲醚(-29.5℃) | 氢键作用 |
| B | 熔点:AlF3(1040℃)远高于AlCl3(178℃升华) | 晶体类型 |
| C | 键角:PF3(94°)小于PCl3(109.5°) | 电负性差异 |
| D | 分解温度:HBr(500℃)高于HI(300℃) | 范德华力作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-15更新
|
918次组卷
|
4卷引用:河北省唐山市2023-2024学年高三一模化学试题
河北省唐山市2023-2024学年高三一模化学试题河北省唐山市2024届高三一模化学试题河北省石家庄市第二中学2023-2024学年高三下3月T8联考化学试题(已下线)通关练07 原子、分子、晶体结构再归纳-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
5 .  为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是

 为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
A.原子半径: |
B.气态氢化物的稳定性: |
C.加热时该离子首先失去的组分是 |
D.两种配体中的键角: |
您最近一年使用:0次
名校
6 . 下列化学用语表述不正确的是
A.基态 原子的价层电子排布图(轨道表示式): 原子的价层电子排布图(轨道表示式):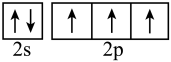 |
B. 分子的球棍模型: 分子的球棍模型: |
C. 的空间结构: 的空间结构: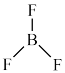 (平面三角形) (平面三角形) |
D. 分子的 分子的 模型: 模型: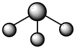 |
您最近一年使用:0次
名校
解题方法
7 . 下列化学用语使用正确的是
A.乙烯的碳碳 键的电子云形状为: 键的电子云形状为: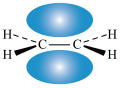 |
B. 分子的VSEPR模型: 分子的VSEPR模型: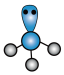 |
C. 的电子式为: 的电子式为: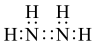 |
D.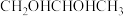 的名称为:丙二醇 的名称为:丙二醇 |
您最近一年使用:0次
名校
8 . 类推是化学学习和研究中常用的思维方法。下列类推正确的是
A. 为直线形分子,则 为直线形分子,则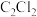 也为直线形分子 也为直线形分子 |
| B.N原子之间可以形成N=N,则P原子之间也可形成P=P |
C. 分子的空间结构为V形,则 分子的空间结构为V形,则 的VSEPR模型也是V形 的VSEPR模型也是V形 |
D.基态V的价层电子排布式为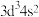 ,基态Cr的价层电子排布式为 ,基态Cr的价层电子排布式为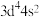 |
您最近一年使用:0次
2024-03-02更新
|
276次组卷
|
2卷引用:河北省沧州市十校2023-2024学年高二下学期3月月考化学试题
名校
解题方法
9 . 化合物XYZ4ME4可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
| A.元素电负性:E>Y>Z | B.1mol M中含有共价键数目为4NA |
| C.半径:X2+>E2- | D.YZ3和YE 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题。
(1)写出基态As原子的简化电子排布式:___________ ,其核外有___________ 种不同空间运动状态的电子。
(2)1 mol [Ni(NH3)6]SO4中σ键的数目为___________ NA。
(3)SCN-中C原子的杂化轨道类型为___________ ,其中含有两个相同的大π键,其形式为___________ (用 表示,n为原子数,m为电子数),检验Fe3+时,SCN-以S原子配位不以N原子配位的原因是
表示,n为原子数,m为电子数),检验Fe3+时,SCN-以S原子配位不以N原子配位的原因是___________ 。
(4)某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第___________ 族。
(5)光气(COCl2)分子中,所有原子均满足8电子稳定结构,其电子式为___________ 。
(6)下列酸中:CF3COOH、CCl3COOH、CHCl2COOH、CH2ClCOOH,酸性最强的是___________ 。
(7)已知:硫代乙酰胺(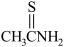 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(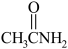 )和硫化氢,硫代乙酰胺比乙酰胺的沸点低,解释其原因为
)和硫化氢,硫代乙酰胺比乙酰胺的沸点低,解释其原因为___________ 。
(8)H3BO3分子中的O-B-O的键角___________ (填“大于”“等于”或“小于”) 中的H-B-H的键角,判断依据是
中的H-B-H的键角,判断依据是___________ 。
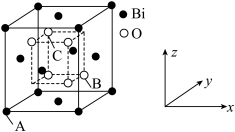
(9)Bi2O3的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为( ,
, ,
, ),则C点坐标为
),则C点坐标为___________ 。
(1)写出基态As原子的简化电子排布式:
(2)1 mol [Ni(NH3)6]SO4中σ键的数目为
(3)SCN-中C原子的杂化轨道类型为
 表示,n为原子数,m为电子数),检验Fe3+时,SCN-以S原子配位不以N原子配位的原因是
表示,n为原子数,m为电子数),检验Fe3+时,SCN-以S原子配位不以N原子配位的原因是(4)某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 578 | 1817 | 2748 | 11575 | 14830 | 18376 | 23293 |
(5)光气(COCl2)分子中,所有原子均满足8电子稳定结构,其电子式为
(6)下列酸中:CF3COOH、CCl3COOH、CHCl2COOH、CH2ClCOOH,酸性最强的是
(7)已知:硫代乙酰胺(
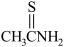 )在酸性溶液中会水解为乙酰胺(
)在酸性溶液中会水解为乙酰胺(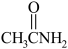 )和硫化氢,硫代乙酰胺比乙酰胺的沸点低,解释其原因为
)和硫化氢,硫代乙酰胺比乙酰胺的沸点低,解释其原因为(8)H3BO3分子中的O-B-O的键角
 中的H-B-H的键角,判断依据是
中的H-B-H的键角,判断依据是(9)Bi2O3的立方晶胞结构如图所示,以A点为原点建立分数坐标,已知A点坐标为(0,0,0),B点坐标为(
 ,
, ,
, ),则C点坐标为
),则C点坐标为
您最近一年使用:0次



