名校
解题方法
1 . 根据所学内容填空:
(1)有下列物质:①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是_______ (填序号,下同),既有 键又有
键又有 键的是
键的是_______ 。
(2)下列分子中,空间构型为正四面体且键角为109°28′的是_______ 。
a. b.
b. c.
c.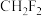 d.
d. e.
e. f.
f.
(3) 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
(4)丙烯腈分子( )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为_______ 。
(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
① 的酸性比
的酸性比
_______ (填“强”或“弱”)。 离子的空间构型为
离子的空间构型为_______ 。
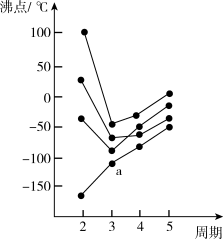
②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (化学式)。
(1)有下列物质:①HF、②
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为109°28′的是
a.
 b.
b. c.
c.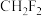 d.
d. e.
e. f.
f.
(3)
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯腈分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
①
 的酸性比
的酸性比
 离子的空间构型为
离子的空间构型为②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
您最近一年使用:0次
2022-04-09更新
|
433次组卷
|
3卷引用:河北省衡水市第二中学2021-2022学年高二下学期期中考试化学试题
解题方法
2 . 铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO ⇌ [Cu(NH3)3CO]+,2CH3COOH +2CH2=CH2+O2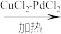 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为______ 。
(2)NH3分子空间构型为_______ , 其中心原子的杂化类型是______ 。
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是_______ ,1mol CH3COOCH=CH2中含 键数目为
键数目为_____ 。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为__________ 。
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构示意图表示为____
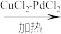 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。(1)Cu2+基态核外电子排布式为
(2)NH3分子空间构型为
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是
 键数目为
键数目为(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构示意图表示为
您最近一年使用:0次
名校
解题方法
3 . 铜是重要的过渡元素,其单质及化合物具有广泛用途。回答下列问题:
(1)铜元素基态原子的价电子排布式为________ 。
(2)铜元素能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。
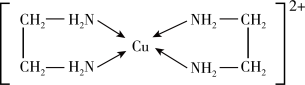
①Cu2+与乙二胺所形成的配离子内部粒子间的作用力类型有________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
②乙二胺分子中氮原子的杂化轨道类型为________ ,C、N、H三种元素的电负性由大到小顺序是 ___ 。
③乙二胺和三甲胺 [N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是________ 。
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是______ 。
(4)Cu和S形成某种晶体的晶胞如图所示。
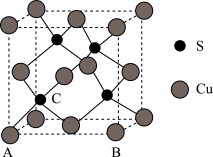
①该晶体的化学式为________ 。
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为________
③已知该晶体的密度为 dg•cm-3,Cu2+和S2-的半径分别为apm和bpm,阿伏加 德罗常数值为NA。列式表示该晶体中原子的空间利用率________ 。
(1)铜元素基态原子的价电子排布式为
(2)铜元素能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。

①Cu2+与乙二胺所形成的配离子内部粒子间的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
②乙二胺分子中氮原子的杂化轨道类型为
③乙二胺和三甲胺 [N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是
(4)Cu和S形成某种晶体的晶胞如图所示。

①该晶体的化学式为
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为
③已知该晶体的密度为 dg•cm-3,Cu2+和S2-的半径分别为apm和bpm,阿伏加 德罗常数值为NA。列式表示该晶体中原子的空间利用率
您最近一年使用:0次
2020-09-01更新
|
805次组卷
|
4卷引用:河北省河北衡水中学2021届高三下学期第二次调研考试化学试题
名校
解题方法
4 . [化学——选修3:物质结构与性质]硼及其化合物用途非常广泛,回答下列问题。
(1)下列B原子电子排布图表示的状态中,能量最低和最高的分别为________ 、________ (填标号)

(2)H3BO3是一元弱酸,可用作医用消毒剂,其水溶液呈酸性的原理为:

则1mol硼酸分子中含有的共用电子对数为________ 个。
(3)BF3可用于制造火箭的高能燃料,其分子的空间构型是________________ ,硼原子杂化方式是________________ ;BF3能与乙醚发生反应:(C2H5)2O+BF3→BF3·O(C2H5)2,该反应能发生,其原因是________________________________ 。
(4)硼的一种化合物结构简式为O=B—CH=C=CH2,该分子中含________ 个σ键。
(5)下图中图(a)为类似石墨的六方BN,图(b)为立方BN。

①六方BN具有良好的润滑性,是因为________________________ ;六方BN不能像石墨一样具有导电性,其原因是________________________ 。
②已知立方BN的晶胞参数为0.3615nm,阿伏伽德罗常数的值为NA,则立方BN的密度为________________ g·cm-3(列出计算式)。
(1)下列B原子电子排布图表示的状态中,能量最低和最高的分别为

(2)H3BO3是一元弱酸,可用作医用消毒剂,其水溶液呈酸性的原理为:

则1mol硼酸分子中含有的共用电子对数为
(3)BF3可用于制造火箭的高能燃料,其分子的空间构型是
(4)硼的一种化合物结构简式为O=B—CH=C=CH2,该分子中含
(5)下图中图(a)为类似石墨的六方BN,图(b)为立方BN。

①六方BN具有良好的润滑性,是因为
②已知立方BN的晶胞参数为0.3615nm,阿伏伽德罗常数的值为NA,则立方BN的密度为
您最近一年使用:0次
2019-01-05更新
|
672次组卷
|
3卷引用:【省级联考】河北省衡水金卷2019届高三第三次联合质量测评理综化学试题
解题方法
5 . 选考[化学——物质结构与性质]由Cu、N、B、Ni等元素组成的新型材料有着广泛用途。
(1)基态 Cu+的最外层核外电子排布式为_________ .
(2)研究者预想合成一个纯粹由氮组成的新物种 N5+N3-,若N5+ 离子中每个氮原子均满足8电子结构,以下有关N5+ 推测正确的是( )
A.N5+有24个电子
B.N5+离子中存在三对未成键的电子对
C.N5+阳离子中存在两个氮氮三键
(3)化合物 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物 。通过
。通过 制得。
制得。
①与上述化学方程式有关的叙述不正确的是_________ (填标号)。
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1个 分子中有
分子中有_________ 个 键。
键。
(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为_________ 图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为_________ 。

(5)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为_________ (用含有a的代数式表示)。在一定温度下,Ni0晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为_________ g(氧离子的半径为1. 40×10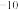 m,
m,  ≈l. 732)。
≈l. 732)。

(1)基态 Cu+的最外层核外电子排布式为
(2)研究者预想合成一个纯粹由氮组成的新物种 N5+N3-,若N5+ 离子中每个氮原子均满足8电子结构,以下有关N5+ 推测正确的是
A.N5+有24个电子
B.N5+离子中存在三对未成键的电子对
C.N5+阳离子中存在两个氮氮三键
(3)化合物
 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物 。通过
。通过 制得。
制得。①与上述化学方程式有关的叙述不正确的是
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1个
 分子中有
分子中有 键。
键。(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为

(5)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为
 m,
m,  ≈l. 732)。
≈l. 732)。
您最近一年使用:0次



