名校
1 . 海带灼烧、溶解、过滤后得到含 的溶液.再经以下步骤得到碘单质:
的溶液.再经以下步骤得到碘单质:
 的溶液.再经以下步骤得到碘单质:
的溶液.再经以下步骤得到碘单质: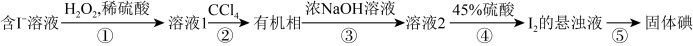
| A.由溶液1到碘的悬浊液的过程实现了碘的富集 |
| B.步骤②和步骤③所用的操作方法相同 |
| C.上述过程中发生的氧化还原反应有2个 |
| D.分液时先打开分液漏斗上口玻璃塞,再打开下端活塞 |
您最近一年使用:0次
2024-05-29更新
|
270次组卷
|
2卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
名校
解题方法
2 . 聚合硫酸铝铁(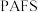 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为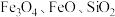 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为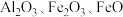 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下:___________ (填序号)。
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有___________ (填化学符号)。
(2)检验“氧化”后溶液中金属阳离子的方法是___________ 。
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是___________ 。
(4)“酸溶”过程中发生反应的离子方程式为___________ 。
(5)滤渣Ⅱ中可以循环利用的物质是___________ (填化学式)。
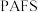 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为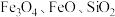 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为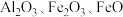 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下: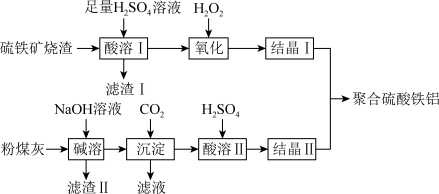
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有
(2)检验“氧化”后溶液中金属阳离子的方法是
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是
(4)“酸溶”过程中发生反应的离子方程式为
(5)滤渣Ⅱ中可以循环利用的物质是
您最近一年使用:0次
2024-04-24更新
|
200次组卷
|
2卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
名校
3 . 实验室用化学沉淀法除去粗盐中的杂质离子,并利用提纯干燥后的 配制一定浓度的
配制一定浓度的 溶液。下列有关说法不正确的是
溶液。下列有关说法不正确的是
 配制一定浓度的
配制一定浓度的 溶液。下列有关说法不正确的是
溶液。下列有关说法不正确的是| A.本实验需要用到的玻璃仪器有酒精灯、量筒、烧杯、玻璃棒、胶头滴管、漏斗、容量瓶 |
B.本实验需要用到的试剂有 溶液、 溶液、 溶液、 溶液、 溶液、盐酸 溶液、盐酸 |
| C.化学沉淀法除去杂质离子过程中只需过滤一次即可,将滤液倒入坩埚中加热蒸发,玻璃棒搅拌,出现较多晶体时停止加热 |
D.配制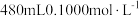 的 的 溶液时,需要用托盘天平称取纯品 溶液时,需要用托盘天平称取纯品 |
您最近一年使用:0次
2024-04-22更新
|
102次组卷
|
2卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
名校
解题方法
4 . 某化学兴趣小组拟按如下步骤合成铁系催化剂的中间体[Fe(CO)2Cl2]: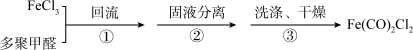
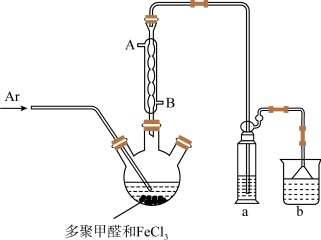
其中步骤①实验装置如图所示:
已知:
(I)多聚甲醛为(CH2O)n(n=6~100),当n<12的多聚甲醛可溶于水,当n≥12则不溶于水;加酸或160~200°C加热时会解聚。
(Ⅰ)[Fe(CO)2Cl2]遇氧气、水都会反应,其中Fe的化合价为+2价。
(Ⅱ)SnCl2有强还原性,可被弱氧化剂HgCl2氧化:2HgCl2+SnCl2=Hg2Cl2↓+SnCl4。
请回答:
(1)步骤③产物干燥后仍需放置在干燥器中,以下称为干燥器的是_______。
(2)操作步骤②时仍需在氩气氛围下完成,理由是_______ 。
(3)写出生成[Fe(CO)2Cl2]的化学反应方程式_______ 。
(4)仪器a中盛放的试剂为_______ ,装置b的作用是_______ 。
(5)测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序:_______ 。
c→ →a→ → →f
a.将准确称量的[Fe(CO)2Cl2]溶解于水
b.准确称量Na2C2O4并配制一定物质的量浓度的溶液,进行滴定
c.将制备的KMnO4溶液加热煮沸,冷却后滤去MnO2
d.用HgCl2除过量的SnCl2,滤去沉淀
e.加入足量SnCl2进行还原
f.用Na2C2O4标准溶液标定后的KMnO4溶液进行滴定
下列情况会导致测量结果偏大的是_______ 。
A.[Fe(CO)2Cl2]产品含少量多聚甲醛杂质
B.过量的SnCl2未被除尽
C.[Fe(CO)2Cl2]产品部分氧化或潮解
D.配好的KMnO4标准溶液久置后使用

其中步骤①实验装置如图所示:

已知:
(I)多聚甲醛为(CH2O)n(n=6~100),当n<12的多聚甲醛可溶于水,当n≥12则不溶于水;加酸或160~200°C加热时会解聚。
(Ⅰ)[Fe(CO)2Cl2]遇氧气、水都会反应,其中Fe的化合价为+2价。
(Ⅱ)SnCl2有强还原性,可被弱氧化剂HgCl2氧化:2HgCl2+SnCl2=Hg2Cl2↓+SnCl4。
请回答:
(1)步骤③产物干燥后仍需放置在干燥器中,以下称为干燥器的是_______。
A. | B. | C.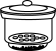 | D. |
(2)操作步骤②时仍需在氩气氛围下完成,理由是
(3)写出生成[Fe(CO)2Cl2]的化学反应方程式
(4)仪器a中盛放的试剂为
(5)测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序:
c→ →a→ → →f
a.将准确称量的[Fe(CO)2Cl2]溶解于水
b.准确称量Na2C2O4并配制一定物质的量浓度的溶液,进行滴定
c.将制备的KMnO4溶液加热煮沸,冷却后滤去MnO2
d.用HgCl2除过量的SnCl2,滤去沉淀
e.加入足量SnCl2进行还原
f.用Na2C2O4标准溶液标定后的KMnO4溶液进行滴定
下列情况会导致测量结果偏大的是
A.[Fe(CO)2Cl2]产品含少量多聚甲醛杂质
B.过量的SnCl2未被除尽
C.[Fe(CO)2Cl2]产品部分氧化或潮解
D.配好的KMnO4标准溶液久置后使用
您最近一年使用:0次
5 . 亚铁氰化钾K4[Fe(CN)6]是一种黄色颜料。以含铁废水[主要成分为Fe2(SO4)3,含少量NiSO4,CuSO4等]为原料合成亚铁氰化钾的工艺流程如下:
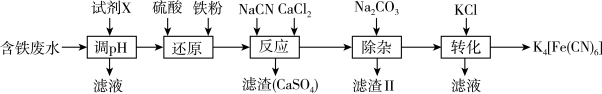
下列说法不正确 的是

下列说法
| A.“调pH”时选用的试剂X可以是钢和镍的氧化物 |
| B.“还原”后可用KSCN溶液检验Fe3+是否被完全还原 |
| C.“反应”时Fe2+提供孤电子对给予CN-形成配位键 |
| D.“滤液Ⅱ”的主要成分是CaCO3 |
您最近一年使用:0次
2022-12-16更新
|
467次组卷
|
3卷引用:浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题
6 . 下列实验操作,不能用于物质分离的是
A.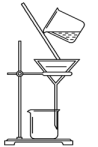 | B.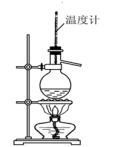 | C. | D.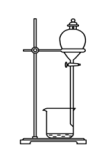 |
您最近一年使用:0次
2022-09-14更新
|
461次组卷
|
68卷引用:浙江省舟山市舟山中学2022-2023学年国庆返校检测高三化学试题
浙江省舟山市舟山中学2022-2023学年国庆返校检测高三化学试题(已下线)2013年新疆乌鲁木齐市一中学业水平化学试卷(1月份)湖南省衡阳县第四中学2019届高三第一次月考(9月)化学试题【市级联考】辽宁省大连市2019届高三下学期学业水平模拟考试化学试题(已下线)专题10.1 常见仪器使用和实验基本操作(练)-《2020年高考一轮复习讲练测》(已下线)09~10年淮安市淮阴区高一下学期期末调查测试化学卷(已下线)2010年四川省成都九中高一上学期期中考试化学试卷(已下线)2011-2012学年北京市重点中学高二上学期期中考试化学(文)试卷(已下线)2011-2012学年重庆市万州二中高一上学期期中考试化学试卷(已下线)2011-2012学年广东省揭阳一中高一上学期期末考试化学试卷(已下线)2011-2012学年湖南省凤凰县华鑫中学高二下期中考试文化学试卷(已下线)2012-2013学年浙江省苍南县求知中学高二上学期期中考试文科化学试卷(已下线)2012-2013学年河北省石家庄市第一中学高一上学期期中考试化学试卷(已下线)2013-2014学年江苏南京市建邺高级中学高一上学期期中考试化学试卷(已下线)2013-2014学年广东省东莞市高一上学期期末考试化学试卷(A)(已下线)2013-2014学年江苏省淮安市高中教学协作体高一上学期期末化学试卷(已下线)2013-2014学年江苏省淮安市高中协作体高二下学期期中考试化学试卷(已下线)2014届浙江省杭州外国语学校高二第二学期期中考试化学试卷 (已下线)2013-2014江苏省南京市高一下学期期末学情调研测试化学试卷2014-2015学年内蒙古巴市一中高一10月月考化学试卷2014西藏拉萨中学高一上学期期末考试化学试卷2014-2015广东省湛江市高一上学期期末考试化学试卷2014-2015广东省揭阳市第一中学高二上学期期末考试化学文试卷2013-2014广东省东莞市高一上学期期末化学A试卷2015-2016学年江苏省华士、成化、山观三校高一上期中联考化学试卷2015-2016学年吉林省吉林一中高二上11月月考化学试卷12015-2016学年河北省定兴三中高一上学期12月月考化学试卷2015-2016学年广东省深圳市宝安中学高一上学期期末化学试卷2015-2016学年江西省临川二中高二下第一次月考化学试卷贵州省铜仁市一中2016-2017学年高一上期中化学试卷2016-2017学年福建省三明一中高二上期中文化学卷2016-2017学年浙江省杭州市五校高一上学期联考化学试卷天津市静海县第一中学2016-2017学年高一6月月考(文)化学试题广东省北京师范大学东莞石竹附属学校2017-2018学年高一上学期期中考试化学试题江苏省盐城市时杨中学2017-2018学年高一上学期期中考试化学试题云南省峨山彝族自治县第一中学2017-2018学年高一12月月考化学试题江苏省宿迁市2017—2018学年度高二第一学期期末化学试卷【全国百强校】广西陆川县中学2017-2018学年高一下学期期末考试化学试题【全国百强校】山西省实验中学2018-2019学年高一上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高二(文)上学期期中考试化学试题海南省海南枫叶国际学校2018-2019学年高一上学期期中考试化学试题【校级联考】吉林省辽源市田家炳高级中学(第六十六届友好学校)2018-2019学年高一上学期期末联考化学试题辽宁省大连渤海高级中学2017-2018学年高二上学期期中考试化学(文)试题内蒙古杭锦后旗奋斗中学2017-2018学年高一上学期期中考试化学试题河南省鲁山县第一高级中学2019-2020学年高一9月月考化学试卷试题贵州省凯里市第一中学2019-2020学年高二上学期期中考试化学(文)试题黑龙江省绥化市青冈县第一中学2019-2020学年高一上学期期中考试(A班)化学试题江苏省苏州市吴江平望中学2019-2020学年高一上学期期中考试化学试题湖南省株洲市攸县三中2019-2020学年高一上学期第一次月考化学试题江苏省连云港市赣榆区海头高级中学2019-2020学年高一上学期期中考试化学试题江西省南昌市新建县第一中学2019-2020学年高一上学期期末考试(共建部)化学试题甘肃省定西市岷县第二中学2019-2020学年高一上学期第三次月考化学试题江苏省淮阴中学2019-2020学年高一下学期期末考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高一10月月考化学试题广东省湛江市2017-2018学年高一上学期期末考试化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(文)试题广西岑溪市2020-2021学年高一上学期期中考试化学试题江苏省苏州市苏州大学附属中学2020-2021学年高一上学期月考化学试卷1江苏省淮安市淮安区2020-2021学年高一上学期期中调研测试化学试题江苏省宿迁市沭阳县正德中学2021-2022学年高二上学期9月月考化学试题浙江省绍兴市第一中学2016-2017学年高一下学期期末考试化学试题贵州省凯里市第一中学2021-2022学年高二上学期期中考试化学(文科)试题江苏省盐城市田家炳中学2021-2022学年高一上学期期中考试化学试题江苏省淮安市淮安区2021-2022学年高一上学期期中调研测试化学试题江苏省淮安市淮安区2021-2022学年高二上学期期中调研测试化学试题江苏省扬州中学2022-2023学年高一上学期期中检测化学试题江苏省奔牛高级中学、江苏省武进高级中学2022~2023学年高一上学期期中联考化学试题江苏省扬州市新华中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
7 .  可用于制备
可用于制备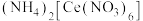 等重要的含铈化合物。实验室由含铈矿物(主要含
等重要的含铈化合物。实验室由含铈矿物(主要含 还含
还含 等杂质)制备
等杂质)制备 的主要实验过程如下:
的主要实验过程如下:
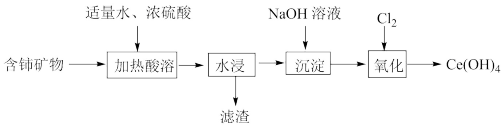
已知: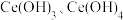 分别为灰白色、黄色难溶物。
分别为灰白色、黄色难溶物。
(1)“加热酸溶”步骤中不使用玻璃仪器而应使用铅制容器,其主要原因是___________ ; 与浓硫酸反应生成
与浓硫酸反应生成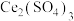 的化学方程式为
的化学方程式为___________ 。
(2)“水浸”过程得到的滤渣主要成分为___________ 。
(3)“沉淀”步骤中得到的沉淀为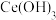 ,能证明沉淀已完全的实验操作为
,能证明沉淀已完全的实验操作为___________ 。
(4)制备 的装置如下图所示:
的装置如下图所示:

①置a的烧瓶中盛放的固体为___________ (填化学式);
②制备 的实验方案为:按照上图搭好装置,
的实验方案为:按照上图搭好装置,___________ ,加入药品,打开电动搅拌装置,___________ ,停止通 后改通空气一段时间,将装置b中的反应混合物取出,
后改通空气一段时间,将装置b中的反应混合物取出,___________ ,低温晾干即得到较纯净的 。
。
 可用于制备
可用于制备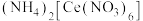 等重要的含铈化合物。实验室由含铈矿物(主要含
等重要的含铈化合物。实验室由含铈矿物(主要含 还含
还含 等杂质)制备
等杂质)制备 的主要实验过程如下:
的主要实验过程如下:
已知:
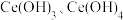 分别为灰白色、黄色难溶物。
分别为灰白色、黄色难溶物。(1)“加热酸溶”步骤中不使用玻璃仪器而应使用铅制容器,其主要原因是
 与浓硫酸反应生成
与浓硫酸反应生成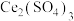 的化学方程式为
的化学方程式为(2)“水浸”过程得到的滤渣主要成分为
(3)“沉淀”步骤中得到的沉淀为
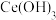 ,能证明沉淀已完全的实验操作为
,能证明沉淀已完全的实验操作为(4)制备
 的装置如下图所示:
的装置如下图所示:
①置a的烧瓶中盛放的固体为
②制备
 的实验方案为:按照上图搭好装置,
的实验方案为:按照上图搭好装置, 后改通空气一段时间,将装置b中的反应混合物取出,
后改通空气一段时间,将装置b中的反应混合物取出, 。
。
您最近一年使用:0次
2022-09-10更新
|
282次组卷
|
2卷引用:浙江省舟山市定海第一中学2022-2023学年高三上学期9月月考化学试题
名校
8 . OMS-2是一种新型环保催化剂,某实验小组以软锰矿(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料模拟工业制法的流程如下:
等杂质)为原料模拟工业制法的流程如下:

已知:实验装置见图1,“浸锰”步骤中实验温度对反应影响的变化关系如图2。

请回答:
(1)仪器A名称为_______ ,X溶液的作用是_______ 。
(2)制备流程中,需要向滤液1中加入适量的H2O2溶液,其主要目的是_______ 。
(3)下列有关表述或操作中,正确的是_______。
(4)下图为 的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:
的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:

a.在20℃蒸发溶剂;b.在90℃蒸发溶剂;
c.冷却至室温;d.真空干燥;
e.将滤液2转移至蒸发皿中;f.趁热过滤;
g.蒸发至溶液出现晶膜;h.蒸发至大量晶体产生;
i.用冷水洗涤晶体;k.用90℃热水洗涤晶体。
则正确的操作顺序为e→()→()→()→()→d。_____________
(5)某同学采用沉淀 的方法来分析
的方法来分析 晶体,测定表明产品纯度为103%,导致该误差的可能原因是
晶体,测定表明产品纯度为103%,导致该误差的可能原因是_______ 。
 ,含少量
,含少量 、
、 、
、 等杂质)为原料模拟工业制法的流程如下:
等杂质)为原料模拟工业制法的流程如下:
已知:实验装置见图1,“浸锰”步骤中实验温度对反应影响的变化关系如图2。

请回答:
(1)仪器A名称为
(2)制备流程中,需要向滤液1中加入适量的H2O2溶液,其主要目的是
(3)下列有关表述或操作中,正确的是_______。
| A.滤液1的pH调节可选用KOH、氨水等碱溶液 |
B.“浸锰”过程中,通过增加SO2的通入量、控制通气速度可提升 的浸出率 的浸出率 |
C.为减少“浸锰”反应中生成副产物 ,恒温电磁炉最适宜的控制温度是90℃ ,恒温电磁炉最适宜的控制温度是90℃ |
D.用相应滤液作洗涤剂充分洗涤滤渣1和滤渣2,有助于提高 的产率与纯度 的产率与纯度 |
 的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:
的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:
a.在20℃蒸发溶剂;b.在90℃蒸发溶剂;
c.冷却至室温;d.真空干燥;
e.将滤液2转移至蒸发皿中;f.趁热过滤;
g.蒸发至溶液出现晶膜;h.蒸发至大量晶体产生;
i.用冷水洗涤晶体;k.用90℃热水洗涤晶体。
则正确的操作顺序为e→()→()→()→()→d。
(5)某同学采用沉淀
 的方法来分析
的方法来分析 晶体,测定表明产品纯度为103%,导致该误差的可能原因是
晶体,测定表明产品纯度为103%,导致该误差的可能原因是
您最近一年使用:0次
2022-09-07更新
|
255次组卷
|
2卷引用:浙江省舟山市舟山中学2022-2023学年国庆返校检测高三化学试题
名校
9 . 蒸馏操作时,需要用到的仪器
A. | B. | C. | D. |
您最近一年使用:0次
2022-09-02更新
|
182次组卷
|
2卷引用:浙江省舟山市普陀中学2022-2023学年高三上学期9月月考化学试题
名校
解题方法
10 . 下列气体中,既可用浓硫酸干燥,又可用NaOH固体干燥的是
| A.Cl2 | B.NH3 | C.O2 | D.HCl |
您最近一年使用:0次
2022-07-13更新
|
291次组卷
|
2卷引用:浙江省舟山市普陀中学2023届高三返校考试化学试题



