2023高三·全国·专题练习
1 . 利用废镍电池的金属电极芯(主要成分为Co、Ni,还含少量Fe、Al等)生产醋酸钴晶体、硫酸镍晶体的工艺流程如图。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀A的主要成分是Fe(OH)3、______ ,“浸出液”调节pH的范围为_____ ,调节pH选用的试剂可以是______ (填字母)。
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Co(OH)3 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀pH | 2.2 | 7.4 | 7.6 | 0.1 | 4.0 | 7.6 |
| 完全沉淀pH | 3.2 | 8.9 | 9.2 | 1.1 | 5.2 | 9.2 |
沉淀A的主要成分是Fe(OH)3、
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸
您最近一年使用:0次
名校
解题方法
2 . 铈(Ce)是一种典型的稀土元素,属于国家战略资源。以某废料(主要含 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈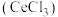 ,主要步骤如下:
,主要步骤如下:
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
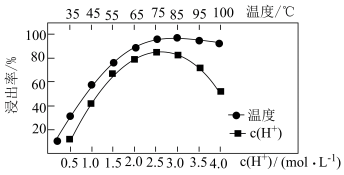
不溶于水,写出其发生反应的离子方程式:________ 。Ce的浸出率与 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为________ 。
(2)除杂:向浸出液中加入NaOH溶液调节pH除去 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度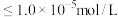 )。
)。
则 的
的
________ ,若浸取液中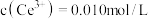 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是________ (加入NaOH溶液过程忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应: (水层)+3HT(有机层)
(水层)+3HT(有机层)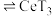 (有机层)
(有机层)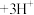 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入_______ 能获得较纯的 溶液。
溶液。
结晶析出:将 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到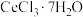 晶体。
晶体。
(4)加热脱水:将 固体和
固体和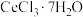 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是________ 。
(5)对 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵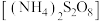 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用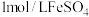 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为________ %(保留小数点后两位)。
 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈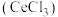 ,主要步骤如下:
,主要步骤如下:(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有
 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
不溶于水,写出其发生反应的离子方程式: 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为
(2)除杂:向浸出液中加入NaOH溶液调节pH除去
 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度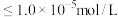 )。
)。沉淀 |
|
|
|
|
恰好完全沉淀时pH | 5.2 | 2.8 | 9.0 | 10.1 |
 的
的
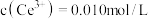 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:
 (水层)+3HT(有机层)
(水层)+3HT(有机层)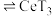 (有机层)
(有机层)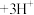 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入 溶液。
溶液。结晶析出:将
 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到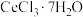 晶体。
晶体。(4)加热脱水:将
 固体和
固体和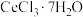 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是(5)对
 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵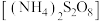 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用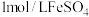 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为
您最近一年使用:0次
2023-08-08更新
|
434次组卷
|
2卷引用:辽宁省丹东市等2地大石桥市第三高级中学等2校2022-2023学年高三上学期1月期末考试化学试题
2023高三·全国·专题练习
3 . 分液的操作方法___________
您最近一年使用:0次
4 . 过滤时洗涤沉淀的方法___________
您最近一年使用:0次
22-23高二下·全国·课时练习
名校
解题方法
5 . 现拟分离乙酸乙酯、乙酸和乙醇的混合物,下图是分离操作步骤流程图。

已知各物质的沸点:乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为_______ ,试剂(b)为_______ 。
(2)图中的分离方法分别是①为_______ ;②为_______ ;③为_______ 。
(3)写出下列有机物的化学式:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 。

已知各物质的沸点:乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为
(2)图中的分离方法分别是①为
(3)写出下列有机物的化学式:A
您最近一年使用:0次
解题方法
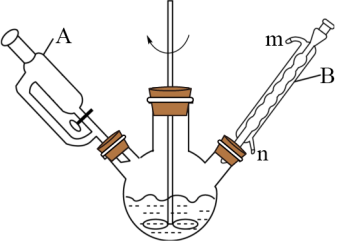
6 . 山梨酸酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。实验室用如图1所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
实验步骤:
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。回答下列问题:
(1)仪器A的名称是_______ ;仪器B的作用是_______ ,冷却水由_______ (填“m”或“n”)口通入。
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是_______ ,若改为加入NaOH的浓溶液,是否可行_______ (填“是”或“否”),原因是:_______ 。
(3)在实验步骤④中加入少量无水MgSO₄的目的是_______
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是_______ 。
(5)本实验中,山梨酸正丁酯的产率是_______ (精确至0.1%)。
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用_______ 。
反应方程式如下: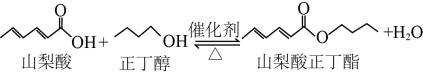
| 物质 | 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.7 | 难溶 |
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。回答下列问题:
(1)仪器A的名称是
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是
(3)在实验步骤④中加入少量无水MgSO₄的目的是
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是
(5)本实验中,山梨酸正丁酯的产率是
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用

您最近一年使用:0次
2023-11-04更新
|
490次组卷
|
2卷引用:云南省大理白族自治州2023-2024学年高三上学期第一次复习统一检测理科综合化学试题
2023高三·全国·专题练习
解题方法
7 . 钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。

“酸浸氧化”需要加热,其原因是_____ 。

“酸浸氧化”需要加热,其原因是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . 某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
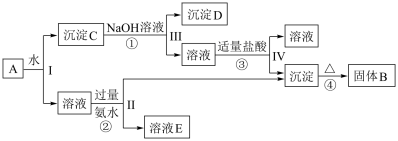
I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是___________ ;获得沉淀后,要对沉淀进行洗涤,请简述洗涤沉淀的操作是___________ 。

I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
您最近一年使用:0次
9 . 高氯酸铵NH4ClO4是复合火箭推进剂的重要成分,实验室可通过下列反应制取。

反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.15,从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)___________ 、___________ 、___________ 、冰水洗涤、干燥。用冰水洗涤的目的是___________ 。


反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.15,从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)

您最近一年使用:0次
名校
解题方法
10 . 氯酸钾为无色或白色晶体,是一种强氧化剂。某化学小组制取氯酸钾并进行有关探究实验。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:
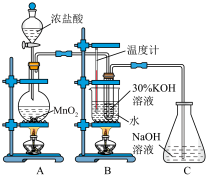
(1)装置A中盛装浓盐酸的仪器名称是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。
(3)氯气和氢氧化钾溶液在加热的条件下可制得氯酸钾,若装置B中加热温度过低,所得主要氧化产物为___________ (填化学式)。已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置B所得溶液中提取氯酸钾晶体的实验操作是蒸发浓缩、___________ 、洗涤、干燥。
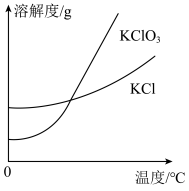
II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3.室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
①3号试管实验中x的值为___________ ;1号试管实验的作用是___________ 。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为___________ 。
③由该系列实验可得出的结论是___________ 。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:

(1)装置A中盛装浓盐酸的仪器名称是
(2)装置A中发生反应的离子方程式为
(3)氯气和氢氧化钾溶液在加热的条件下可制得氯酸钾,若装置B中加热温度过低,所得主要氧化产物为

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3.室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 5.0 | 0 |
| 取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为
③由该系列实验可得出的结论是
您最近一年使用:0次
2023-11-13更新
|
433次组卷
|
2卷引用:广东省汕头市潮阳实验学校2024届高三上学期期中考试化学试题





