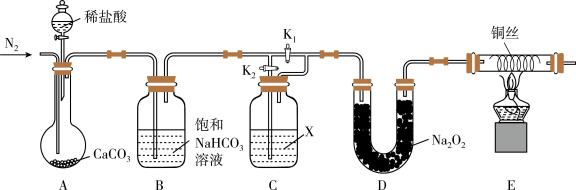
1 . 某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如下装置进行实验(夹持仪器已省略)。
回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是________ 。
(2)饱和NaHCO3溶液的作用是_________ ;试剂X是___________ 。
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是_______ 。
(4)若_____ (填操作),E中灼热的铜丝变为黑色,可证明潮湿的CO2能与Na2O2反应。
(5)写出D中CO2与Na2O2反应的化学方程式___________ 。

回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是
(2)饱和NaHCO3溶液的作用是
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是
(4)若
(5)写出D中CO2与Na2O2反应的化学方程式
您最近一年使用:0次
2 . I.某化学实验小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置(氯气易溶于CCl4,HCl不溶于CCl4)。

请回答下列问题:
(1)装置A中连接橡皮管的目的是_____________________________________ 。
(2)装置A中发生反应的离子方程式为_________________________________ ,装置B中盛放的试剂是___________ 。
(3)装置D与E中出现的不同现象说明的问题是_________________________ 。
(4)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,其目的是___________________________________ 。
Ⅱ.某研究性学习小组欲制备漂白粉,设计在上述装置A后连接如右图所示的组合装置:
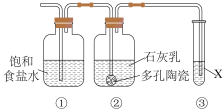
(5)装置②中发生反应的化学方程为___________________________________ 。
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________________________________ 。

请回答下列问题:
(1)装置A中连接橡皮管的目的是
(2)装置A中发生反应的离子方程式为
(3)装置D与E中出现的不同现象说明的问题是
(4)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,其目的是
Ⅱ.某研究性学习小组欲制备漂白粉,设计在上述装置A后连接如右图所示的组合装置:

(5)装置②中发生反应的化学方程为
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是
您最近一年使用:0次
2020-06-04更新
|
434次组卷
|
2卷引用:江西省南昌市八一中学、洪都中学等七校2020-2021学年高一上学期期末联考化学试题
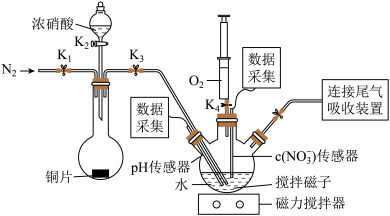
3 . 实验小组为验证NO2与水反应的产物,用如图所示装置进行实验(夹持装置已略去,气密性已检验)。
【实验过程】
步骤II中,传感器记录数据如图所示:

【解释及结论】
(1)NO2与水反应的离子方程式为___ 。
(2)步骤I中,通入N2的目的是___ 。
(3)将步骤II中圆底烧瓶内的实验现象补充完整:___ 。
(4)该实验验证NO2与水反应产物的实验证据包括___ (填序号)。
A.圆底烧瓶中溶液变为蓝绿色
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO3-传感器记录所得数据
(5)有同学认为该实验不严谨,因为也可能导致传感器所记录的数据结果___ 。

【实验过程】
| 实验步骤 | 实验现象 |
| Ⅰ.打开K1、K3、K5,关闭K2、K4,通入一段时间N2,关闭K1 | —— |
| Ⅱ.打开K2,放入足量浓HNO3,同时打开pH传感器和NO3-传感器,记录数据 | 圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色, ;片刻后,三颈瓶内的导管口有气泡冒出 |
| III.5min后,打开K4,用注射器将少量空气注入三颈瓶,关闭K4 | 三颈瓶内的气体从无色变为浅红棕色 |
步骤II中,传感器记录数据如图所示:

【解释及结论】
(1)NO2与水反应的离子方程式为
(2)步骤I中,通入N2的目的是
(3)将步骤II中圆底烧瓶内的实验现象补充完整:
(4)该实验验证NO2与水反应产物的实验证据包括
A.圆底烧瓶中溶液变为蓝绿色
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO3-传感器记录所得数据
(5)有同学认为该实验不严谨,因为也可能导致传感器所记录的数据结果
您最近一年使用:0次
2020-06-02更新
|
222次组卷
|
2卷引用:北京市海淀区首师大附属育新学校中部2019-2020学年高一下学期期末考试化学试题
名校
解题方法
4 . 下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。下列说法错误的是
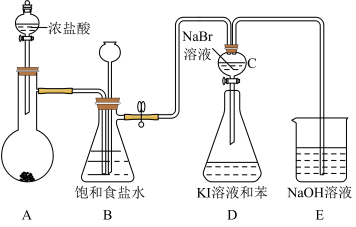
| A.装置A烧瓶内的试剂可以是KMnO4 |
| B.装置B具有除杂和贮存气体的作用 |
| C.实验结束后,振荡D会观察到液体分层且下层呈紫红色 |
| D.利用该装置能证明氯、溴、碘的非金属性逐渐减弱 |
您最近一年使用:0次
2020-05-28更新
|
527次组卷
|
7卷引用:河北省廊坊市第一中学2022~2023 学年高一上学期期末考试化学试题
解题方法
5 . 氯化亚铜(CuCl) 为白色粉末,其露置于空气中易被氧化为绿色的碱式氯化铜Cu2(OH)3Cl]。某兴趣小组高温加热分解氯化铜晶体(CuCl2·xH 2O)制备CuCl,其装置如下(加热仪器、夹持仪器省略)

回答下列问题:
(1)装有无水硫酸铜的仪器名称为______ ,装置 D 的作用是______ 。
(2)通入 HCl 气体的主要作用是______ 。
(3)实验过程中,装置C 中的现象为______ 。
(4)硬质玻璃管A 中发生主要反应的化学方程式为__________ 。
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=______ (精确到 0.1)。
②若加热时有固体溅出坩埚,则测得x 值______ 填“偏大”“不变”或“偏小”)。

回答下列问题:
(1)装有无水硫酸铜的仪器名称为
(2)通入 HCl 气体的主要作用是
(3)实验过程中,装置C 中的现象为
(4)硬质玻璃管A 中发生主要反应的化学方程式为
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=
②若加热时有固体溅出坩埚,则测得x 值
您最近一年使用:0次
2020-05-25更新
|
132次组卷
|
3卷引用:贵州省黔西南州兴义市义龙新区2021-2022高三上学期期末考试化学试题
名校
解题方法
6 . 为探究铁和硫反应产物中铁的化合价,某同学设计了如下所示的实验过程:

已知:①铁和硫反应产物不溶于碱,能溶于硫酸
②硫可溶于热碱溶液,发生类似于 Cl2和 NaOH 溶液的化学反应下列说法不正确的是

已知:①铁和硫反应产物不溶于碱,能溶于硫酸
②硫可溶于热碱溶液,发生类似于 Cl2和 NaOH 溶液的化学反应下列说法不正确的是
| A.混合粉末应在 N2 氛围中进行加热,所用 H2SO4溶液应先煮沸 |
| B.取溶液 A,滴加 KSCN 溶液,未出现红色,可证明铁和硫反应只有+2 价铁生成 |
| C.滤渣用稀 H2SO4 溶解时应在通风橱中进行 |
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH- 2S2-+SO32-+3H2O 2S2-+SO32-+3H2O |
您最近一年使用:0次
2020-05-21更新
|
177次组卷
|
2卷引用:河南省兰考县第一高级中学2021-2022学年高一上学期期末考试化学试题
7 . 用如图所示装置进行下列实验,所选的药品、现象和结论正确的一组是( )
| 选项 | a | b | c | 现象 | 结论 | 装置 |
| A | 稀盐酸 | 大理石 | Na2SiO3溶液 | c中有白色胶状沉淀生成 | H2CO3酸性大于H2SiO3 | 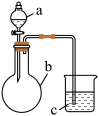 |
| B | 浓盐酸 | MnO2 | 石蕊试液 | 石蕊试液先变红后褪色 | 氯气具有漂白性 | |
| C | 稀硫酸 | 锌粒 | 水 | 一段时间有气泡 | 反应生成了H2 | |
| D | NaOH溶液 | Al | 水 | 产生大量气泡 | Al能与NaOH溶液反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-19更新
|
114次组卷
|
2卷引用:江西省吉安市泰和县第二中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 某学习小组为验证浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,设计如图装置进行实验(夹持仪器已略去)。【查阅资料】:NO与NaOH溶液不反应,NO2与NaOH溶液能反应(反应的化学方程式为2NO2+2NaOH=NaNO3+NaNO2+H2O)。
备选药品:浓硝酸、3mol·L-1稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。回答下列问题。
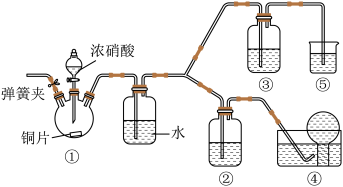
(1)连接好装置,滴加浓硝酸之前的操作依次是:____________ ,加入药品,打开装置①中的弹簧夹后通入CO2一段时间,关闭弹簧夹,将装置④中导管末端伸入倒置的烧瓶内。通入CO2的目的是____________ 。
(2)若用质量分数为70%浓硝酸(密度为1.42g·cm-3)配制250mL3mol·L-1的稀硝酸,除量筒、烧杯、胶头滴管外,还要用到的玻璃仪器有____________ 、____________ 。
(3)装置①中发生反应的化学方程式为____________ 。
(4)装置①中产生的气体通过盛有水的洗气瓶时发生反应的化学方程式为____________ 。
(5)根据实验设计,装置②中盛放的试剂是____________ 。
(6)做实验时应避免有害气体排放到空气中,装置⑤中盛放的药品是____________ 。
(7)验证浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO的实验现象是____________ 。
备选药品:浓硝酸、3mol·L-1稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。回答下列问题。

(1)连接好装置,滴加浓硝酸之前的操作依次是:
(2)若用质量分数为70%浓硝酸(密度为1.42g·cm-3)配制250mL3mol·L-1的稀硝酸,除量筒、烧杯、胶头滴管外,还要用到的玻璃仪器有
(3)装置①中发生反应的化学方程式为
(4)装置①中产生的气体通过盛有水的洗气瓶时发生反应的化学方程式为
(5)根据实验设计,装置②中盛放的试剂是
(6)做实验时应避免有害气体排放到空气中,装置⑤中盛放的药品是
(7)验证浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO的实验现象是
您最近一年使用:0次
2020-05-16更新
|
378次组卷
|
3卷引用:福建省宁德市2019-2020学年高一上学期期末考试化学试题
9 . 化学小组为探究 在酸性
在酸性 溶液中的反应,利用如图装置进行实验:
溶液中的反应,利用如图装置进行实验:
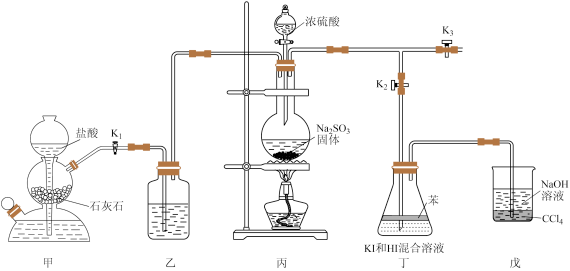
I.排出装置内的空气。减缓 的流速,向丁装置中通入
的流速,向丁装置中通入 和
和 的混合气体。
的混合气体。
Ⅱ.一段时间后,溶液变黄并出现浑浊。摇动锥形瓶、静置,苯与溶液边缘呈紫红色。
Ⅲ.持续向丁装置中通入 和
和 混合气体,溶液变为无色。
混合气体,溶液变为无色。
Ⅳ.再静置一段时间,取锥形瓶中水溶液,滴加 溶液,产生白色沉淀。
溶液,产生白色沉淀。
回答下列问题:
(1)苯的作用为__________ 。排出装置内空气的具体操作为_________ 。
(2)向装置丁中缓慢通入 的作用是
的作用是__________ 。
(3)步骤Ⅱ反应的离子方程式为__________ ;步骤Ⅲ反应的离子方程式为______________ 。
(4)实验的总反应为_________ , 和
和 在反应中的作用为
在反应中的作用为___________ 。
 在酸性
在酸性 溶液中的反应,利用如图装置进行实验:
溶液中的反应,利用如图装置进行实验:
I.排出装置内的空气。减缓
 的流速,向丁装置中通入
的流速,向丁装置中通入 和
和 的混合气体。
的混合气体。Ⅱ.一段时间后,溶液变黄并出现浑浊。摇动锥形瓶、静置,苯与溶液边缘呈紫红色。
Ⅲ.持续向丁装置中通入
 和
和 混合气体,溶液变为无色。
混合气体,溶液变为无色。Ⅳ.再静置一段时间,取锥形瓶中水溶液,滴加
 溶液,产生白色沉淀。
溶液,产生白色沉淀。回答下列问题:
(1)苯的作用为
(2)向装置丁中缓慢通入
 的作用是
的作用是(3)步骤Ⅱ反应的离子方程式为
(4)实验的总反应为
 和
和 在反应中的作用为
在反应中的作用为
您最近一年使用:0次
2020-05-12更新
|
1170次组卷
|
8卷引用:湖南省邵阳市新邵县2019-2020学年高二下学期期末考试化学试题
湖南省邵阳市新邵县2019-2020学年高二下学期期末考试化学试题山东省烟台市中英文学校2021届高三上学期期末考试化学试题山东省青岛市2020届高三4月统一质量检测(一模)化学试题湖北省2020年荆、荆、襄、宜四地七校考试联盟高一联考化学模拟试题(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练湖南省湖南师范大学附属中学2020-2021学年高二上学期入学考试化学试题(已下线)第9周 晚练题-备战2022年高考化学周测与晚练(新高考专用)安徽省滁州市定远县育才学校2022届高三上学期第一次月考化学试题
解题方法
10 . 某小组探究酸化条件对0.1mol/LKI溶液氧化反应的影响。
(1)溶液变蓝,说明溶液中含有____________ 。结合实验1和实验2,该小组同学认为酸化能够加快I-氧化反应的速率。
(2)同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:_________________________________________________________ 。
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是_____________________________________________________________________________________ 。
(3)同学甲进一步设计实验验证分析的合理性。
(4)该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
从实验5可以看出pH越大,歧化反应速率越_______________ (填“快”或“慢”)。
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:_________________________ 。
| 序号 | 操作及现象 |
| 实验1 | 取放置一段时间后依然无色的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液立即变蓝 |
| 实验2 | 取新制的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液10s后微弱变蓝 |
(1)溶液变蓝,说明溶液中含有
(2)同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
| 时间 | 5分钟 | 1天 | 3天 | 10天 |
| pH | 7.2 | 7.4 | 7.8 | 8.7 |
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是
(3)同学甲进一步设计实验验证分析的合理性。
| 序号 | 操作 | 现象 |
| 实验4 | 重复实验2操作后,继续向溶液中加入 | 溶液立即变蓝 |
(4)该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
| 实验组 | A | B | C | D |
| pH | 11.4 | 10.6 | 9.5 | 8.4 |
| 现象 | 无颜色变化 | 产生蓝色后瞬间消失 | 产生蓝色,30s后蓝色消失 | |
从实验5可以看出pH越大,歧化反应速率越
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:
您最近一年使用:0次
2020-05-11更新
|
317次组卷
|
4卷引用:北京市北京交通大学附属中学2020-2021学年高二上学期期末练习化学试题
北京市北京交通大学附属中学2020-2021学年高二上学期期末练习化学试题天津市河北区2021-2022学年高三上学期期末考试化学试题北京市丰台区2020届高三第一次模拟考试化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究



