17. 含碳化合物对环境、生产和人类生命活动具有很大影响。回答下列问题:
(1)治理汽车尾气污染对保护环境至关重要。
①汽车尾气中含有大量CO和NO等大气污染物,反应为:2NO(g) +2C0(g)

N
2(g) +2CO
2(g),其他条件不变时,NO平衡转化率随温度变化的曲线如下图:
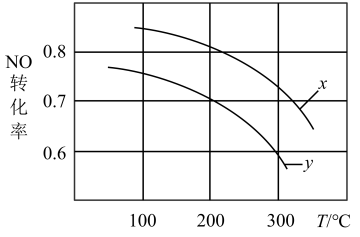
由图象知:∆H
_________0(填“>"或“<");图中曲线x变为y时,对压强的改变为
______(填“加压"或“减压")。
②在催化剂存在时,也可用CH
4还原氮氧化合物使其生成无毒气体,改善汽车尾气对环境的影响。

对于反应a加入催化剂,可使Eal
_____(填“ 增大”“减小”或“不变”);相同条件下,反应b比反应a
_____ ( 填“易”或“难" )发生,理由是
________________;反应CH
4(g) +2NO
2(g)=N
2(g)+2H
2O(g) +CO
2(g) ∆H=
______kJ·mol
-1(用含∆H
1、∆H
2的代数表示)。
(2)碳资源化处理对于缓解能源危机有重要意义。对于反应:CO(g) +2H
2(g)→CH
3OH ∆H<0,在催化剂作用下,分别在T
1°C和T
2°C时(T
1 >T
2),向容积为2 L的密闭容器内加入4mol的CO和8molH
2,随反应进行CH
3OH的物质的量的变化情况如下图:

①比较ab点反应速率大小:v
a _____v
b,(填“大于”“小于”或“等于”)。
②T
2时,前4 min内用H
2表示的反应速率v(H
2)为
_____,T
1时,反应的化学平衡常数K=
__________。
③已知:反应速率v=v
正-v
逆= k
正x(CO)x
2(H
2) -k
逆x(CH
3OH),k
正和k
逆分别为正、逆反应速率常数,x为物质的量分数,计算a点v正:v逆=
_______( 保留两位有效数字)。
④若容器容积不变,下列措施可增加甲醇产率的是
______(填字母标号)。
A.按相同比例再向容器中充人原料气体
B. 将生成的CH
3OH从体系中分离
C.选用高效催化剂
D.充入He,使体系的总压增大