河北省石家庄市第一中学2019-2020学年高一下学期3月月考化学试题.
河北
高一
阶段练习
2021-05-07
377次
整体难度:
适中
考查范围:
化学与STSE、物质结构与性质、化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B.我国城市环境中的大气污染物主要是SO2、CO2、NO2、粉尘等 |
| C.利用太阳能在催化剂参与下分解水制氢气是把光能转化为化学能的绿色化学方法 |
| D.石油、煤、天然气、可燃冰、花生油都属于化石燃料 |
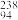 Pu作为热源材料,下列关于
Pu作为热源材料,下列关于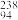 Pu的说法正确的是
Pu的说法正确的是A.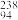 Pu与 Pu与 U互为同位素 U互为同位素 |
B.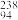 Pu与 Pu与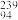 Pu具有相同的最外层电子数 Pu具有相同的最外层电子数 |
C.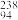 Pu与 Pu与 U互为同素异形体 U互为同素异形体 |
D.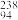 Pu与 Pu与 U具有完全相同的化学性质 U具有完全相同的化学性质 |
| A.反应物能量总和大于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(g)ΔH=-131.4kJ/mol |
| C.水煤气反应中生成1molH2(g)放出131.4kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4kJ热量 |
【知识点】 能量的相互转化 焓变 反应焓变与热化学方程式的关系解读
| A.离子化合物可能含共价键 | B.共价化合物不可能含离子键 |
| C.离子化合物中只含离子键 | D.共价化合物中只含共价键 |
【知识点】 化学键与物质类别关系的判断解读
A.氨气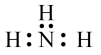 | B.四氯化碳 |
C.氮气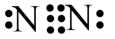 | D.二氧化碳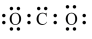 |
【知识点】 有关粒子结构的化学用语 共价型分子结构式、电子式解读
| A.(A-x+m) mol |
| B.(A-x-m) mol |
C. (A-x+m) mol (A-x+m) mol |
D. (A-x-m) mol (A-x-m) mol |
②稀溶液中,H+(aq)+OH-(aq)=H2O(1)ΔH=-57.3kJ·mol-1。
下列结论正确的是
| A.碳的燃烧热ΔH<-110.5kJ·mol-1 |
| B.反应①的反应热为221kJ·mol-1 |
| C.98%的浓硫酸与稀氢氧化钠溶液反应生成1mol水的中和热为-57.3kJ·mol-l |
| D.稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
A.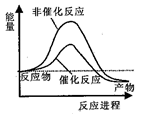 | B.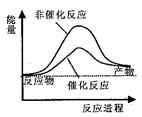 |
C.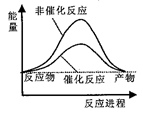 | D.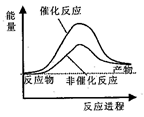 |
【知识点】 化学反应中能量变化的原因 碰撞理论及活化能解读
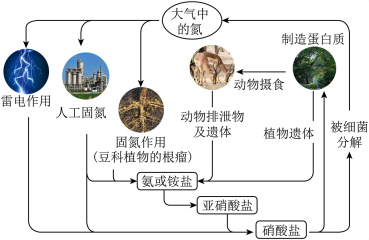
| A.氮元素均被氧化 |
| B.工业合成氨属于人工固氮 |
| C.含氮无机物和含氮有机物可相互转化 |
| D.碳、氢、氧三种元素也参与了氮循环 |
①参加反应的物质的性质是影响化学反应速率的主要因素
②光是影响某些化学反应速率的外界条件之一
③决定化学反应速率的主要因素是浓度
④不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率
| A.①② | B.①②④ | C.③④ | D.①④ |
①FeCl2 ②H2SO4 ③NH4Cl ④HCl ⑤Fe(OH)3 ⑥FeCl3
| A.只有①②③⑥ | B.只有②③⑤⑥ |
| C.只有①③④ | D.全部 |
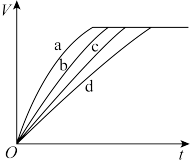
| 组别 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
| A.第4组实验的反应速率最慢 |
| B.第1组实验中盐酸的浓度大于2.5mol·L-1 |
| C.第2组实验中盐酸的浓度等于2.5mol·L-1 |
| D.第3组实验的反应温度低于30℃ |
| A.物质发生化学变化都伴有能量的变化 |
| B.吸热反应在任何条件都不能发生 |
| C.伴有能量变化的物质变化都是化学变化 |
| D.需要加热的反应一定不是放热反应 |
【知识点】 化学反应中能量变化的原因 能量的相互转化 吸热反应和放热反应解读
 NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) H2(g)+I2(g),当达到化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是
H2(g)+I2(g),当达到化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是| A.8:8:1 | B.10:8:1 | C.2:2:1 | D.3:2:1 |
【知识点】 化学平衡的有关计算

| A.等浓度C的氢化物水溶液酸性比E的氢化物水溶液酸性强 |
B.A与B形成的微粒可能有:AB 、AB2 、AB2 |
| C.D在过量的B单质中燃烧产物为DB2 |
| D.C、B、A的氢化物稳定性依次减小 |
 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是①相同时间内,氧气的生成速率为n mol
 ·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1
·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
| A.①③⑤⑥ | B.②③⑤ |
| C.①③④ | D.①②③④⑤⑥ |
【知识点】 化学平衡状态的判断方法解读
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )| A.v(C)=0.2 mol·L-1·s-1 | B.z=3 | C.B的转化率为25% | D.C的体积分数为28.6% |
【知识点】 化学平衡的有关计算
| A.HF、HCl、HBr、HI的酸性逐渐增强,说明F、Cl、Br、I的非金属性逐渐增强 |
| B.元素R最高正价为+7价,表明R元素属于VIIA族元素 |
| C.若M+和R2-具有相同的电子层结构,则原子半径:M<R |
| D.从元素在周期表中的位置可以推断,硅和锗都可用作半导体材料 |
| A.赤铁矿的主要成分是Fe3O4 |
| B.铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
| C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤 |
| D.Fe3+与KSCN反应产生血红色沉淀 |
①SiO2→Na2SiO3②CuSO4→CuCl2③SiO2→H2SiO3④CuO→Cu(OH)2⑤Na2O2→NaOH
| A.①② | B.③④ | C.②③④ | D.③④⑤ |
| A.560mL | B.448mL | C.896mL | D.672mL |
| A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物充分加热,减重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
【知识点】 碳酸钠、碳酸氢钠混合物的有关求算解读

| A.若甲为单质铁,则丙一定为FeCl3 |
| B.若甲为强碱,则X一定为CO2 |
| C.若乙是一种白色胶状沉淀,则甲溶液中一定含有Al3+ |
| D.若甲为单质,则此关系中涉及的反应一定都是氧化还原反应 |
【知识点】 氧化还原反应方程式的配平解读 铝三角转化解读 铁的其他化合物
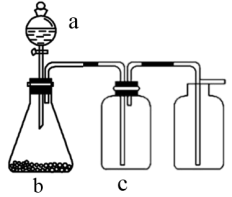
| 选项 | 气体 | a | b | c |
| A | SO2 | 浓硫酸 | Na2SO3 | 浓硫酸 |
| B | H2 | 稀硫酸 | 锌片 | 浓硫酸 |
| C | CO2 | 稀盐酸 | 石灰石 | NaOH溶液 |
| D | NO | 稀硝酸 | 铜粉 | 碱石灰 |
| A.A | B.B | C.C | D.D |
| A.2.24g | B.3.36g | C.5.60g | D.10.08g |
【知识点】 铁及铁的氧化物混合物反应的相关计算解读
| 选项 | 叙述I | 叙述II |
| A | 浓硝酸和稀硝酸都具有强氧化性 | 浓硝酸和稀硝酸常温下都可与单质碳反应 |
| B | 浓硫酸具有强氧化性和吸水性 | 浓硫酸可干燥H2和CO,不可干燥H2S |
| C | SO2是酸性氧化物 | SO2可使品红溶液褪色 |
| D | 铵盐受热易分解 | NH4Cl和NH4HCO3均可用作氮肥和制取氨气 |
| A.A | B.B | C.C | D.D |
| A.H2O很稳定是因为水分子之间存在氢键 |
| B.NaCl固体熔化时破坏离子键,干冰熔化时破坏共价键 |
| C.卤素单质从上到下熔沸点升高是因为它们的组成和结构相似,从上到下其摩尔质量增大,分子间的范德华力增大 |
| D.液氨常用作制冷剂是因为NH3极易溶解于水 |
 、Fe2+、K+、I-、SO
、Fe2+、K+、I-、SO 、SO
、SO ,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知还原性:SO
,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知还原性:SO >I->Fe2+)
>I->Fe2+)| A.肯定不含I- | B.肯定含有SO |
C.肯定含有SO | D.肯定含有NH |
| 实验 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 | ||
| 体积/mL | 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | /mL | ||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
| A.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响 |
| B.实验①和③溶液变浑浊(产生等量的沉淀)的时间相同 |
| C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤ |
| D.实验④和⑤溶液变浑浊(产生等量的沉淀)的时间⑤>④ |
二、解答题 添加题型下试题

(1)推断A、B、C、D的化学式:A
(2)写出①②变化的离子方程式:
①
②
(3)写出实验室制取气体B的反应原理
【知识点】 无机综合推断 氨与氯化氢反应的实验解读 氨气的实验室制法解读

(1) A试管中发生反应的化学方程式为
(2) 反应一段时间后,可观察到B试管中的现象为
(3) C试管口浸有NaOH溶液的棉团作用是
(4) 如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是
(5) 实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是
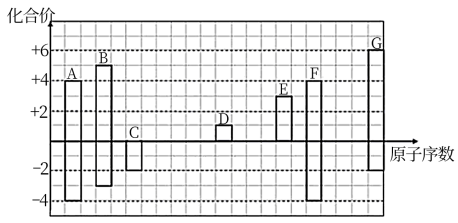
(1)元素A在周期表中的位置
(2)写出D2C2的电子式
(3)C2-、D+、G2-离子半径大小顺序是___________>___________>___________(用离子符号回答)
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
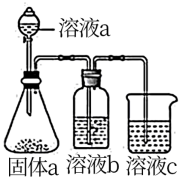
①溶液a和b分别为
②溶液c中的离子方程式为
③下列事实或解释能说明非金属性B>A的是
甲.原子半径B<A,最外层电子数B>A,核对最外层电子的束缚力B>A
乙.B的氢化物分子间有氢键,而A的氢化物分子间没有
丙.B的单质是双原子分子,常温下是气态,而A的单质常温下为固态
丁.元素的氧化物的水化物的酸性B弱于A
(1)实验测得:5g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5kJ的热量。试写出甲醇燃烧热的热化学方程式:
(2)合成甲醇的主要反应是2H2(g)+CO(g)
 CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:| 物质 | H2 | CO | CH3OH |
| 浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
(3)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)
 2NH3(g)
2NH3(g)①若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=
②反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为
③达到平衡时,N2和H2的转化率之比α(N2):α(H2)=
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 化石能源 太阳能的利用 生物质能的利用 | |
| 2 | 0.85 | 原子的构成 元素、核素、同位素 几组常见同素异形体 | |
| 3 | 0.65 | 能量的相互转化 焓变 反应焓变与热化学方程式的关系 | |
| 4 | 0.65 | 化学键与物质类别关系的判断 | |
| 5 | 0.65 | 有关粒子结构的化学用语 共价型分子结构式、电子式 | |
| 6 | 0.65 | 根据n=m/M的相关计算 原子中相关数值及其之间的相互关系 | |
| 7 | 0.85 | 中和热概念 燃烧热概念 反应热大小比较 | |
| 8 | 0.85 | 化学反应中能量变化的原因 碰撞理论及活化能 | |
| 9 | 0.65 | 氧化还原反应定义、本质及特征 氮元素的存在及用途 自然界氮的固定 | |
| 10 | 0.65 | 影响化学反应速率的因素 影响化学反应速率的内因 影响化学反应速率的外因 | |
| 11 | 0.85 | 氨的碱性 三氧化硫 铁与非金属单质反应 氢氧化亚铁的还原性 | |
| 12 | 0.65 | 影响化学反应速率的外因 外因对化学反应速率影响的综合分析 | |
| 13 | 0.85 | 化学反应中能量变化的原因 能量的相互转化 吸热反应和放热反应 | |
| 14 | 0.65 | 化学平衡的有关计算 | |
| 15 | 0.65 | 元素周期律、元素周期表的推断 同周期元素性质递变规律理解及应用 根据原子结构进行元素种类推断 “位构性”关系理解及应用 | |
| 16 | 0.65 | 化学平衡状态的判断方法 | |
| 17 | 0.85 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 18 | 0.65 | 化学平衡的有关计算 | |
| 19 | 0.85 | 同主族元素性质递变规律 元素周期律的应用 同主族元素性质递变规律理解及应用 | |
| 20 | 0.65 | 铁与水蒸气的反应 几种铁的氧化物的物理性质及用途 Fe3+的检验 铁盐、亚铁盐相互除杂 | |
| 21 | 0.65 | 物质的转化 二氧化硅的化学性质 过氧化钠与水的反应 硫酸铜 | |
| 22 | 0.65 | 硝酸的强氧化性 有关酸性环境下硝酸根氧化性的有关计算 | |
| 23 | 0.65 | 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 24 | 0.65 | 氧化还原反应方程式的配平 铝三角转化 铁的其他化合物 | |
| 25 | 0.85 | 一氧化氮的化学性质 二氧化硫的化学性质 二氧化硫的制备 常见气体的制备与收集 | |
| 26 | 0.4 | 铁及铁的氧化物混合物反应的相关计算 | |
| 27 | 0.65 | 硝酸的强氧化性 铵盐的不稳定性 二氧化硫的漂白性 浓硫酸的强氧化性 | |
| 28 | 0.65 | 分子间作用力 氢键 范德华力对物质性质的影响 化学键与分子间作用力 | |
| 29 | 0.65 | 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 离子的检验 | |
| 30 | 0.65 | 影响化学反应速率的因素 浓度对化学反应速率的影响 温度对化学反应速率的影响 | |
| 二、解答题 | |||
| 31 | 0.85 | 无机综合推断 氨与氯化氢反应的实验 氨气的实验室制法 | 无机推断题 |
| 32 | 0.65 | 二氧化硫的化学性质 二氧化硫的制备 物质性质的探究 综合实验设计与评价 | 实验探究题 |
| 33 | 0.65 | 元素周期律、元素周期表的推断 根据物质性质进行元素种类推断 “定位法”在推断中的应用 “位构性”关系理解及应用 | 无机推断题 |
| 34 | 0.65 | 表示燃烧热的热化学方程式书写 化学反应速率计算 转化率的相关计算及判断 | 原理综合题 |



