17. 氨在国民经济中占有重要的地位,十九世纪初人们就开始致力于研究工业合成氨。合成氨生产包括造气、净化、合成三个步骤。
(1)已知:①CH
4(g)+CO
2(g)

2CO(g)+2H
2(g) △H
1=+247.4kJ/mol
②CH
4(g)+2H
2O(g)

CO
2(g)+4H
2(g) △H
2=+165kJ/mol
则CH
4和水蒸气在高温下反应生成CO和氢气的热化学反应方程式为
___________。
(2)某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中测得如表所示数据。请回答下列问题:
| 时间/min | CH4/mol | H2O/mol | CO/mol | H2/mol |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
①分析表中数据,判断5min时反应是否处于平衡状态
___________(填“是”或“否”);前5min反应的平均反应速率v(CH
4)=
___________。
②反应在7~10min内,CO的物质的量减少的原因可能是
___________(填字母)。
A.减小压强
B.降低温度
C.升高温度
D.充入H
2(3)在密闭反应器中按n(N
2):n(H
2)=1:3投料后,在200℃、400℃、600℃下,当反应N
2(g)+3H
2(g)

2NH
3(g) △H=﹣92.4kJ/mol达到平衡时,混合物中NH
3的物质的量分数随压强的变化曲线如图所示。
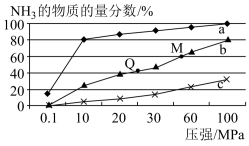
①曲线a对应的温度是
___________。
②M点对应的H
2的转化率是
___________。