名校
1 . 柳州水质连夺全国第一,下列做法有利于保护水资源的是
| A.大量开采使用地下水 | B.生活污水直接排放 |
| C.生活中节约用水 | D.工业废水任意排放 |
您最近一年使用:0次
名校
2 . 下列说法错误的是
| A.中国空间站使用的碳纤维,是一种新型无机非金属材料 |
| B.O2和O3互为同位素 |
| C.正丁烷的沸点比异丁烷的沸点高 |
D.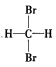 和 和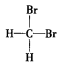 结构一样 结构一样 |
您最近一年使用:0次
解题方法
3 . 某化学小组对碳酸氢钠和碳酸钠的制备与性质产生兴趣,他们了解到下列化学史及相关信息:
 .我国化学家侯德榜在吕布兰法和索尔维法的基础上创立了先进的侯氏制碱法,基本消除废弃物的排放,同时生产NaHCO3和NH4Cl。
.我国化学家侯德榜在吕布兰法和索尔维法的基础上创立了先进的侯氏制碱法,基本消除废弃物的排放,同时生产NaHCO3和NH4Cl。
(1)请写出碳酸氢钠的一种用途:___________ 。
 .索尔维法的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl、2NaHCO3
.索尔维法的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl、2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
 .氨气(NH3)是一种有刺激性气味、极易溶于水的碱性气体。
.氨气(NH3)是一种有刺激性气味、极易溶于水的碱性气体。
 .Na2CO3与HCl的反应分步进行,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl
.Na2CO3与HCl的反应分步进行,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl
【实验目的】利用下图所示装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
步骤1:关闭K1,打开K2使氨气进入装置C,调节气流速率,等装置C中气流平衡后,打开K1通入CO2。
步骤2:待装置C的锥形瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2。
步骤3:将锥形瓶内反应后的混合物过滤、洗涤、低温干燥,即得碳酸氢钠固体。
步骤4:将所得碳酸氢钠固体加热制取碳酸钠。
【表达交流】
(2)装置B中饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为___________ 。
(3)装置C锥形瓶上连接的长颈漏斗的作用是___________ (填序号)。
A.用于添加饱和食盐水 B.平衡气压 C.冷凝回流CO2
(4)步骤2中关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是___________ 。
(5)步骤3中“低温干燥”的原因是___________ 。
【反思评价】
(6)有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是___________ 。
【延伸拓展】
(7)该小组继续探究碳酸钠的性质,向碳酸钠溶液中逐滴加入足量的稀盐酸,观察到:___________ 。
 .我国化学家侯德榜在吕布兰法和索尔维法的基础上创立了先进的侯氏制碱法,基本消除废弃物的排放,同时生产NaHCO3和NH4Cl。
.我国化学家侯德榜在吕布兰法和索尔维法的基础上创立了先进的侯氏制碱法,基本消除废弃物的排放,同时生产NaHCO3和NH4Cl。(1)请写出碳酸氢钠的一种用途:
 .索尔维法的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl、2NaHCO3
.索尔维法的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl、2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O .氨气(NH3)是一种有刺激性气味、极易溶于水的碱性气体。
.氨气(NH3)是一种有刺激性气味、极易溶于水的碱性气体。 .Na2CO3与HCl的反应分步进行,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl
.Na2CO3与HCl的反应分步进行,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl【实验目的】利用下图所示装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
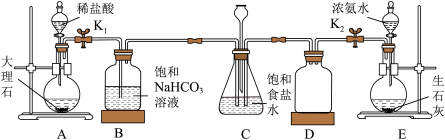
步骤1:关闭K1,打开K2使氨气进入装置C,调节气流速率,等装置C中气流平衡后,打开K1通入CO2。
步骤2:待装置C的锥形瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2。
步骤3:将锥形瓶内反应后的混合物过滤、洗涤、低温干燥,即得碳酸氢钠固体。
步骤4:将所得碳酸氢钠固体加热制取碳酸钠。
【表达交流】
(2)装置B中饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为
(3)装置C锥形瓶上连接的长颈漏斗的作用是
A.用于添加饱和食盐水 B.平衡气压 C.冷凝回流CO2
(4)步骤2中关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是
(5)步骤3中“低温干燥”的原因是
【反思评价】
(6)有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是
【延伸拓展】
(7)该小组继续探究碳酸钠的性质,向碳酸钠溶液中逐滴加入足量的稀盐酸,观察到:
您最近一年使用:0次
解题方法
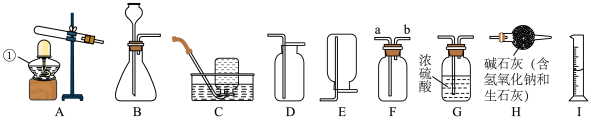
4 . 下图是实验室常用气体制备装直,据图回答问题:___________ 。用A装置制取氧气的化学方程式是___________ 。选择C装置收集氧气是因为___________ 。集满氧气的集气瓶应___________ (填“正”或“倒”)放在桌面上。
(2)用装置F和装置___________ (填序号)收集并测量O2体积, 实验时气体应从装满水的装置F中的导管___________ (填“a”或“b”)端通入。
(3)实验室常用加热氯化铵和熟石灰固体混合物制取极易溶于水的氨气(NH3)。若要制取并收集干燥的氨气,正确的装置连接顺序是___________ (填字母代号)。
(2)用装置F和装置
(3)实验室常用加热氯化铵和熟石灰固体混合物制取极易溶于水的氨气(NH3)。若要制取并收集干燥的氨气,正确的装置连接顺序是
您最近一年使用:0次
5 . 用“84”消毒液消毒时发生的一个化学反应为:2NaClO+CO2+X=Na2CO3+2HClO,则X的化学式为
| A.O2 | B.H2O | C.H2O2 | D.HCl |
您最近一年使用:0次
6 . 常温下,向盛有100.0 g KOH溶液的烧杯中逐滴加入120.0 g 质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如下:
(1)恰好完全反应时,消耗稀盐酸的质量为___________ g。
(2)求该KOH溶液中溶质的质量分数为___________ (结果精确到0.1%)。
| 加入稀盐酸的质量/g | 60.0 | 80.0 | 100.0 | 120.0 |
| 烧杯中溶液的pH | 13.7 | 13.3 | 7.0 | 0.7 |
(2)求该KOH溶液中溶质的质量分数为
您最近一年使用:0次
解题方法
7 . 碳酸钡是一种重要的化工产品。某厂用含二氧化硅杂质的碳酸钡原料生产碳酸钡产品,采用了以下的工艺流程:___________ ;加入过量的盐酸的目的是___________ 。
(2)向氯化钡溶液中加入过量的氢氧化钾并通入二氧化碳,其中能生成碳酸钡的化学方程式是___________ 。
(3)溶液A中溶质的成分,可能的组合有___________ 。
(4)操作3包括的两个操作是___________ 。

(2)向氯化钡溶液中加入过量的氢氧化钾并通入二氧化碳,其中能生成碳酸钡的化学方程式是
(3)溶液A中溶质的成分,可能的组合有
(4)操作3包括的两个操作是
您最近一年使用:0次
解题方法
8 . 填写实验报告。
【实验目的】探究铜、铝、银的金属活动性顺序。
【实验过程】
【实验结论】铜、铝、银的金属活动性顺序由强到弱为___________ 。
【实验目的】探究铜、铝、银的金属活动性顺序。
【实验过程】
| 实验内容 | 实验现象 | 解释或化学方程式 |
| (1)将一根用砂纸打磨干净的铝线浸入硫酸铜溶液中。 | 铝线表面有 | 用砂纸打磨铝线的目的是 |
| (2)将一根用砂纸打磨干净的铜线浸入 | 铜线表面有银白色物质生成,溶液由无色变成蓝色。 | 化学方程式: |
您最近一年使用:0次
解题方法
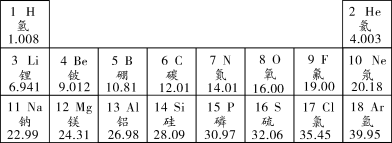
9 . 下N是元素的信息,和国所给信息按要求填空。___________ ,它属于___________ (填“金属”或“非金属”)元素。
(2)写出8号元素的离子符号___________ 。
(3)写出由五个原子构成且含有10个质子的分子的物质___________ (写名称)。
(4)由原子序数为8、11、16三种元素组成的盐是___________ (写化学式)。
(2)写出8号元素的离子符号
(3)写出由五个原子构成且含有10个质子的分子的物质
(4)由原子序数为8、11、16三种元素组成的盐是
您最近一年使用:0次
解题方法
10 . 水和溶液在生产、生活中有着重要的作用。
(1)生活中常用___________ 的方法降低水的硬度。
(2)下列物质在水中不能形成溶液的是___________(填序号)。
(3)甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。___________ 。
②t1℃时,分别向100 g水中加入20 g甲和20 g乙,能形成饱和溶液的是___________ 。
③下列有关叙述正确的是___________ (填序号)。
A. t2℃时,甲的饱和溶液中溶质的质量分数为50%
B. 分别将甲和乙的饱和溶液从t2℃降到t1℃时,析出固体的质量为甲>乙
C. 从接近饱和的甲溶液中析出一定量的甲晶体后,剩余溶液的溶质质量分数变小
D. t2℃时,分别将50 g甲、乙、丙固体溶于水,配成饱和溶液,需要水的质量为甲<乙<丙
(1)生活中常用
(2)下列物质在水中不能形成溶液的是___________(填序号)。
| A.白糖 | B.汽油 | C.食盐 | D.高锰酸钾 |
(3)甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。
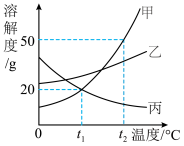
②t1℃时,分别向100 g水中加入20 g甲和20 g乙,能形成饱和溶液的是
③下列有关叙述正确的是
A. t2℃时,甲的饱和溶液中溶质的质量分数为50%
B. 分别将甲和乙的饱和溶液从t2℃降到t1℃时,析出固体的质量为甲>乙
C. 从接近饱和的甲溶液中析出一定量的甲晶体后,剩余溶液的溶质质量分数变小
D. t2℃时,分别将50 g甲、乙、丙固体溶于水,配成饱和溶液,需要水的质量为甲<乙<丙
您最近一年使用:0次



