名校
1 . 化学电源在生产生活中有着广泛的应用,同学们常常通过设计实验和查阅资料的方式学习化学电源的相关知识。
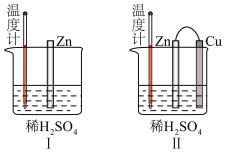
(1)甲同学为了解反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。____ Ⅱ(>、<或=),温度计的示数Ⅰ___ II(>、<或=)。
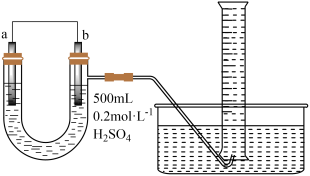
(2)乙同学用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为________ ,当量筒中收集到 336mL(标准状况下)气体时,通过导线的电子的物质的量为_______ 。
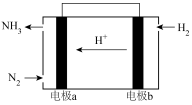
(3)丙同学了解到科学家正在研究利用原电池原理常温常压下合成氨,在该装置如图,电极 a 为____ 极(填“正”或“负”)。_____ ,电解质溶液为_____ ,负极的电极反应式为_____ 。
(1)甲同学为了解反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。
(2)乙同学用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为

(3)丙同学了解到科学家正在研究利用原电池原理常温常压下合成氨,在该装置如图,电极 a 为
您最近一年使用:0次
2024-04-04更新
|
219次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高一下学期4月期中考试化学试题
2 . 部分含N 及Cl物质的分类与相应化合价关系如图所示,下列推断错误的是
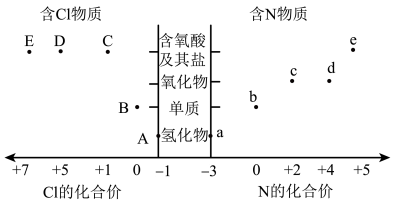
| A.A与过量 a 反应可以产生白烟 |
| B.工业上通过a c d e 来制备HNO3 |
| C.向亚铁盐e 的溶液中滴加A 溶液,无明显现象 |
| D.c a b 和d a b ,一定条件下都可以实现 |
您最近一年使用:0次
2024-04-04更新
|
123次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高一下学期4月期中考试化学试题
解题方法
3 . 回答下列问题。
(1)请用双线桥标出下列反应的电子转移情况:
①Cl2+2NaOH=NaCl+NaClO+H2O:___________ 。
②MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:___________ 。
(2)请写出下列反应的离子方程式。
①钠与水反应的离子方程式:___________ 。
②氢氧化铜与盐酸反应的离子方程式:___________ 。
(3)小苏打可做胃药,治疗胃酸过多,请用化学方程式写出其反应原理:___________ 。
(1)请用双线桥标出下列反应的电子转移情况:
①Cl2+2NaOH=NaCl+NaClO+H2O:
②MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O:
MnCl2+Cl2↑+2H2O:(2)请写出下列反应的离子方程式。
①钠与水反应的离子方程式:
②氢氧化铜与盐酸反应的离子方程式:
(3)小苏打可做胃药,治疗胃酸过多,请用化学方程式写出其反应原理:
您最近一年使用:0次
解题方法
4 . 次氯酸钠是家用消毒剂的有效成分。实验室制备次氯酸钠的装置如图所示。
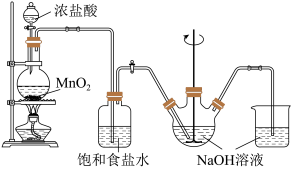
(1)在圆底烧瓶里加入二氧化锰后,通过___________ (填仪器名称)向烧瓶中加入适量的浓盐酸并加热。发生反应的离子方程式为___________ 。
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。
①用双线桥标出该反应中电子转移的方向和数目___________ 。
②若产生标准状况下4.48L ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是___________ mol,转移电子的物质的量为___________ mol。
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:___________ 。

(1)在圆底烧瓶里加入二氧化锰后,通过
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。①用双线桥标出该反应中电子转移的方向和数目
②若产生标准状况下4.48L
 ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:
您最近一年使用:0次
名校
解题方法
5 . 实验室用浓硫酸与铜丝加热生成的 制备少量
制备少量 并检验性质。
并检验性质。 并检验性质
并检验性质
操作及现象:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,试管ⅲ中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
(1)ⅰ中发生反应的化学反应方程式为______ 。
(2)ⅱ中现象说明 具有
具有______ 作用。
(3)若将试管ⅲ与试管ⅱ位置互换,石蕊溶液变为红色能否作为 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:______ 。
Ⅱ.制备 并检验性质
并检验性质
(4)ⅳ中反应的离子方程式为______ 。
(5)进行实验:

①A中溶液褪色,说明 具有
具有______ 性。
②B中产生淡黄色沉淀的离子方程式为______ 。
③C中无明显现象,甲同学通过检测 的生成证明
的生成证明 和
和 发生反应:取1mL C中溶液于试管中,
发生反应:取1mL C中溶液于试管中,______ (填试剂、操作和现象)。
乙同学认为甲同学的实验没有排除 的影响,设计对比实验:
的影响,设计对比实验:______ 。
综合甲、乙同学的实验可知, 能将
能将 氧化。
氧化。
 制备少量
制备少量 并检验性质。
并检验性质。
 并检验性质
并检验性质操作及现象:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,试管ⅲ中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
(1)ⅰ中发生反应的化学反应方程式为
(2)ⅱ中现象说明
 具有
具有(3)若将试管ⅲ与试管ⅱ位置互换,石蕊溶液变为红色能否作为
 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:Ⅱ.制备
 并检验性质
并检验性质(4)ⅳ中反应的离子方程式为
(5)进行实验:

①A中溶液褪色,说明
 具有
具有②B中产生淡黄色沉淀的离子方程式为
③C中无明显现象,甲同学通过检测
 的生成证明
的生成证明 和
和 发生反应:取1mL C中溶液于试管中,
发生反应:取1mL C中溶液于试管中,乙同学认为甲同学的实验没有排除
 的影响,设计对比实验:
的影响,设计对比实验:综合甲、乙同学的实验可知,
 能将
能将 氧化。
氧化。
您最近一年使用:0次
2024-04-03更新
|
102次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高一下学期4月期中考试化学试题
解题方法
6 . 回答下列问题。
(1)将一小块金属钠投入盛有水的烧杯里,钠熔化成闪亮的小球,说明___________ ;向烧杯中滴加酚酞试液,溶液呈___________ 色;其中反应的化学方程式为___________ ;若钠着火,可如何处理?___________ 。
(2)Na2O2可在呼吸面具中作为氧气的来源,其发生反应的化学方程式为___________ 。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用___________ 方法,所涉及的化学方程式为___________ 。
(1)将一小块金属钠投入盛有水的烧杯里,钠熔化成闪亮的小球,说明
(2)Na2O2可在呼吸面具中作为氧气的来源,其发生反应的化学方程式为
(3)除去Na2CO3粉末中混入的NaHCO3杂质用
您最近一年使用:0次
名校
解题方法
7 . 实验室制取下列气体,所选的反应试剂、制备装置与收集方法合理的是

| 选项 | 气体 | 反应试剂 | 制备装置 | 收集方法 |
| A |  | 石灰石、稀硫酸 | b | e |
| B |  |  、浓盐酸 、浓盐酸 | b | d |
| C |  |  、 、 | a | e |
| D |  | Cu、浓硝酸 | b | f |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-03更新
|
133次组卷
|
2卷引用:山西大学附属中学校2023-2024学年高一下学期期中考试化学试题
名校
8 . 设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 熔融态时含有 熔融态时含有 个离子 个离子 |
B. 和 和 混合气体中氧原子总数为 混合气体中氧原子总数为 |
C.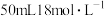 硫酸与足量铜共热,转移的电子数为 硫酸与足量铜共热,转移的电子数为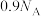 |
D. 的 的 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
您最近一年使用:0次
2024-04-03更新
|
120次组卷
|
2卷引用:山西省阳泉市第一中学校2023-2024学年高一下学期5月期中考试化学试题
名校
解题方法
9 . 氮及其化合物的转化过程如图所示。下列分析不合理的是
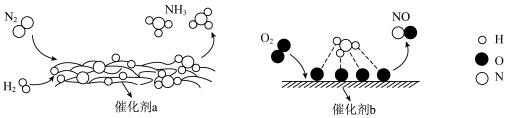
| A.催化剂a表面发生了极性共价键的断裂和形成 |
B. 与 与 反应生成 反应生成 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% |
| C.在催化剂b表面形成氮氧键时,涉及电子转移 |
| D.使用催化剂a、b均可以提高单位时间内生成物的产量 |
您最近一年使用:0次
2024-04-02更新
|
234次组卷
|
3卷引用:山西大学附属中学校2023-2024学年高一下学期期中考试化学试题
名校
解题方法
10 . 能通过单质间化合反应生成的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-04-01更新
|
88次组卷
|
2卷引用:山西省阳泉市第一中学校2023-2024学年高一下学期5月期中考试化学试题



