名校
1 . 某 无土栽培用的营养液中含有
无土栽培用的营养液中含有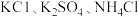 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:

(1)该营养液中 的物质的量浓度为
的物质的量浓度为________  ,含
,含 的质量为
的质量为______________ 。
(2)该营养液中 的物质的量为
的物质的量为__________________ 。
(3)将该营养液加水稀释,稀释过程中 的浓度
的浓度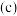 随溶液体积
随溶液体积 变化的曲线如图乙所示,则
变化的曲线如图乙所示,则
________________ 。
 无土栽培用的营养液中含有
无土栽培用的营养液中含有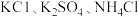 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
(1)该营养液中
 的物质的量浓度为
的物质的量浓度为 ,含
,含 的质量为
的质量为(2)该营养液中
 的物质的量为
的物质的量为(3)将该营养液加水稀释,稀释过程中
 的浓度
的浓度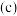 随溶液体积
随溶液体积 变化的曲线如图乙所示,则
变化的曲线如图乙所示,则
您最近一年使用:0次
解题方法
2 . I.SO2和CO2的混合气体38g,测得CO2体积为11.2L(STP),则
(1)混合气体中SO2的质量是_____ g。
(2)混合气体中SO2在标准状况下的体积是____ L。
(3)SO2和CO2同温同压下体积比是_____ 。
(4)标准状况下混合气体的密度为_____ g/L。
II.已知某混合气体的成分按体积分数计算是:80.0%CH4,15.0%C2H4,5.0%C2H6。试计算:
(5)该混合气体的平均式量为_____ ;该混合气体在标准状况下对氢气的密度是_____ 。
(1)混合气体中SO2的质量是
(2)混合气体中SO2在标准状况下的体积是
(3)SO2和CO2同温同压下体积比是
(4)标准状况下混合气体的密度为
II.已知某混合气体的成分按体积分数计算是:80.0%CH4,15.0%C2H4,5.0%C2H6。试计算:
(5)该混合气体的平均式量为
您最近一年使用:0次
名校
3 . 通过计算回答以下问题:
(1)已知标准状况下,双原子分子气体A的密度为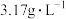 ,则气体A的相对分子质量为
,则气体A的相对分子质量为_________ ,可能是_________ 气体(用化学式表示)。
(2)标准状况下,1.92g某气体的体积为672mL,则此气体的摩尔质量为_________ 。
(3)在一定条件下, 完全分解生成
完全分解生成 、
、 、
、 ,按要求填空。
,按要求填空。
①若所得混合气体对 的相对密度为d,则混合气体的物质的量为
的相对密度为d,则混合气体的物质的量为_________ 。 的摩尔质量为
的摩尔质量为_________ (用含m、d的代数式表示)。
②若所得混合气体的密度折合成标准状况为 ,则混合气体的平均摩尔质量为
,则混合气体的平均摩尔质量为_________ (用含 的代数式表示)。
的代数式表示)。
③若在该条件下,所得 、
、 、
、 的体积分数分别为
的体积分数分别为 、
、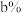 、
、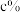 ,则混合气体的平均相对分子质量为
,则混合气体的平均相对分子质量为_________ (用含a、b、c的代数式表示)。
(4)在25℃、101kPa的条件下,等质量的 和A气体的体积之比为15:8,则A的摩尔质量为
和A气体的体积之比为15:8,则A的摩尔质量为_________ 。
(5)相同条件下,有两份 和
和 的体积比为
的体积比为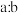 和质量比为
和质量比为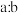 的混合气体,其平均相对分子质量分别
的混合气体,其平均相对分子质量分别_________ 和_________ 。
(1)已知标准状况下,双原子分子气体A的密度为
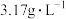 ,则气体A的相对分子质量为
,则气体A的相对分子质量为(2)标准状况下,1.92g某气体的体积为672mL,则此气体的摩尔质量为
(3)在一定条件下,
 完全分解生成
完全分解生成 、
、 、
、 ,按要求填空。
,按要求填空。①若所得混合气体对
 的相对密度为d,则混合气体的物质的量为
的相对密度为d,则混合气体的物质的量为 的摩尔质量为
的摩尔质量为②若所得混合气体的密度折合成标准状况为
 ,则混合气体的平均摩尔质量为
,则混合气体的平均摩尔质量为 的代数式表示)。
的代数式表示)。③若在该条件下,所得
 、
、 、
、 的体积分数分别为
的体积分数分别为 、
、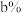 、
、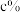 ,则混合气体的平均相对分子质量为
,则混合气体的平均相对分子质量为(4)在25℃、101kPa的条件下,等质量的
 和A气体的体积之比为15:8,则A的摩尔质量为
和A气体的体积之比为15:8,则A的摩尔质量为(5)相同条件下,有两份
 和
和 的体积比为
的体积比为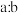 和质量比为
和质量比为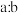 的混合气体,其平均相对分子质量分别
的混合气体,其平均相对分子质量分别
您最近一年使用:0次
2022-11-15更新
|
626次组卷
|
2卷引用:上海市控江中学2022-2023学年高一上学期期中考试化学试题
名校
解题方法
4 . 回答下列问题:
(1)如图为物质B(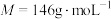 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。

①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为_______ g,物质的量为_______ mol;
②80℃时,物质饱和溶液的物质的量浓度为_______ mol∙L-1。
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。

计算:
①反应后溶液中c(H+)=_______ mol∙L-1 (忽略反应前后溶液体积变化);
②计算常温常压下的气体摩尔体积_______ L∙mol-1。
(1)如图为物质B(
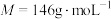 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为
②80℃时,物质饱和溶液的物质的量浓度为
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL
 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
计算:
①反应后溶液中c(H+)=
②计算常温常压下的气体摩尔体积
您最近一年使用:0次
2022-11-15更新
|
226次组卷
|
3卷引用:上海市格致中学2023-2024学年高一上学期期中考试化学试题
名校
5 . 质量、物质的量、物质的量浓度等是用于化学计算的常见物理量。
(1)质量之比为16:7:6的三种气体 、CO、NO。分子个数之比为
、CO、NO。分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下的体积之比为_______ 。
(2)标准状况下,17g 的体积为
的体积为_______ ,含有氢原子个数为_______ ,它与标准状况下_______ L  含有相同数目的氢原子。
含有相同数目的氢原子。
(3)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(4)同温同压下, 气体与
气体与 气体等体积化合,生成
气体等体积化合,生成 气体,已知反应前后气体的密度不变,则
气体,已知反应前后气体的密度不变,则 的分子式为
的分子式为_______ 。
(5)在t℃时将a g 完全溶于水得到V mL溶液,该溶液的密度为
完全溶于水得到V mL溶液,该溶液的密度为 ;质量分数为w,物质的量浓度为c
;质量分数为w,物质的量浓度为c  。下列计算结果正确的是
。下列计算结果正确的是
(6)将a L  和
和 的混合溶液分成两等份,一份加入b mol
的混合溶液分成两等份,一份加入b mol  溶液使溶液中的
溶液使溶液中的 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol ,则原溶液中
,则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全。写出加入NaOH溶液发生的相关离子方程式_______ ,需要NaOH溶液的体积为_______ mL。
(8)常温下A和B两种气体组成的混合物(A的摩尔质量大于B的摩尔质量),经分析混合气体中只含有C、O元素:
①当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是_______ 、_______ 。
②当混合物中C、O的质量比为1:2时,混合气体中A的体积百分数为_______ 。
(1)质量之比为16:7:6的三种气体
 、CO、NO。分子个数之比为
、CO、NO。分子个数之比为(2)标准状况下,17g
 的体积为
的体积为 含有相同数目的氢原子。
含有相同数目的氢原子。(3)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(4)同温同压下,
 气体与
气体与 气体等体积化合,生成
气体等体积化合,生成 气体,已知反应前后气体的密度不变,则
气体,已知反应前后气体的密度不变,则 的分子式为
的分子式为(5)在t℃时将a g
 完全溶于水得到V mL溶液,该溶液的密度为
完全溶于水得到V mL溶液,该溶液的密度为 ;质量分数为w,物质的量浓度为c
;质量分数为w,物质的量浓度为c  。下列计算结果正确的是
。下列计算结果正确的是A.溶质的质量分数 |
B.溶质的物质的量浓度 |
C.溶液密度 可表示为 可表示为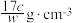 |
| D.上述溶液中再加入V mL水,所得溶液溶质的质量分数小于0.5w |
 和
和 的混合溶液分成两等份,一份加入b mol
的混合溶液分成两等份,一份加入b mol  溶液使溶液中的
溶液使溶液中的 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol ,则原溶液中
,则原溶液中 的物质的量浓度为
的物质的量浓度为(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全。写出加入NaOH溶液发生的相关离子方程式
(8)常温下A和B两种气体组成的混合物(A的摩尔质量大于B的摩尔质量),经分析混合气体中只含有C、O元素:
①当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是
②当混合物中C、O的质量比为1:2时,混合气体中A的体积百分数为
您最近一年使用:0次
6 . 电解26.8%的食盐水1500克,若只有87.3%的食盐发生了反应,求:(请写出相关反应的化学方程式及计算过程,按步骤得分)
(1)在标准状况下可制得氢气多少升?______
(2)这些氢气和氯气全部化合成氯化氢,溶于水制成31%的盐酸,其质量为多少克?(结果保留小数点后一位)______
(1)在标准状况下可制得氢气多少升?
(2)这些氢气和氯气全部化合成氯化氢,溶于水制成31%的盐酸,其质量为多少克?(结果保留小数点后一位)
您最近一年使用:0次
名校
解题方法
7 . 完成下列填空
(1)1.7g氨气在标准状况下的体积约为_______ 升;
(2)在标准状况下硫化氢的密度约为_______ (保留3位有效数字);
(3)等质量的氨气和硫化氢气体分子个数比为_______ ,含氢原子的个数比为_______ 。
(4)标准状况下 和
和 的混合气体0.12g,体积为1.12L,该混合气体对
的混合气体0.12g,体积为1.12L,该混合气体对 的相对密度为
的相对密度为_______ ,其中 的质量分数是
的质量分数是_______ (保留三位有效数字)。
(1)1.7g氨气在标准状况下的体积约为
(2)在标准状况下硫化氢的密度约为
(3)等质量的氨气和硫化氢气体分子个数比为
(4)标准状况下
 和
和 的混合气体0.12g,体积为1.12L,该混合气体对
的混合气体0.12g,体积为1.12L,该混合气体对 的相对密度为
的相对密度为 的质量分数是
的质量分数是
您最近一年使用:0次
名校
解题方法
8 . 甲烷 是一种无色无味的气体,是天然气的主要成分。
是一种无色无味的气体,是天然气的主要成分。
(1)现有 ,它的摩尔质量是
,它的摩尔质量是_______ ,要把 完全燃烧,消耗氧气
完全燃烧,消耗氧气_______ g。
(2)标准状况下, 的密度为
的密度为_______ (保留3位有效数字)。如果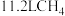 中含有x个氢原子,则阿伏加德罗常数的值为
中含有x个氢原子,则阿伏加德罗常数的值为_______ 。
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为_______ ,密度之比为_______ 。若把质量相等的这两种气体混合,则混合气体的平均相对分子质量为_______ (保留2位有效数字)。
(4)某沼气成分是 和
和 。取2L该沼气与
。取2L该沼气与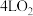 点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中
点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中 和
和 的物质的量之比为(气体体积均在同温同压下测定)
的物质的量之比为(气体体积均在同温同压下测定)_______ 。
 是一种无色无味的气体,是天然气的主要成分。
是一种无色无味的气体,是天然气的主要成分。(1)现有
 ,它的摩尔质量是
,它的摩尔质量是 完全燃烧,消耗氧气
完全燃烧,消耗氧气(2)标准状况下,
 的密度为
的密度为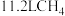 中含有x个氢原子,则阿伏加德罗常数的值为
中含有x个氢原子,则阿伏加德罗常数的值为(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为
(4)某沼气成分是
 和
和 。取2L该沼气与
。取2L该沼气与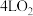 点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中
点燃充分反应后,除去水分,剩余气体的体积为3L。该沼气中 和
和 的物质的量之比为(气体体积均在同温同压下测定)
的物质的量之比为(气体体积均在同温同压下测定)
您最近一年使用:0次
名校
解题方法
9 . 向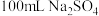 和
和 的混合溶液中加过量
的混合溶液中加过量 溶液得到
溶液得到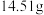 白色沉淀,向白色沉淀中再加过量稀
白色沉淀,向白色沉淀中再加过量稀 ,充分反应后,沉淀减少
,充分反应后,沉淀减少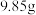 并有气体产生。
并有气体产生。
(1)求原混合物中 的物质的量浓度
的物质的量浓度_______ 。
(2)从原溶液中取出 ,在标准状况下与足量的盐酸反应,可生成
,在标准状况下与足量的盐酸反应,可生成
_______ mL。
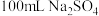 和
和 的混合溶液中加过量
的混合溶液中加过量 溶液得到
溶液得到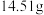 白色沉淀,向白色沉淀中再加过量稀
白色沉淀,向白色沉淀中再加过量稀 ,充分反应后,沉淀减少
,充分反应后,沉淀减少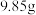 并有气体产生。
并有气体产生。(1)求原混合物中
 的物质的量浓度
的物质的量浓度(2)从原溶液中取出
 ,在标准状况下与足量的盐酸反应,可生成
,在标准状况下与足量的盐酸反应,可生成
您最近一年使用:0次
名校
10 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。NaClO是“84”消毒液的有效成分,常温下,氯气与烧碱溶液反应得“84”消毒液,已知 与浓盐酸反应的化学方程式如下,该反应可以用来制取氯气:
与浓盐酸反应的化学方程式如下,该反应可以用来制取氯气: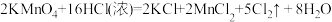
(1)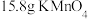 能和
能和_______ 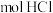 发生上述反应。
发生上述反应。
(2)产生的 在标准状况下的体积为
在标准状况下的体积为_______ L。
 与浓盐酸反应的化学方程式如下,该反应可以用来制取氯气:
与浓盐酸反应的化学方程式如下,该反应可以用来制取氯气: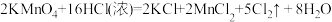
(1)
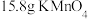 能和
能和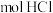 发生上述反应。
发生上述反应。(2)产生的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次



