1 . 回答下列问题:
(1)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是_______ ,所含的原子数比是_______ 。
(2)12.4克Na2R中含Na+0.4mol,则Na2R摩尔质量为_______ 。
(3)无土栽培试验时需要配制两份成分完全相同的某营养液各1L,配方如下表。
配方表(每升溶液所含溶质的物质的量)
①所配制的溶液中,K+的物质的量浓度为_______ 。
②实验员在配完第一份溶液时发现,实验室的ZnSO4已经用完了,锌盐中只剩下了氯化锌(ZnCl2)。请为实验员想想如何配,使第二份营养液与第一份营养液的成份完全相同(将所需溶质的物质的量填入下列横线中):KCl_______ 、K2SO4_______ 、ZnCl2_______ 。
(1)0.1mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是
(2)12.4克Na2R中含Na+0.4mol,则Na2R摩尔质量为
(3)无土栽培试验时需要配制两份成分完全相同的某营养液各1L,配方如下表。
配方表(每升溶液所含溶质的物质的量)
| 溶质 | KCl | K2SO4 | ZnSO4 |
| 物质的量/mol | 0.3 | 0.2 | 0.1 |
①所配制的溶液中,K+的物质的量浓度为
②实验员在配完第一份溶液时发现,实验室的ZnSO4已经用完了,锌盐中只剩下了氯化锌(ZnCl2)。请为实验员想想如何配,使第二份营养液与第一份营养液的成份完全相同(将所需溶质的物质的量填入下列横线中):KCl
您最近一年使用:0次
解题方法
2 . 工业上利用电解饱和食盐水可制得重要化工产品,该工业又称为“氯碱工业”。
(1)电解饱和食盐水的化学方程式为_______ ;常用_______ 检验与电源正极相连的电极上产生的气体,相关的化学方程式为_______ 。
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为_______ ;氯水不稳定,需现用现配,下列制备氯水的装置最合理的是_______ (填字母)。

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为_______ 。
(1)电解饱和食盐水的化学方程式为
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为
您最近一年使用:0次
解题方法
3 . 下列实验基本操作不正确 的是
| A.进行蒸馏操作时,冷凝管中的冷凝水应从下口进,上口出 |
| B.进行蒸发操作时,应待大量晶体析出,利用余热将剩余水分蒸干 |
| C.试纸在检测气体时都需湿润并粘在玻璃棒的一端 |
| D.配制750mL0.1mol·L-1的NaCl溶液时,选择规格为250mL和500mL两个容量瓶 |
您最近一年使用:0次
解题方法
4 . 下列说法不正确 的是
| A.可用分液漏斗分离氯化钠溶液和四氯化碳的混合物 |
| B.用托盘天平称量11.7g氯化钠晶体 |
| C.用润湿的pH试纸测定pH值一定有误差 |
| D.用元素分析仪确定物质中是否含有C、H、O、N、S、Cl、Br等元素 |
您最近一年使用:0次
名校
解题方法
5 . 有X、Y、Z三种元素,已知Y与X形成的化合物YX中,X的化合价为-1价,Y与Z可能形成化合物Y2Z,X、Y、Z离子的核外电子数目均为10。下列说法不正确 的是
| A.X为非金属性最强的元素 |
| B.Y的最高价氧化物对应水化物为强碱 |
| C.Z与氢元素形成的化合物只有一种 |
| D.Y2Z为离子化合物 |
您最近一年使用:0次
2022-02-20更新
|
387次组卷
|
5卷引用:浙江省临海市回浦中学2021-2022学年高一上学期第二次质量抽测(12月)化学试题
名校
解题方法
6 . 下列说明不正确 的是
| A.轻微烫伤,可先用洁净的冷水处理,降低局部温度,然后涂上烫伤药膏 |
| B.如果不慎将酸沾到皮肤上,应立即用大量水冲洗,然后用NaOH溶液涂在皮肤上 |
| C.一旦发生火情,应立即切断室内电源,移走可燃物 |
| D.易燃物如钠、钾等若随便丢弃易引起火灾,可以将未用完的钠、钾等放回原试剂瓶 |
您最近一年使用:0次
7 . 下列说法错误 的是
| A.胶体与溶液的本质区别是分散质微粒直径的大小 |
| B.氯气是一种有毒的气体,所以不可能用于自来水的杀菌消毒 |
| C.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物 |
| D.当火灾现场有大量钠等金属时,不可以用水或泡沫灭火器来灭火 |
您最近一年使用:0次
8 . 铅在氧化物中的价态有+2价和+4价,含+4价铅的氧化物是一种很强的氧化剂,常温时在酸性条件下可将 氧化成
氧化成 ,自身还原为+2价。
,自身还原为+2价。 在加热过程发生分解的失重曲线如下图所示。
在加热过程发生分解的失重曲线如下图所示。

已知: 。
。
请计算:
(1)若用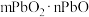 表示A点的化学组成,则
表示A点的化学组成,则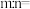
_______ 。
(2)取71.7g ,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g
,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g 。求剩余固体中氧元素的质量
。求剩余固体中氧元素的质量_______ 。(写出计算过程)
 氧化成
氧化成 ,自身还原为+2价。
,自身还原为+2价。 在加热过程发生分解的失重曲线如下图所示。
在加热过程发生分解的失重曲线如下图所示。
已知:
 。
。请计算:
(1)若用
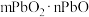 表示A点的化学组成,则
表示A点的化学组成,则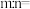
(2)取71.7g
 ,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g
,加热一段时间后冷却,在剩余的固体中加足量浓盐酸充分反应,生成7.1g 。求剩余固体中氧元素的质量
。求剩余固体中氧元素的质量
您最近一年使用:0次
名校
9 . 连二亚硫酸钠( )俗称保险粉,是印染工业中常用的漂白剂。具有以下性质:
)俗称保险粉,是印染工业中常用的漂白剂。具有以下性质:
Ⅰ.易溶于水且随温度升高溶解度增大,难溶于酒精;
Ⅱ.酸性条件下易分解、碱性条件下稳定,固态时 相对
相对 较稳定;
较稳定;
Ⅲ.水溶液中低于52℃以 形态结晶,碱性溶液中高于52℃脱水成无水盐。
形态结晶,碱性溶液中高于52℃脱水成无水盐。
工业中经典的制取方法是以 、Zn、NaOH为原料,主要反应及实验室模拟流程如下:
、Zn、NaOH为原料,主要反应及实验室模拟流程如下: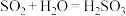 ;
; ;
;

(1)步骤①的反应装置如图。

制备 选用的最佳试剂组合为
选用的最佳试剂组合为_______ 。
A.70%硫酸+ 固体 B.10%硫酸+
固体 B.10%硫酸+ 固体
固体
C.70%硫酸+饱和 溶液 D.稀硝酸+饱和
溶液 D.稀硝酸+饱和 溶液
溶液
虚线方框内仪器的作用是_______ 。反应控制在35℃~45℃的原因是_______ 。
(2)步骤②加过量NaOH溶液的作用除了使 充分生成
充分生成 外,还有一个作用是
外,还有一个作用是_______ 。
(3)从下列操作中选择合理操作完成步骤③并排序: 溶液→
溶液→_______ →_______ →_______ →_______ →干燥。
a.搅拌下通入略高于60℃的水蒸气;b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;c.趁热过滤;d.用酒精水溶液洗涤;e.用酒精洗涤;f.用水洗涤
(4)产品纯度测定。取1.2800g产品与足量甲醛水溶液混合于锥形瓶中,生成甲醛亚硫酸氢钠与甲醛次硫酸氢钠: ,在所得的混合溶液中加入3.8100g I2、轻轻振荡,发生反应:
,在所得的混合溶液中加入3.8100g I2、轻轻振荡,发生反应: 。过量的
。过量的 以淀粉为指示剂,用0.1000
以淀粉为指示剂,用0.1000 的标准
的标准 溶液滴定:
溶液滴定: 。消耗标准
。消耗标准 溶液20.00mL。
溶液20.00mL。
①则产品的纯度为_______ 。(精确到0.01%)
②下列操作会导致测定的纯度偏高的是_______ 。
A.装标准 溶液的满定管用蒸馏水洗涤后没有用标准液润洗
溶液的满定管用蒸馏水洗涤后没有用标准液润洗
B.滴定前尖嘴处有气泡,滴定后无气泡
C.起始读数正确,滴定后俯视读数
D.制备时由于操作不当,样品中混有
E.滴定时当溶液由蓝色变成无色时立即读数,半分钟后又变回蓝色
 )俗称保险粉,是印染工业中常用的漂白剂。具有以下性质:
)俗称保险粉,是印染工业中常用的漂白剂。具有以下性质:Ⅰ.易溶于水且随温度升高溶解度增大,难溶于酒精;
Ⅱ.酸性条件下易分解、碱性条件下稳定,固态时
 相对
相对 较稳定;
较稳定;Ⅲ.水溶液中低于52℃以
 形态结晶,碱性溶液中高于52℃脱水成无水盐。
形态结晶,碱性溶液中高于52℃脱水成无水盐。工业中经典的制取方法是以
 、Zn、NaOH为原料,主要反应及实验室模拟流程如下:
、Zn、NaOH为原料,主要反应及实验室模拟流程如下: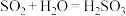 ;
; ;
;

(1)步骤①的反应装置如图。

制备
 选用的最佳试剂组合为
选用的最佳试剂组合为A.70%硫酸+
 固体 B.10%硫酸+
固体 B.10%硫酸+ 固体
固体C.70%硫酸+饱和
 溶液 D.稀硝酸+饱和
溶液 D.稀硝酸+饱和 溶液
溶液虚线方框内仪器的作用是
(2)步骤②加过量NaOH溶液的作用除了使
 充分生成
充分生成 外,还有一个作用是
外,还有一个作用是(3)从下列操作中选择合理操作完成步骤③并排序:
 溶液→
溶液→a.搅拌下通入略高于60℃的水蒸气;b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;c.趁热过滤;d.用酒精水溶液洗涤;e.用酒精洗涤;f.用水洗涤
(4)产品纯度测定。取1.2800g产品与足量甲醛水溶液混合于锥形瓶中,生成甲醛亚硫酸氢钠与甲醛次硫酸氢钠:
 ,在所得的混合溶液中加入3.8100g I2、轻轻振荡,发生反应:
,在所得的混合溶液中加入3.8100g I2、轻轻振荡,发生反应: 。过量的
。过量的 以淀粉为指示剂,用0.1000
以淀粉为指示剂,用0.1000 的标准
的标准 溶液滴定:
溶液滴定: 。消耗标准
。消耗标准 溶液20.00mL。
溶液20.00mL。①则产品的纯度为
②下列操作会导致测定的纯度偏高的是
A.装标准
 溶液的满定管用蒸馏水洗涤后没有用标准液润洗
溶液的满定管用蒸馏水洗涤后没有用标准液润洗B.滴定前尖嘴处有气泡,滴定后无气泡
C.起始读数正确,滴定后俯视读数
D.制备时由于操作不当,样品中混有

E.滴定时当溶液由蓝色变成无色时立即读数,半分钟后又变回蓝色
您最近一年使用:0次
2021-11-19更新
|
705次组卷
|
4卷引用:浙江省台州市2021-2022学年上学期高三11月选考科目教学质量评估化学试题
浙江省台州市2021-2022学年上学期高三11月选考科目教学质量评估化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】17(已下线)解密13 实验化学(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省乐清市知临中学2023届高三下学期第二次仿真考试化学试题
解题方法
10 . 氢气在实验室和工业上有着广泛的用途。请回答:
(1)氢气可以与煤在催化剂作用下制备乙炔,已知部分反应如下:
Ⅰ.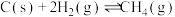

Ⅱ.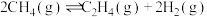

Ⅲ.
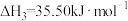
Ⅳ.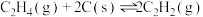

通过计算说明反应Ⅳ自发进行的条件_______ 。
(2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以 的投料比充入体积固定的密闭容器中,发生反应:
的投料比充入体积固定的密闭容器中,发生反应:
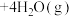 ,平衡时水蒸气的物质的量百分数为50.0%。请回答:
,平衡时水蒸气的物质的量百分数为50.0%。请回答:
①反应的平衡常数表达式为_______ 。
②达到平衡时, 的转化率为
的转化率为_______ 。
(3)氢气可合成氨气,氨气与二氧化碳可以合成尿素,反应为:
 ,分为两步:
,分为两步:
已知投料的组成为 、
、 和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵(
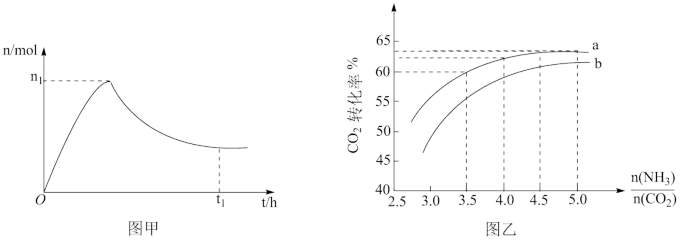
和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵( )物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(
)物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(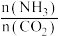 )与水碳比(
)与水碳比(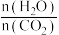 )投料时
)投料时 平衡转化率图象(图乙,a、b代表水碳比):
平衡转化率图象(图乙,a、b代表水碳比):
回答下列问题:
①已知反应I又可以分成两步:_______、 ,请写出第一步的化学方程式
,请写出第一步的化学方程式_______ 。
②下列叙述正确的是_______ 。
A.反应Ⅰ的活化能大于反应Ⅱ,
B.增大氨碳比有利于提高尿素产率,原因之一是过量氨气与反应Ⅱ生成的水反应,促进平衡正移
C.实际生产中若选择曲线a,则氨碳比应控制在4.0左右
D.曲线a的水碳比大于曲线b,减小水碳比有利于尿素生成
③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,请在图甲中画出保持其他条件不变,加入该催化剂后从0h到t1时的氨基甲酸铵物质的量变化曲线_______ 。
(1)氢气可以与煤在催化剂作用下制备乙炔,已知部分反应如下:
Ⅰ.
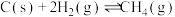

Ⅱ.
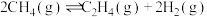

Ⅲ.

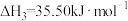
Ⅳ.
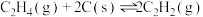

通过计算说明反应Ⅳ自发进行的条件
(2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以
 的投料比充入体积固定的密闭容器中,发生反应:
的投料比充入体积固定的密闭容器中,发生反应:
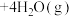 ,平衡时水蒸气的物质的量百分数为50.0%。请回答:
,平衡时水蒸气的物质的量百分数为50.0%。请回答:①反应的平衡常数表达式为
②达到平衡时,
 的转化率为
的转化率为(3)氢气可合成氨气,氨气与二氧化碳可以合成尿素,反应为:

 ,分为两步:
,分为两步:反应步骤 | 反应方程式 |
|
| Ⅰ | 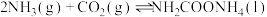  | 快速放热 |
| Ⅱ |  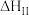 | 慢速吸热 |
已知投料的组成为
 、
、 和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵(
和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵( )物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(
)物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(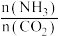 )与水碳比(
)与水碳比(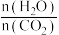 )投料时
)投料时 平衡转化率图象(图乙,a、b代表水碳比):
平衡转化率图象(图乙,a、b代表水碳比):
回答下列问题:
①已知反应I又可以分成两步:_______、
 ,请写出第一步的化学方程式
,请写出第一步的化学方程式②下列叙述正确的是
A.反应Ⅰ的活化能大于反应Ⅱ,

B.增大氨碳比有利于提高尿素产率,原因之一是过量氨气与反应Ⅱ生成的水反应,促进平衡正移
C.实际生产中若选择曲线a,则氨碳比应控制在4.0左右
D.曲线a的水碳比大于曲线b,减小水碳比有利于尿素生成
③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,请在图甲中画出保持其他条件不变,加入该催化剂后从0h到t1时的氨基甲酸铵物质的量变化曲线
您最近一年使用:0次



