名校
解题方法
1 . I.由于基团间相互影响导致O-H键极性有差异,进而导致酸性强弱不同。
(1)下列四种羧酸,①FClCHCOOH、②Cl2CHCOOH、③ClCH2COOH、④CH3COOH,其中酸性最强的是___________ (填序号,下同),分子中含有手性碳原子的是___________ 。
II:下列转化:

(2)转化①、②、③、⑤所需的足量试剂分别为___________ 。
(3)写出转化④中加入少量CO2、H2O的化学方程式___________ 。
(1)下列四种羧酸,①FClCHCOOH、②Cl2CHCOOH、③ClCH2COOH、④CH3COOH,其中酸性最强的是
II:下列转化:

(2)转化①、②、③、⑤所需的足量试剂分别为
(3)写出转化④中加入少量CO2、H2O的化学方程式
您最近一年使用:0次
名校
2 . 有机玻璃(聚甲基丙烯酸甲酯,结构见流程)用途广泛。一种合成路线如下:
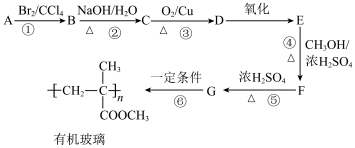
(1)已知原料A的分子式为C4H8,核磁共振氢谱中有两个吸收峰,并且面积比为1:3,则所属的物质类别为___________ 。
(2)写出流程中标有序号的六个反应中,属于取代反应的是___________ 。
(3)E中含有两种官能团,名称分别为___________ 。
(4)写出流程中反应的化学方程式②___________ ;③___________ 。
(5)G有多种同分异构体,写出期中一种链状的,含有-COOH且为顺式结构的同分异构体的结构简式___________ (写出一种即可)。

(1)已知原料A的分子式为C4H8,核磁共振氢谱中有两个吸收峰,并且面积比为1:3,则所属的物质类别为
(2)写出流程中标有序号的六个反应中,属于取代反应的是
(3)E中含有两种官能团,名称分别为
(4)写出流程中反应的化学方程式②
(5)G有多种同分异构体,写出期中一种链状的,含有-COOH且为顺式结构的同分异构体的结构简式
您最近一年使用:0次
名校
3 . 下列有机物
①CH3CH2=CH2;②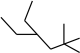 ;③
;③ ;④
;④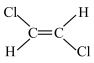 ;⑤CH2=CH-C≡C-CH3;⑥CH3CH(OH)CH3;⑦CH2=C-CH2-CH3;⑧
;⑤CH2=CH-C≡C-CH3;⑥CH3CH(OH)CH3;⑦CH2=C-CH2-CH3;⑧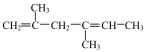 ;⑨
;⑨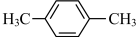 ;
;
(1)请用系统命名法命名有机物②___________ ,⑦___________ 。
(2)写出①发生加聚反应的化学方程式___________ 。
(3)⑤中碳原子的杂化方式为___________ 。
(4)⑧被酸性高猛酸钾氧化的产物为___________ 。
(5)属于非极性分子的是___________ (填序号,下同)。
(6)所有原子一定共面的是___________ 。
(7)水溶性最好的是___________ ,原因是___________ 。
①CH3CH2=CH2;②
 ;③
;③ ;④
;④ ;⑤CH2=CH-C≡C-CH3;⑥CH3CH(OH)CH3;⑦CH2=C-CH2-CH3;⑧
;⑤CH2=CH-C≡C-CH3;⑥CH3CH(OH)CH3;⑦CH2=C-CH2-CH3;⑧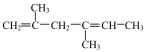 ;⑨
;⑨ ;
;(1)请用系统命名法命名有机物②
(2)写出①发生加聚反应的化学方程式
(3)⑤中碳原子的杂化方式为
(4)⑧被酸性高猛酸钾氧化的产物为
(5)属于非极性分子的是
(6)所有原子一定共面的是
(7)水溶性最好的是
您最近一年使用:0次
名校
解题方法
4 . 下列关于基团相互影响的说法错误的是
| A.甲苯能使酸性KMnO4溶液褪色,是因为苯环使甲基活化 |
| B.苯酚溶液呈酸性,是因为苯环使羟基活化 |
| C.苯酚和饱和溴水生成三溴苯酚白色沉淀,是因为羟基使苯环活化 |
| D.甲苯能与H2加成,是因为甲基使苯环活化 |
您最近一年使用:0次
2023-12-28更新
|
314次组卷
|
3卷引用:北京市第一○一中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
5 . 为验证“2Fe3++2I- 2Fe2++I2”是可逆反应,进行以下实验。
2Fe2++I2”是可逆反应,进行以下实验。
【试剂】
【实验I】

(1)③中出现的实验现象是___________ ,④中加入试剂b______ (填化学式)溶液后,溶液颜色变红。由③、④可得结论:在该条件下充分反应后,反应物与生成物仍能同时存在,即可说明该反应是可逆反应。
(2)⑤中出现的实验现象是________ 。请用化学平衡移动原理解释⑤中现象产生的原因是_______ 。由此可得结论:若改变反应条件可以出现平衡移动现象,即可说明该反应是可逆反应。
【实验Ⅱ】
(3)如图所示的原电池装置,a、b均为石墨电极。闭合开关K后,检流计指针向右偏转,b发生的电极反应式是___________ 。
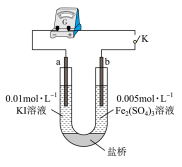
(4)当指针归零后,向U型管左管中滴加少量0.01mol/LAgNO3溶液。产生的现象是________ 。此时,b发生的电极反应式是___________ 。在该装置中,改变反应条件出现了平衡移动的现象,说明该反应是可逆反应。
(5)通过以上实验,可以证实“2Fe3++2I- 2Fe2++I2”是可逆反应。以下事实能说明该反应达到化学平衡状态的是
2Fe2++I2”是可逆反应。以下事实能说明该反应达到化学平衡状态的是___________ (填字母)。
a.①中各物质浓度不再改变 b.⑤中溶液颜色不再改变 c.实验Ⅱ中检流计指针归零
 2Fe2++I2”是可逆反应,进行以下实验。
2Fe2++I2”是可逆反应,进行以下实验。【试剂】
| 试剂 | Fe2(SO4)3溶液0.005mol·L-1 | KI溶液0.01mol·L-1 | KI溶液1mol·L-1 |
| 颜色 | 浅黄色 | 无色 | 无色 |

(1)③中出现的实验现象是
(2)⑤中出现的实验现象是
【实验Ⅱ】
(3)如图所示的原电池装置,a、b均为石墨电极。闭合开关K后,检流计指针向右偏转,b发生的电极反应式是

(4)当指针归零后,向U型管左管中滴加少量0.01mol/LAgNO3溶液。产生的现象是
(5)通过以上实验,可以证实“2Fe3++2I-
 2Fe2++I2”是可逆反应。以下事实能说明该反应达到化学平衡状态的是
2Fe2++I2”是可逆反应。以下事实能说明该反应达到化学平衡状态的是a.①中各物质浓度不再改变 b.⑤中溶液颜色不再改变 c.实验Ⅱ中检流计指针归零
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是___________ ,用平衡原理解释原因___________ 。
(2)常温下,0.1 mol/L 的NaOH溶液的pH=___________ ,0.05mol/L的硫酸的pH=___________ ,取一定体积的两溶液混合,所得混合液的pH=2,则所取硫酸溶液的体积与NaOH溶液的体积比为___________ 。
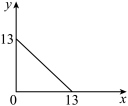
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为___________ ,则该温度t___________ 25℃(填“>”“<”或“=”)。
(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为___________ 。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是
(2)常温下,0.1 mol/L 的NaOH溶液的pH=
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为

(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
7 . 化合物A~H存在如下转化关系:
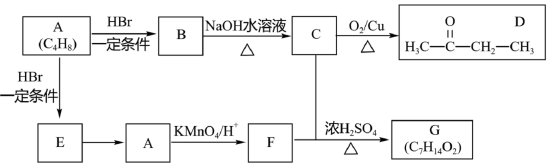
其中A为链状化合物,B、E为一对同分异构体。
已知:R-CH=CH2 R-COOH + H2O + CO2
R-COOH + H2O + CO2
(1)写出A的结构简式___________ 。
(2)物质C的系统命名法为___________ 。
(3)写出B、E的其他2种同分异构体___________ ,___________ 。
(4)写出C和F反应生成G的化学方程式:___________ 。
(5)关于上述有机物的描述中,正确的是___________ 。
a.由A到B的反应为加成反应
b.C的核磁共振氢谱图中有4组信号峰
c.由E重新生成A的反应条件为浓硫酸、加热
d.在一定条件下,E、F与G均可与NaOH水溶液发生反应
(6)工业生产中利用A的同分异构体(2-甲基丙烯)与CH3OH在一定条件下发生加成反应制备一种醚类化合物。
①写出该反应的化学方程式___________ 。
②实际生产中不采用醇分子间脱水反应制备此醚类化合物,主要原因是该过程中会发生很多副反应。试写出至少两种可能生成的副产物___________ ,___________ 。

其中A为链状化合物,B、E为一对同分异构体。
已知:R-CH=CH2
 R-COOH + H2O + CO2
R-COOH + H2O + CO2(1)写出A的结构简式
(2)物质C的系统命名法为
(3)写出B、E的其他2种同分异构体
(4)写出C和F反应生成G的化学方程式:
(5)关于上述有机物的描述中,正确的是
a.由A到B的反应为加成反应
b.C的核磁共振氢谱图中有4组信号峰
c.由E重新生成A的反应条件为浓硫酸、加热
d.在一定条件下,E、F与G均可与NaOH水溶液发生反应
(6)工业生产中利用A的同分异构体(2-甲基丙烯)与CH3OH在一定条件下发生加成反应制备一种醚类化合物。
①写出该反应的化学方程式
②实际生产中不采用醇分子间脱水反应制备此醚类化合物,主要原因是该过程中会发生很多副反应。试写出至少两种可能生成的副产物
您最近一年使用:0次
名校
8 . 有一种历史悠久的解热镇痛药A,该药物微溶于水,化学式为C9H8O4,分子含有苯环,不含其他环状结构。某小组同学进行了如下实验,推断A中可能含有的官能团。
(1)首先基于分子组成推测A可能的分子结构。计算A分子的不饱和度为Ω=___________ 。推测A中官能团的组合可能为___________ :
a.2个羧基 b.1个羧基、1个酯基 c.2个酚羟基、3个碳碳双键
(2)其次基于实验探究确定A中含有的官能团。取一片A药片在研钵中研碎,将粉末置于烧杯中,加少量水溶解。分别取上清液开展如下实验,请将实验记录补充完整。
(3)另从烧杯中取上清液,向其中加适量NaOH溶液,加热几分钟,冷却后朱滴滴入稀硫酸,边滴加边振荡,再滴加氯化铁溶液,观察到溶液逐渐变为紫色,说明A中含有的官能团为___________ 。
(4)经查阅资料,A中有两个取代基,位于苯环上的相邻位置。写出A与足量NaOH反应的化学方程式:___________ 。
(5)请以甲苯为原料,设计合成该药物A,无机试剂任选,写出合成路线____________ 。
已知:i.
ii.苯环上的取代基分为两类:第一类取代基主要使新导入的取代基进入苯环的邻位或对位,如-CH3;第二类取代基主要使新导入的取代基进入苯环的间位,如-COOH。
(6)后来,人们发现了一种解热镇痛效果更好的药物——贝诺酯,它是由药物A与药物B( )经酯化反应后得到的产物,据此写出贝诺酯的结构:
)经酯化反应后得到的产物,据此写出贝诺酯的结构:____________ 。
(1)首先基于分子组成推测A可能的分子结构。计算A分子的不饱和度为Ω=
a.2个羧基 b.1个羧基、1个酯基 c.2个酚羟基、3个碳碳双键
(2)其次基于实验探究确定A中含有的官能团。取一片A药片在研钵中研碎,将粉末置于烧杯中,加少量水溶解。分别取上清液开展如下实验,请将实验记录补充完整。
| 操作 | 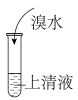 |  | 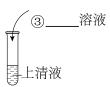 |  |
| 实验现象 | 无明显现象 | ② | ④ | ⑤ |
| 结论 | 该结构中不含 ① | 该结构不含酚羟基 | 该结构中含有羧基(-COOH) | 该结构中不含醛基(-CHO) |
(3)另从烧杯中取上清液,向其中加适量NaOH溶液,加热几分钟,冷却后朱滴滴入稀硫酸,边滴加边振荡,再滴加氯化铁溶液,观察到溶液逐渐变为紫色,说明A中含有的官能团为
(4)经查阅资料,A中有两个取代基,位于苯环上的相邻位置。写出A与足量NaOH反应的化学方程式:
(5)请以甲苯为原料,设计合成该药物A,无机试剂任选,写出合成路线
已知:i.

ii.苯环上的取代基分为两类:第一类取代基主要使新导入的取代基进入苯环的邻位或对位,如-CH3;第二类取代基主要使新导入的取代基进入苯环的间位,如-COOH。
(6)后来,人们发现了一种解热镇痛效果更好的药物——贝诺酯,它是由药物A与药物B(
 )经酯化反应后得到的产物,据此写出贝诺酯的结构:
)经酯化反应后得到的产物,据此写出贝诺酯的结构:
您最近一年使用:0次
名校
9 . 茶叶中含有丰富的有机物,通过不同提取方法可以获得不同的有机物成分。
I.从茶叶中提取咖啡因的主要流程如下:

资料:咖啡因能溶于乙醇等溶剂,120℃升华显著,熔点为238℃
(1)第①步使用乙醇提取咖啡因的原因是___________ 。
(2)步骤②使用的装置是___________ (填序号)。
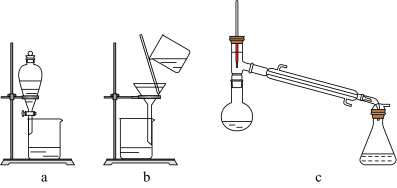
(3)上述步骤中主要利用化学变化进行物质分离的是___________ (填数字序号)。
(4)由液相色谱法从茶叶中可以分离得到B,为确定B的结构,进行如下实验:
综上所述,B的结构简式是___________ 。
I.从茶叶中提取咖啡因的主要流程如下:

资料:咖啡因能溶于乙醇等溶剂,120℃升华显著,熔点为238℃
(1)第①步使用乙醇提取咖啡因的原因是
(2)步骤②使用的装置是

(3)上述步骤中主要利用化学变化进行物质分离的是
(4)由液相色谱法从茶叶中可以分离得到B,为确定B的结构,进行如下实验:
| 实验步骤 | 解释或实验结论 |
| ①取适量B用质谱仪确定相对分子质量 | B的相对分子质量212 |
| ②将此2.12gB在足量纯O2中充分燃烧,使其产物依次缓缓通过浓硫酸,碱石灰,计算发现生成0.06mol H2O和0.10molCO2 | B的分子式为 |
| ③B能使FeCl3溶液变紫色,另取2.12gB与足量NaOH溶液反应,最多消耗0.04molNaOH,且产物之一是1-丙醇 | B中含有的官能团有: |
| ④B的核磁共振氢谱有6组信号峰且峰面积比为1:2:2:2:2:3,且环上有3个相同的取代基位于相邻位置。 | B中含 |
您最近一年使用:0次
名校
10 . 填空
(1)五倍子被广泛应用于有机合成,其结构简式 ,为根据该物质的结构推测其可能具有的化学性质
,为根据该物质的结构推测其可能具有的化学性质
①该有机物显酸性,能与碳酸钠反应。
②该有机物能与______ 反应。
③该有机物能与______ 反应。
(2)阿司匹林可用于解热镇痛,其结构简式为 ,写出其核磁共振氢谱有四个峰的同分异构体(至少写四种)
,写出其核磁共振氢谱有四个峰的同分异构体(至少写四种)______ 、______ 、______ 、______
(1)五倍子被广泛应用于有机合成,其结构简式
 ,为根据该物质的结构推测其可能具有的化学性质
,为根据该物质的结构推测其可能具有的化学性质①该有机物显酸性,能与碳酸钠反应。
②该有机物能与
③该有机物能与
(2)阿司匹林可用于解热镇痛,其结构简式为
 ,写出其核磁共振氢谱有四个峰的同分异构体(至少写四种)
,写出其核磁共振氢谱有四个峰的同分异构体(至少写四种)
您最近一年使用:0次



