名校
解题方法
1 . 1909年哈伯(P•Haber)在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮,对人类的生存和发展有着重要意义,因此获得了诺贝尔奖。请回答:
(1)已知:①N2(g)+O2(g) 2NO(g) K(298K)=5×10-31
2NO(g) K(298K)=5×10-31
②N2(g)+3H2(g 2NH3(g) K(298K)=4×106
2NH3(g) K(298K)=4×106
分析以上数据,说明工业固氮选择反应②而非反应①的原因是_____ 。
(2)在铁触媒催化和30MPa下,合成氨反应平衡体系中氨的含量随温度的变化如下表所示。
目前工业实际生产一般选择500℃,其主要原因是_____ 。
(3)化学家GethardErtl证实了氮气与氢气在固体催化剂表面合成氨的过程,示意图如下:

下列说法正确的是_____
(4)在如图密闭容器中充入2molN2和6molH2,固定活塞保持容器体积为5L,在一定温度下催化反应,NH3的物质的量浓度随时间的变化如图所示。求:
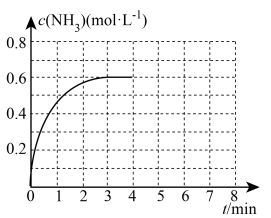
①前3min内平均反应速率:v(H2)=_____ 。
②平衡常数:K=_____ 。
③若在4min时,开启活塞保持恒温恒压,从容器中快速分离出2molNH3,在6min时,反应重新达到化学平衡,在下图1中画出4~8min内氨气的浓度变化曲线_____ 。
(5)我国科学家研制了Ti-H-Fe双温区催化剂(温差达100℃)合成氨,其主反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。
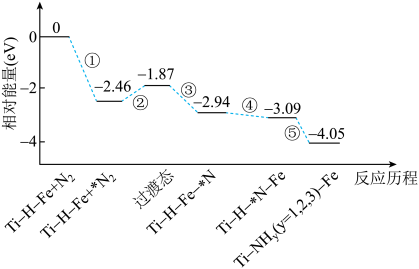
①②③所在Fe区域为_____ 温区(填:高或低),有利于_____ ;
④⑤所在Ti-H区域的温度有利于_____ 。
(1)已知:①N2(g)+O2(g)
 2NO(g) K(298K)=5×10-31
2NO(g) K(298K)=5×10-31②N2(g)+3H2(g
 2NH3(g) K(298K)=4×106
2NH3(g) K(298K)=4×106分析以上数据,说明工业固氮选择反应②而非反应①的原因是
(2)在铁触媒催化和30MPa下,合成氨反应平衡体系中氨的含量随温度的变化如下表所示。
| 温度/℃ | 200 | 300 | 400 | 500 |
| 氨的平衡含量 | 89.9% | 71.0% | 47.0% | 26.4% |
(3)化学家GethardErtl证实了氮气与氢气在固体催化剂表面合成氨的过程,示意图如下:

下列说法正确的是_____
| A.①→②吸附过程放热,有利于化学键的断裂,从而降低反应的活化能 |
| B.整个反应过程中,能量状态最低的是⑤处 |
| C.适时从反应体系中分离出氨气,有利于提高氨的解吸速率 |
| D.氮气和氢气以一定流速通过反应器,是否使用催化剂,对反应物的转化率无影响 |

①前3min内平均反应速率:v(H2)=
②平衡常数:K=
③若在4min时,开启活塞保持恒温恒压,从容器中快速分离出2molNH3,在6min时,反应重新达到化学平衡,在下图1中画出4~8min内氨气的浓度变化曲线
(5)我国科学家研制了Ti-H-Fe双温区催化剂(温差达100℃)合成氨,其主反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。

①②③所在Fe区域为
④⑤所在Ti-H区域的温度有利于
您最近一年使用:0次
名校
2 . 完成下列小题
(1)①如图表示某反应的能量变化关系图,该反应的△H=_____ kJ/mol(用a~e表示)。

②已知:2H2(g)+O2(g)=2H2O(g)△H=—484kJ/mol,则表中x=_____ 。
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

系统(Ⅰ)的热化学方程式为:H2O(l)=H2(g)+ O2(g)△H=
O2(g)△H=_____ ;系统(Ⅱ)的热化学方程式为:_____ 。
(3)工业上,常采用“加碳氯化”的方法以TiO2为原料生产TiCl4,相关反应为:
i、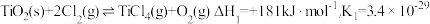
ii、
①TiO2(s)加炭氯化生成TiCl4(g)和CO(g)的热化学方程式为:_____ 。
②TiO2氯化过程中加碳的作用是为_____ 和_____ 。
(1)①如图表示某反应的能量变化关系图,该反应的△H=

②已知:2H2(g)+O2(g)=2H2O(g)△H=—484kJ/mol,则表中x=
| 化学键 | H—H | O=O | O—H |
| 键能(kJ∙mol-1) | 436 | x | 463 |

系统(Ⅰ)的热化学方程式为:H2O(l)=H2(g)+
 O2(g)△H=
O2(g)△H=(3)工业上,常采用“加碳氯化”的方法以TiO2为原料生产TiCl4,相关反应为:
i、
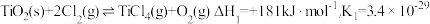
ii、

①TiO2(s)加炭氯化生成TiCl4(g)和CO(g)的热化学方程式为:
②TiO2氯化过程中加碳的作用是为
您最近一年使用:0次
3 . 凤凰石的主要成分为水合铜硅酸盐,还含有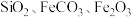 等杂质,以凤凰石为原料生产媒染剂无水
等杂质,以凤凰石为原料生产媒染剂无水 的工业流程如下:
的工业流程如下:
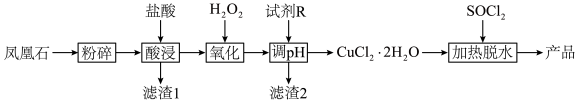
已知: ;
;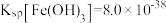 ;
;
回答下列问题:
(1)已知 是一种二元弱酸,则其第二步电离的方程式为
是一种二元弱酸,则其第二步电离的方程式为___________ ,常温下 的
的 溶液的
溶液的 约为
约为___________ (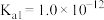 、
、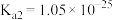 ),“氧化”步骤发生反应的离子方程式为
),“氧化”步骤发生反应的离子方程式为___________ 。
(2)加入“试剂R”调解溶液pH将溶液中铁元素转化为氢氧化物沉淀而除去,“试剂R”最好是___________(填字母)。
(3) 遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出
遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出 水解的化学方程式:
水解的化学方程式:___________ 。 脱水时
脱水时 可抑制
可抑制 的水解,其抑制原理主要包含两点:①
的水解,其抑制原理主要包含两点:① 与水反应减少了水的量;②
与水反应减少了水的量;②___________ 。
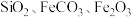 等杂质,以凤凰石为原料生产媒染剂无水
等杂质,以凤凰石为原料生产媒染剂无水 的工业流程如下:
的工业流程如下:
已知:
 ;
;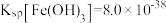 ;
;
回答下列问题:
(1)已知
 是一种二元弱酸,则其第二步电离的方程式为
是一种二元弱酸,则其第二步电离的方程式为 的
的 溶液的
溶液的 约为
约为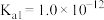 、
、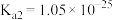 ),“氧化”步骤发生反应的离子方程式为
),“氧化”步骤发生反应的离子方程式为(2)加入“试剂R”调解溶液pH将溶液中铁元素转化为氢氧化物沉淀而除去,“试剂R”最好是___________(填字母)。
A. | B. | C. | D. |
(3)
 遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出
遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出 水解的化学方程式:
水解的化学方程式: 脱水时
脱水时 可抑制
可抑制 的水解,其抑制原理主要包含两点:①
的水解,其抑制原理主要包含两点:① 与水反应减少了水的量;②
与水反应减少了水的量;②
您最近一年使用:0次
4 . 已知常温下 的某一元酸
的某一元酸 溶液中
溶液中 ,下列叙述错误的是
,下列叙述错误的是
 的某一元酸
的某一元酸 溶液中
溶液中 ,下列叙述错误的是
,下列叙述错误的是A.常温下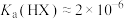 |
| B.加水稀释促进电离,溶液的pH减小 |
C.升高温度后, 均增大 均增大 |
D.加入少量NaOH固体,溶液中 减小但 减小但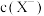 增大 增大 |
您最近一年使用:0次
名校
解题方法
5 . 下列仪器、pH试纸读数时,需要精确到0.01的是
 |  | 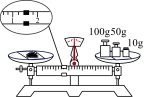 |  |
| A.滴定管 | B.量筒 | C.托盘天平 | D.广泛pH试纸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-12更新
|
34次组卷
|
2卷引用:黑龙江省海伦市第一中学2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
6 .  及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:
(1)基态铁原子的核外电子排布式为:______ , 比
比 更稳定的原因是:
更稳定的原因是:______ 。
(2) 中铁元素的配位数是
中铁元素的配位数是______ ,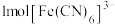 中含有的
中含有的 键的数目为
键的数目为______ , 中C原子的杂化方式为
中C原子的杂化方式为______ 。
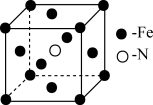
(3)铁和氨在 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:______ 。
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)______ 。

 及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:(1)基态铁原子的核外电子排布式为:
 比
比 更稳定的原因是:
更稳定的原因是:(2)
 中铁元素的配位数是
中铁元素的配位数是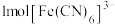 中含有的
中含有的 键的数目为
键的数目为 中C原子的杂化方式为
中C原子的杂化方式为(3)铁和氨在
 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出
 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)
您最近一年使用:0次
7 . 捕集 的技术对解决全球温室效应意义重大。回答下列问题:
的技术对解决全球温室效应意义重大。回答下列问题:
(1)国际空间站处理 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为: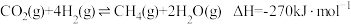 几种化学键的键能如表所示:
几种化学键的键能如表所示:
则a=______ 。
(2)将 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一,装置如图所示:
资源化利用的有效途径之一,装置如图所示:
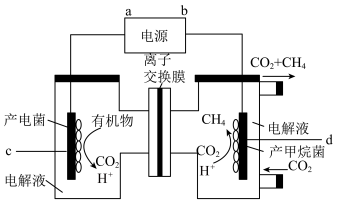
① 的移动方向为
的移动方向为______ (填“自左至右”或“自右至左”);d电极的电极反应式为______ 。
②若电源为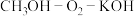 清洁燃料电池,当消耗
清洁燃料电池,当消耗 燃料
燃料 时,离子交换膜中通过
时,离子交换膜中通过______ 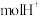 ,该清洁燃料电池中的正极反应式为
,该清洁燃料电池中的正极反应式为______ 。
(3)甲醇是一种可再生能源,由 制备甲醇的过程可能涉及的反应如下:
制备甲醇的过程可能涉及的反应如下:
反应Ⅰ: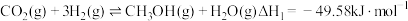
反应Ⅱ: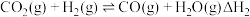
反应Ⅲ:
①反应Ⅱ的
______  。
。
②若反应Ⅱ在一恒温恒容密闭容器中进行,下面能说明反应已达到平衡状态的是______ 。
a.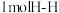 断裂的同时有
断裂的同时有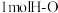 断裂
断裂
b.气体密度不变
c.平衡常数不变
d.容器内 保持不变
保持不变
 的技术对解决全球温室效应意义重大。回答下列问题:
的技术对解决全球温室效应意义重大。回答下列问题:(1)国际空间站处理
 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为: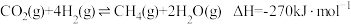 几种化学键的键能如表所示:
几种化学键的键能如表所示:化学键 |
|
|
|
|
键能/ | 413 | 436 | a | 745 |
(2)将
 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一,装置如图所示:
资源化利用的有效途径之一,装置如图所示:
①
 的移动方向为
的移动方向为②若电源为
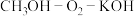 清洁燃料电池,当消耗
清洁燃料电池,当消耗 燃料
燃料 时,离子交换膜中通过
时,离子交换膜中通过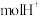 ,该清洁燃料电池中的正极反应式为
,该清洁燃料电池中的正极反应式为(3)甲醇是一种可再生能源,由
 制备甲醇的过程可能涉及的反应如下:
制备甲醇的过程可能涉及的反应如下:反应Ⅰ:
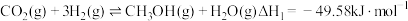
反应Ⅱ:
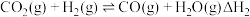
反应Ⅲ:

①反应Ⅱ的

 。
。②若反应Ⅱ在一恒温恒容密闭容器中进行,下面能说明反应已达到平衡状态的是
a.
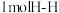 断裂的同时有
断裂的同时有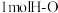 断裂
断裂b.气体密度不变
c.平衡常数不变
d.容器内
 保持不变
保持不变
您最近一年使用:0次
名校
解题方法
8 . 甲醇是重要的工业原料。
(1)已知CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ•mol-1。T℃下,向体积为2L的恒容密闭容器中充入2molCO2(g)和6molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图。
CH3OH(g)+H2O(g) △H=-49.0kJ•mol-1。T℃下,向体积为2L的恒容密闭容器中充入2molCO2(g)和6molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图。
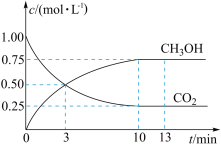
①T℃时,计算该反应的平衡常数为_______ (结果保留3位有效数字)。
②若保持温度和容器体积不变,13min时,向容器中充入1molCO2(g)和1molH2O(g),此时,该反应的v正_______ v逆(填“>”、“<”或=)。
③已知下列物质总键能(1mol物质所含化学键的键能之和)的数据如表,由此可计算表中a=_______ 。
(2)已知:(Ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1
(Ⅱ)CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.1kJ•mol-1
CO(g)+H2O(g) △H2=+41.1kJ•mol-1
(Ⅲ)2H2(g)+CO(g) CH3OH(g) △H3
CH3OH(g) △H3
①△H3=_______ kJ/mol。
②在一定温度下,已知反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为K1、K2、K3,则K3=________ (用K1、K2表示)。
(1)已知CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.0kJ•mol-1。T℃下,向体积为2L的恒容密闭容器中充入2molCO2(g)和6molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图。
CH3OH(g)+H2O(g) △H=-49.0kJ•mol-1。T℃下,向体积为2L的恒容密闭容器中充入2molCO2(g)和6molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图。
①T℃时,计算该反应的平衡常数为
②若保持温度和容器体积不变,13min时,向容器中充入1molCO2(g)和1molH2O(g),此时,该反应的v正
③已知下列物质总键能(1mol物质所含化学键的键能之和)的数据如表,由此可计算表中a=
| 物质 | CO2 | H2 | CH3OH | H2O |
| 总键能/kJ•mol | 1620 | a | 2047 | 930 |
 CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1(Ⅱ)CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.1kJ•mol-1
CO(g)+H2O(g) △H2=+41.1kJ•mol-1(Ⅲ)2H2(g)+CO(g)
 CH3OH(g) △H3
CH3OH(g) △H3①△H3=
②在一定温度下,已知反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为K1、K2、K3,则K3=
您最近一年使用:0次
名校
解题方法
9 . 工业上以 和
和 为原料可制备合成气(CO、
为原料可制备合成气(CO、 ),该反应的化学方程式为
),该反应的化学方程式为 。回答下列问题:
。回答下列问题:
(1)已知: 、
、 、CO的燃烧热分别为
、CO的燃烧热分别为 ,
, ,
, ,则
,则 的
的
_______ 。
(2)在1L恒温恒容密闭容器中充入 和
和 发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
_______  (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(3)已知在高温条件下,会发生如下副反应:
 ,且温度越高副反应的转化率越高。投料比
,且温度越高副反应的转化率越高。投料比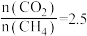 时温度变化对平衡时
时温度变化对平衡时 配比的影响如图所示。
配比的影响如图所示。
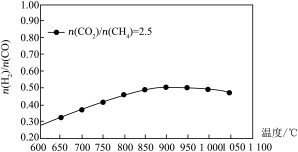
按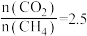 的配比进料,900℃以后,随温度升高,合成气
的配比进料,900℃以后,随温度升高,合成气 配比的变化规律是
配比的变化规律是_______ ;其原因可能是_______ 。
(4)工业上常利用生成的合成气制备甲醇( ),将CO和
),将CO和 通入某密闭容器中,只发生反应
通入某密闭容器中,只发生反应 ,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、
,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、 ,达到平衡时生成
,达到平衡时生成 。相同温度下,在乙容器中通入2mol CO、
。相同温度下,在乙容器中通入2mol CO、 ,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成
,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成 的物质的量为
的物质的量为_______ ;若乙的容积与甲的容积相等,乙中反应达到平衡时,生成 的物质的量
的物质的量_______ (填“大于”“小于”或“等于”) 。
。
 和
和 为原料可制备合成气(CO、
为原料可制备合成气(CO、 ),该反应的化学方程式为
),该反应的化学方程式为 。回答下列问题:
。回答下列问题:(1)已知:
 、
、 、CO的燃烧热分别为
、CO的燃烧热分别为 ,
, ,
, ,则
,则 的
的
(2)在1L恒温恒容密闭容器中充入
 和
和 发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
 (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。(3)已知在高温条件下,会发生如下副反应:

 ,且温度越高副反应的转化率越高。投料比
,且温度越高副反应的转化率越高。投料比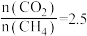 时温度变化对平衡时
时温度变化对平衡时 配比的影响如图所示。
配比的影响如图所示。
按
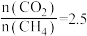 的配比进料,900℃以后,随温度升高,合成气
的配比进料,900℃以后,随温度升高,合成气 配比的变化规律是
配比的变化规律是(4)工业上常利用生成的合成气制备甲醇(
 ),将CO和
),将CO和 通入某密闭容器中,只发生反应
通入某密闭容器中,只发生反应 ,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、
,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、 ,达到平衡时生成
,达到平衡时生成 。相同温度下,在乙容器中通入2mol CO、
。相同温度下,在乙容器中通入2mol CO、 ,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成
,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成 的物质的量为
的物质的量为 的物质的量
的物质的量 。
。
您最近一年使用:0次
解题方法
10 . 金属钛(22Ti)号称航天材料。回答下列问题。
(1)基态钛原子的价层电子排布式为___________ ,它位于元素周期表的___________ 区。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是___________ 。
(3)TiX4的熔点如下表所示:
依F、Cl、Br、I次序,TiX4的化学键中离子键成分的百分数逐渐___________ (填“增强”、“减弱”或“不变”);分析TiCl4、TiBr4、TiI4的熔点呈现一定变化规律的原因是___________ 。
(1)基态钛原子的价层电子排布式为
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是
(3)TiX4的熔点如下表所示:
| TiF4 | TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
您最近一年使用:0次







