名校
1 . 下列分子结构图中的“○”表示氢原子,“●”表示短周期中相邻的三种元素原子。小黑点表示没有形成共价键的最外层电子,短线表示共价键。

(1)以上分子中,中心原子采用 杂化的是
杂化的是_____ (填化学式)。
(2)③的分子中有_____ 个 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的_____ 键(填“ ”或“
”或“ ),形成的是
),形成的是_____ 键(填“ ”或“
”或“ ”)。
”)。
(3)4种分子中,属于极性分子的是_____ (填序号,下同)。键角由大到小的顺序是_____ ,能结合质子(即 )形成稳定离子的是
)形成稳定离子的是_____ 。
(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为_____ 。

(1)以上分子中,中心原子采用
 杂化的是
杂化的是(2)③的分子中有
 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的 ”或“
”或“ ),形成的是
),形成的是 ”或“
”或“ ”)。
”)。(3)4种分子中,属于极性分子的是
 )形成稳定离子的是
)形成稳定离子的是(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为
您最近一年使用:0次
名校
2 . 研究电解质在水溶液中的离子反应与平衡有重的意义。有以下物质:①石墨②铜③酒精④氨水⑤二氧化碳⑥碳酸钠固体⑦氢氧化钡溶液⑧纯醋酸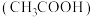 ⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
(1)其中能导电的是___________ ;属于非电解质的是___________ ;属于强电解质的是___________ :属于弱电解质的是___________ 。
(2)写出下列电解质在水溶液中的电离方程式:

___________ ;

___________ 。
稀氨水中存在下述平衡: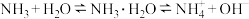 。
。
(3)常温下, 氨水的
氨水的
___________ 13(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(4)向氨水中加入 固体时,平衡
固体时,平衡___________ 移动(填“向左”、“向右”或“不移动”), 的浓度
的浓度___________ (填“减小”“增大”或“不变”)。
(5)常温下,用 盐酸溶液滴定
盐酸溶液滴定 氨水时,溶液中
氨水时,溶液中 变化曲线如图所示。结合图示,回答下列问题:
变化曲线如图所示。结合图示,回答下列问题:

①写出滴定过程中,反应的离子方程式___________ 。
②M点溶液中:
___________  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
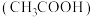 ⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。(1)其中能导电的是
(2)写出下列电解质在水溶液中的电离方程式:


稀氨水中存在下述平衡:
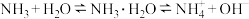 。
。(3)常温下,
 氨水的
氨水的
 ”、“
”、“ ”或“
”或“ ”)。
”)。(4)向氨水中加入
 固体时,平衡
固体时,平衡 的浓度
的浓度(5)常温下,用
 盐酸溶液滴定
盐酸溶液滴定 氨水时,溶液中
氨水时,溶液中 变化曲线如图所示。结合图示,回答下列问题:
变化曲线如图所示。结合图示,回答下列问题:
①写出滴定过程中,反应的离子方程式
②M点溶液中:

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
3 . 弱电解质在水溶液中存在多种平衡,它们在工农业生产中都有广泛的应用。
I.25℃时部分弱酸的电离平衡常数如下表:
(1)室温下五种溶液:① ②
② ③
③ ④
④ ⑤
⑤ 。上述溶液中水的电离被抑制的是
。上述溶液中水的电离被抑制的是___________ (填序号,下同),水的电离被促进的是___________ 。
(2)室温下等pH的① 、②
、② 、③
、③ 三种溶液,溶质的物质的量浓度由大到小的顺序是
三种溶液,溶质的物质的量浓度由大到小的顺序是___________ (填序号)。
(3)将少量 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是___________ 。
II.亚砷酸 可以用于治疗白血病。25℃,向
可以用于治疗白血病。25℃,向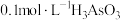 溶液中滴加
溶液中滴加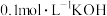 溶液,各种微粒的物质的量分数与溶液的关系如图所示。
溶液,各种微粒的物质的量分数与溶液的关系如图所示。

(4)人体血液的 在
在 ,患者用药后人体中含砷元素的主要微粒是
,患者用药后人体中含砷元素的主要微粒是___________ 。
(5)25℃,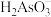 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是:___________ 。
(6)以酚酞为指示剂,将 溶液滴入
溶液滴入 溶液中,滴定终点的离子方程式是
溶液中,滴定终点的离子方程式是_______ 。
(7) 点溶液中:
点溶液中: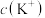
___________ 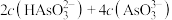 (选填“
(选填“ ”,“
”,“ ”或“
”或“ ”)
”)
(8)砷的化合物会影响人体代谢和免疫功能造成砷中毒。工业上采用化学沉降法处理含砷废水,将砷元素转化为 沉淀。则要除去
沉淀。则要除去 ,溶液中的
,溶液中的 至少为
至少为_____  。(已知:
。(已知: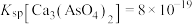 ,当残留在溶液中的离子浓度
,当残留在溶液中的离子浓度 ,可认为沉淀完全)。
,可认为沉淀完全)。
I.25℃时部分弱酸的电离平衡常数如下表:
| 弱酸 |  |  |  |
| 电离平衡常数 |  | 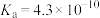 |  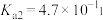 |
(1)室温下五种溶液:①
 ②
② ③
③ ④
④ ⑤
⑤ 。上述溶液中水的电离被抑制的是
。上述溶液中水的电离被抑制的是(2)室温下等pH的①
 、②
、② 、③
、③ 三种溶液,溶质的物质的量浓度由大到小的顺序是
三种溶液,溶质的物质的量浓度由大到小的顺序是(3)将少量
 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是II.亚砷酸
 可以用于治疗白血病。25℃,向
可以用于治疗白血病。25℃,向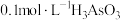 溶液中滴加
溶液中滴加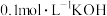 溶液,各种微粒的物质的量分数与溶液的关系如图所示。
溶液,各种微粒的物质的量分数与溶液的关系如图所示。
(4)人体血液的
 在
在 ,患者用药后人体中含砷元素的主要微粒是
,患者用药后人体中含砷元素的主要微粒是(5)25℃,
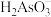 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是:(6)以酚酞为指示剂,将
 溶液滴入
溶液滴入 溶液中,滴定终点的离子方程式是
溶液中,滴定终点的离子方程式是(7)
 点溶液中:
点溶液中: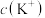
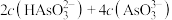 (选填“
(选填“ ”,“
”,“ ”或“
”或“ ”)
”)(8)砷的化合物会影响人体代谢和免疫功能造成砷中毒。工业上采用化学沉降法处理含砷废水,将砷元素转化为
 沉淀。则要除去
沉淀。则要除去 ,溶液中的
,溶液中的 至少为
至少为 。(已知:
。(已知: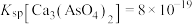 ,当残留在溶液中的离子浓度
,当残留在溶液中的离子浓度 ,可认为沉淀完全)。
,可认为沉淀完全)。
您最近一年使用:0次
名校
解题方法
4 . 下列说法不正确的是
| A.可以用新制氢氧化铜悬浊液区分蔗糖和麦芽糖 |
| B.用溴水可以鉴别苯酚溶液、2,4-己二烯、甲苯和苯 |
| C.HCl是共价化合物而NaCl是离子化合物,是因为H和Cl的电负性差小而Na与Cl电负性差大 |
| D.[Cu(NH3)4]SO4中含有离子键和配位键 |
您最近一年使用:0次
名校
解题方法
5 . 下列关于有机物说法正确的是
| A.卤代烃和醇均能在浓硫酸加热的条件下发生消去反应生成不饱和烃 |
| B.苯及其同系物以及苯酚都可以和溴水发生取代反应 |
| C.检验CH2=CHCHO中的两种官能团的操作是:先向待测液中加入银氨溶液加热,充分反应后冷却,再向冷却后的溶液中加入溴水 |
D.可用 和HCHO为原料合成 和HCHO为原料合成 |
您最近一年使用:0次
名校
6 . 某芳香烃X是一种重要的有机化工原料,质谱法测定其相对分子质量为92,现以它为初始原料设计出如下转化关系图。期中C、E互为同分异构体,且相对分子质量比X大34.5;A、B互为同分异构体,分子式为C7H7NO2。
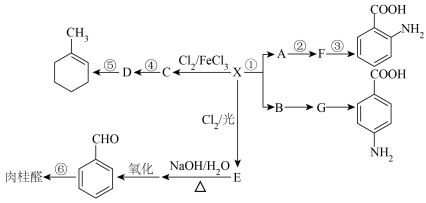
已知:Ⅰ.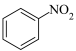
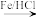
 (苯胺,易被氧化)
(苯胺,易被氧化)
Ⅱ.RCH2CHO+R′CHO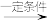
 +H2O
+H2O
(1)X的名称为___________ ,F的结构简式为___________ 。
(2)反应①的试剂条件为___________ ,反应③的类型为___________ 。
(3)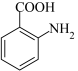 、
、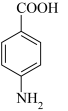 沸点较低的是
沸点较低的是___________ ,原因是___________ 。
(4)反应④两种反应物的物质的量之比为___________ 。
(5)反应⑤的方程式为___________ 。
(6)肉桂醛的结构简式为 ,请写出反应⑥的方程式
,请写出反应⑥的方程式___________ 。
(7)肉桂醛有多种同分异构体,符合下列三个条件的同分异构体共有___________ 种,写出其中核磁共振氢谱中有4个吸收峰的物质的结构简式___________ 。
①与FeCl3能发生显色反应 ②含碳碳三键 ③苯环上有两个取代基
(8)2-丁烯醛(CH3CH=CHCHO)广泛用于树脂生产和有机合成中。结合题中信息,以乙烯为原料,经过三步反应制得2-丁烯醛。CH2=CH2→M→N→CH3CH=CHCHO,写出中间产物M、N得结构简式。M___________ ;N___________ 。

已知:Ⅰ.

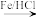
 (苯胺,易被氧化)
(苯胺,易被氧化)Ⅱ.RCH2CHO+R′CHO
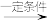
 +H2O
+H2O(1)X的名称为
(2)反应①的试剂条件为
(3)
 、
、 沸点较低的是
沸点较低的是(4)反应④两种反应物的物质的量之比为
(5)反应⑤的方程式为
(6)肉桂醛的结构简式为
 ,请写出反应⑥的方程式
,请写出反应⑥的方程式(7)肉桂醛有多种同分异构体,符合下列三个条件的同分异构体共有
①与FeCl3能发生显色反应 ②含碳碳三键 ③苯环上有两个取代基
(8)2-丁烯醛(CH3CH=CHCHO)广泛用于树脂生产和有机合成中。结合题中信息,以乙烯为原料,经过三步反应制得2-丁烯醛。CH2=CH2→M→N→CH3CH=CHCHO,写出中间产物M、N得结构简式。M
您最近一年使用:0次
7 . 下列实验能达到目的是
| 选项 | 反应及实验目的 | 检验试剂 |
| A | 溴乙烷和NaOH的乙醇溶液共热,证明发生了消去反应 | Br2的CCl4溶液 |
| B | 溴乙烷与NaOH溶液共热,检验溴元素 | AgNO3溶液 |
| C | 电石与饱和食盐水混合,检验乙炔气体 | 酸性KMnO4溶液 |
| D | 溴乙烷和NaOH的乙醇溶液共热,检验乙烯 | 酸性KMnO4溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 生产生活中常见各类有机物,部分有机物的结构与用途如下:
(1)根据有机物的组成与结构,判断上述有机物中属于烃类的是___________ ,存在顺反异构的是___________ 。
(2)有机物①用作燃料时发生反应的化学方程式是___________ 。
(3)利用有机物②合成橡胶时的步骤如下:

①物质B的结构简式是___________ 。
②过程ii的试剂a是___________ 。
③过程ii的反应类型是___________ 反应。
(4)有机物③含有的官能团是___________ 。有机物③作为酸味剂发挥作用时,断裂的化学键是(在下图中标出) __________ 。

(5)有机物④合成蛋白质时,自身反应生成二肽的结构简式是:___________ 。
(6)已知葡萄糖在溶液中存在链式和环式两种结构,且存在如下平衡:
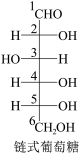

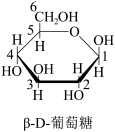
①β-D-葡萄糖是通过链式葡萄糖分子中___________ 和___________ (填官能团)通过___________ (填反应类型)反应而形成的。
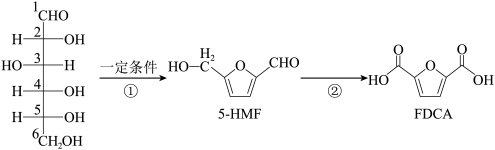
②利用葡萄糖可以合成FDCA,用于制造树脂,其合成路线如下:
下列说法正确的是___________ 。
a.①中发生了取代反应和消去反应
b.反应①说明了葡萄糖分子中多羟基的性质
c.反应②可以由5-HMF与银氨溶液直接反应获得
d.FDCA的分子式为C6H4O5
| HC≡CH焊接金属的燃料 |  合成橡胶的基础原料 | CH3CH(OH)COOH食品常用的酸味剂 | 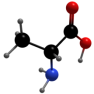 合成蛋白质原料 | 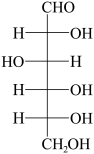 为机体供能,制造树脂 |
| ① | ② | ③ | ④ | ⑤ |
(1)根据有机物的组成与结构,判断上述有机物中属于烃类的是
(2)有机物①用作燃料时发生反应的化学方程式是
(3)利用有机物②合成橡胶时的步骤如下:

①物质B的结构简式是
②过程ii的试剂a是
③过程ii的反应类型是
(4)有机物③含有的官能团是

(5)有机物④合成蛋白质时,自身反应生成二肽的结构简式是:
(6)已知葡萄糖在溶液中存在链式和环式两种结构,且存在如下平衡:



①β-D-葡萄糖是通过链式葡萄糖分子中
②利用葡萄糖可以合成FDCA,用于制造树脂,其合成路线如下:

下列说法正确的是
a.①中发生了取代反应和消去反应
b.反应①说明了葡萄糖分子中多羟基的性质
c.反应②可以由5-HMF与银氨溶液直接反应获得
d.FDCA的分子式为C6H4O5
您最近一年使用:0次
名校
9 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
I. 破坏臭氧层的机理为:
破坏臭氧层的机理为:
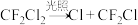
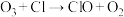

(1)活性氯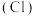 的作用是
的作用是___________ 。
(2)下列关于氟利昂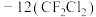 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有___________ 。
A.两种氟利昂在 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应
B.两种氟利昂均不存在同分异构体
C.直接用 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素
II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如: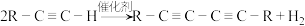 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
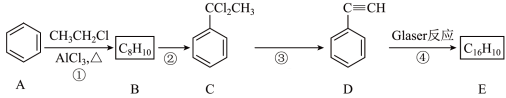
请回答下列问题:
(3)步骤①的反应类型为___________ ,步骤②的试剂和条件为___________ ,D的名称为___________ 。
(4)写出步骤③反应的化学方程式:___________ 。
(5)E的结构简式为___________ 。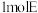 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
___________  。
。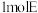 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
___________  。
。
(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为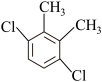
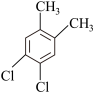
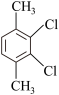
___________ 、___________ 。
(7)设计一条以环己醇(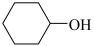 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成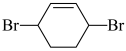 的合成路线
的合成路线_________ 。
(合成路线常用的表示方式为: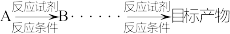 )
)
I.
 破坏臭氧层的机理为:
破坏臭氧层的机理为: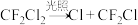
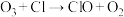

(1)活性氯
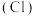 的作用是
的作用是(2)下列关于氟利昂
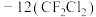 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有A.两种氟利昂在
 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应B.两种氟利昂均不存在同分异构体
C.直接用
 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如:
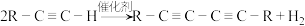 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
请回答下列问题:
(3)步骤①的反应类型为
(4)写出步骤③反应的化学方程式:
(5)E的结构简式为
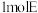 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
 。
。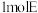 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
 。
。(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为
 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为


(7)设计一条以环己醇(
 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成 的合成路线
的合成路线(合成路线常用的表示方式为:
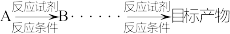 )
)
您最近一年使用:0次
名校
解题方法
10 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属键本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
250次组卷
|
3卷引用:北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷



