名校
解题方法
1 . 三聚氰胺曾引起奶粉事件,它是一种重要化工原料,其结构简式如图所示,下列有关说法正确的是

| A.分子中既有极性键又有非极性键 |
B.分子中采用 杂化的原子有3个 杂化的原子有3个 |
| C.该物质分子间的作用力有范德华力、氢键 |
D.该物质中原子的第一电离能大小: |
您最近一年使用:0次
2 . 最近中外科学家团队共同合成了T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子构成的正四面体结构单元取代,形成碳的一种新型三维立体晶体结构,如图所示(图中的●表示碳形成的正四面体结构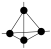 )。已知T-碳晶胞参数为
)。已知T-碳晶胞参数为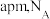 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
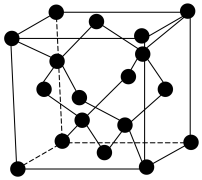
| A.每个T-碳晶胞中含8个碳原子 | B.T-碳中 键的最小夹角约为 键的最小夹角约为 |
| C.T-碳属于分子晶体 | D.T-碳的密度为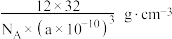 |
您最近一年使用:0次
名校
3 . 二茂铁 的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究思维新领域。已知二茂铁的熔点是
的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究思维新领域。已知二茂铁的熔点是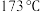 (在
(在 以上能升华),沸点是
以上能升华),沸点是 ,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法正确的是
,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法正确的是
 的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究思维新领域。已知二茂铁的熔点是
的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究思维新领域。已知二茂铁的熔点是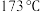 (在
(在 以上能升华),沸点是
以上能升华),沸点是 ,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法正确的是
,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法正确的是A.在二茂铁中, 与 与 之间形成的化学键类型是离子键 之间形成的化学键类型是离子键 |
| B.二茂铁属于离子晶体 |
C. 中 中 键和π键个数之比为 键和π键个数之比为 |
D.已知环戊二烯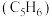 的结构式为 的结构式为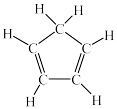 ,则分子环戊二烯中有2个碳原子采用 ,则分子环戊二烯中有2个碳原子采用 杂化 杂化 |
您最近一年使用:0次
4 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:(已知: 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)
(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为___________ ;配合物 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是___________ (填元素符号)。
(2)现有下列实验:___________ ,溶剂X可以是___________ (填名称),继续添加氨水,沉淀溶解的离子方程式为___________ 。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是___________ 。
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为
 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是(2)现有下列实验:

②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 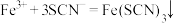 |
| B | 向由0.1mol CrCl3∙6H2O配成的溶液中加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知Cr3+的配位数为6,则CrCl3∙6H2O的化学式可表示为 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在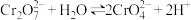 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
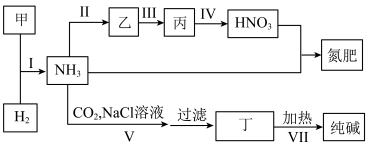
5 . 合成氨及其相关工业中,部分物质间的转化关系如图所示。回答下列问题: 的电子式:
的电子式:___________ ,反应I的化学方程式为___________ 。
(2)写出反应Ⅳ的离子方程式:___________ 。
(3)反应Ⅵ产生的___________ (填化学式)可以在流程V中被循环利用。
(4)硝酸是无色、易挥发、有刺激性气味的液体。浓硝酸一般将其保存在棕色试剂瓶中,并放置在阴凉处,说明浓硝酸具有___________ 性,用化学方程式表示该操作的原因:___________ 。
(5)乙是污染性气体,可以在催化剂加热条件下用 来处理,生成对环境没有污染的产物,写出用
来处理,生成对环境没有污染的产物,写出用 处理乙的化学方程式:
处理乙的化学方程式:___________ 。
 的电子式:
的电子式:(2)写出反应Ⅳ的离子方程式:
(3)反应Ⅵ产生的
(4)硝酸是无色、易挥发、有刺激性气味的液体。浓硝酸一般将其保存在棕色试剂瓶中,并放置在阴凉处,说明浓硝酸具有
(5)乙是污染性气体,可以在催化剂加热条件下用
 来处理,生成对环境没有污染的产物,写出用
来处理,生成对环境没有污染的产物,写出用 处理乙的化学方程式:
处理乙的化学方程式:
您最近一年使用:0次
6 . 硝基胍是固体火箭推进剂的重要组分,其结构简式如图所示。
(1)硝基胍分子中含有的共价键类型为___________ (从成键方式角度考虑)。
(2)硝基胍分子中C、H、O、N四种元素,这四种元素___________ (填“能”或“不能”)形成离子化合物。
(3)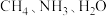 三种分子的中心原子杂化类型相同,但键角大小为
三种分子的中心原子杂化类型相同,但键角大小为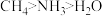 ,原因是
,原因是___________ 。
(4)硝基胍中N原子的杂化方式为___________ 。从结构上分析硝基胍___________ (填“易”或“不”)溶于水,原因是___________ 。
(5)下图中表示的碳原子能量最高的是___________(填字母)。

(1)硝基胍分子中含有的共价键类型为
(2)硝基胍分子中C、H、O、N四种元素,这四种元素
(3)
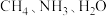 三种分子的中心原子杂化类型相同,但键角大小为
三种分子的中心原子杂化类型相同,但键角大小为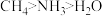 ,原因是
,原因是(4)硝基胍中N原子的杂化方式为
(5)下图中表示的碳原子能量最高的是___________(填字母)。
A.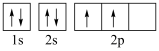 | B.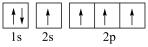 |
C.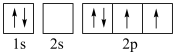 | D.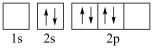 |
您最近一年使用:0次
名校
解题方法
7 . 根据原电池原理,回答下列问题:
(1)铜锌原电池的装置如图所示:___________ (填“正极”或“负极”),溶液中的 向
向___________ (填“铁”或“铜”)电极方向移动。
②负极的电极反应式为___________ 。
③若反应过程中有 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为___________  。
。
(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
已知:实验均为常温下完成;电流计指针偏转方向为正极方向。
①实验3中, 为
为___________ 极,电极反应式为___________ 。
②实验4中, 为
为___________ 极,电池总反应的离子方程式是___________ 。
③根据实验结果总结出影响铝在电池中做正极或负极的因素有___________ 。
(1)铜锌原电池的装置如图所示:

 向
向②负极的电极反应式为
③若反应过程中有
 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为 。
。(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | 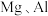 | 稀盐酸 | 偏向 |
| 2 | 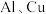 | 稀盐酸 | 偏向 |
| 3 | 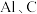 (石墨) (石墨) | 稀盐酸 | 偏向石墨 |
| 4 | 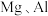 |  溶液 溶液 | 偏向 |
| 5 | 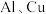 | 浓硝酸 | 偏向 |
①实验3中,
 为
为②实验4中,
 为
为③根据实验结果总结出影响铝在电池中做正极或负极的因素有
您最近一年使用:0次
名校
8 . 某元素X的逐级电离能如图所示,下列说法正确的是

| A.X元素最外层有5个电子 | B.X最可能生成的阳离子为 |
| C.X元素属于s区 | D.X一定为金属元素 |
您最近一年使用:0次
名校
解题方法
9 . 制备纯二氧化硅工艺流程如下图所示,下列说法错误的是

| A.X可用作木材防火剂 | B.步骤Ⅱ的硫酸可以用 替代 替代 |
C. 不与任何酸反应 不与任何酸反应 | D.步骤Ⅲ一般在坩埚中进行 |
您最近一年使用:0次
10 . 如下图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是
| 甲 | 乙 | ||
| A |  和浓盐酸 和浓盐酸 |  溶液和 溶液和 |
|
| B |  和浓硫酸 和浓硫酸 |  和稀硝酸 和稀硝酸 | |
| C |  和稀硫酸 和稀硫酸 |  和水 和水 | |
| D |  和稀硝酸 和稀硝酸 |  溶液和稀盐酸 溶液和稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-03更新
|
118次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高一下学期4月期中考试化学试题




