名校
解题方法
1 . 以硫酸工业的尾气 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示:
(1)反应I的化学方程式为___________ 。
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有___________ 。
(3)反应Ⅲ所得的 可在反应
可在反应___________ (填“I”、“Ⅱ”或“Ⅳ”)中重复使用,检验滤液中阳离子的操作方法是___________ 。
(4)已知 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为___________ ,当生成的无污染性气体体积为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为___________ 。
(5)将一定比例的氢气和二氧化硫以一定流速通过装有 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:___________ 。
 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示: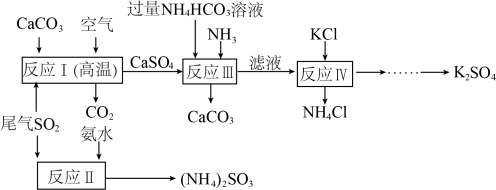
(1)反应I的化学方程式为
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有
(3)反应Ⅲ所得的
 可在反应
可在反应(4)已知
 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为(5)将一定比例的氢气和二氧化硫以一定流速通过装有
 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式: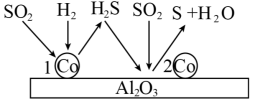
您最近一年使用:0次
2 . 有机化合物 可由葡萄糖发酵得到,在医药和食品领域中有广泛应用,研究化合物
可由葡萄糖发酵得到,在医药和食品领域中有广泛应用,研究化合物 的分子结构,性质如下:
的分子结构,性质如下:
(1)确定 的分子式
的分子式
经元素分析得到化合物 的实验式为
的实验式为 ,通过
,通过___________ 法(填仪器分析方法)可以测得 的相对分子质量为90,则A的分子式为
的相对分子质量为90,则A的分子式为___________ 。
(2)确定 的分子结构
的分子结构
使用现代分析仪器对 的分子结构进行测定,结果如表:
的分子结构进行测定,结果如表:
通过以上分析 的结构简式为
的结构简式为___________ 。
(3)研究 的结构和性质的关系
的结构和性质的关系
①A的分子存在两种空间结构,它们具有完全相同的组成和原子排列,却互为镜像,具有不同的光学性质,两种分子的关系为___________ (填字母,下同)。
A.碳架异构 B.位置异构 C.手性异构 D.官能闭异构
②已知 的酸性强于丙酸的,请从共价键极性和基团间相互影响的角度解释原因
的酸性强于丙酸的,请从共价键极性和基团间相互影响的角度解释原因___________ 。
(4)除了葡萄糖发酵可以制得A, 和
和 等在一定条件下也可以合成A,一种合成路线如图:
等在一定条件下也可以合成A,一种合成路线如图: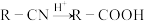 。
。
①写出 和
和 反应生成
反应生成 的化学方程式
的化学方程式___________ 。
② 的结构简式为
的结构简式为___________ 。
(5)A在浓硫酸、加热条件下反应生成含有六元环的有机化合物 ,写出
,写出 的结构简式
的结构简式___________ 。
 可由葡萄糖发酵得到,在医药和食品领域中有广泛应用,研究化合物
可由葡萄糖发酵得到,在医药和食品领域中有广泛应用,研究化合物 的分子结构,性质如下:
的分子结构,性质如下:(1)确定
 的分子式
的分子式经元素分析得到化合物
 的实验式为
的实验式为 ,通过
,通过 的相对分子质量为90,则A的分子式为
的相对分子质量为90,则A的分子式为(2)确定
 的分子结构
的分子结构使用现代分析仪器对
 的分子结构进行测定,结果如表:
的分子结构进行测定,结果如表:| 谱图 | 数据分析结果 | |
| 红外光谱 |
| 含有: 、 、 |
| 核磁共振氢谱 |
| 峰面积比为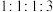 |
 的结构简式为
的结构简式为(3)研究
 的结构和性质的关系
的结构和性质的关系①A的分子存在两种空间结构,它们具有完全相同的组成和原子排列,却互为镜像,具有不同的光学性质,两种分子的关系为
A.碳架异构 B.位置异构 C.手性异构 D.官能闭异构
②已知
 的酸性强于丙酸的,请从共价键极性和基团间相互影响的角度解释原因
的酸性强于丙酸的,请从共价键极性和基团间相互影响的角度解释原因(4)除了葡萄糖发酵可以制得A,
 和
和 等在一定条件下也可以合成A,一种合成路线如图:
等在一定条件下也可以合成A,一种合成路线如图:
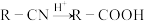 。
。①写出
 和
和 反应生成
反应生成 的化学方程式
的化学方程式②
 的结构简式为
的结构简式为(5)A在浓硫酸、加热条件下反应生成含有六元环的有机化合物
 ,写出
,写出 的结构简式
的结构简式
您最近一年使用:0次
名校
3 . 近日,济南大学原长洲教授制备了一种高性能的钾离子电池负极材料(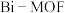 ),反应可简单表示为
),反应可简单表示为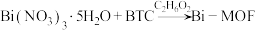 。回答下列问题:
。回答下列问题:
(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为___________ 。 中阴离子的立体构型为
中阴离子的立体构型为___________ 。基态O原子核外成对电子数与未成对电子数之比为___________ 。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为___________ 。 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
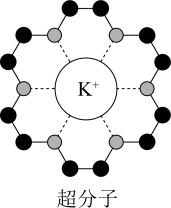
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。 原子的杂化类型为
原子的杂化类型为___________ 。
②下列叙述正确的是___________ (填字母)。
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成氢键
(4)该电池负极材料(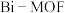 )充电时,会形成钾铋合金
)充电时,会形成钾铋合金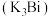 ,其晶胞结构如图,已知该晶胞底边长为
,其晶胞结构如图,已知该晶胞底边长为 ,高为
,高为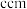 ,
, 为阿伏伽德罗常数的值。该晶体密度
为阿伏伽德罗常数的值。该晶体密度___________  (只列计算式)。
(只列计算式)。
 ),反应可简单表示为
),反应可简单表示为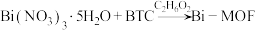 。回答下列问题:
。回答下列问题:(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为
 中阴离子的立体构型为
中阴离子的立体构型为(2)BTC分子中组成元素C、N、O的电负性由大到小排序为
 的沸点高于
的沸点高于 ,原因是
,原因是(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。
 原子的杂化类型为
原子的杂化类型为②下列叙述正确的是
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成氢键
(4)该电池负极材料(
 )充电时,会形成钾铋合金
)充电时,会形成钾铋合金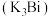 ,其晶胞结构如图,已知该晶胞底边长为
,其晶胞结构如图,已知该晶胞底边长为 ,高为
,高为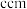 ,
, 为阿伏伽德罗常数的值。该晶体密度
为阿伏伽德罗常数的值。该晶体密度 (只列计算式)。
(只列计算式)。
您最近一年使用:0次
名校
4 .  主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含 、
、 ,还含有少量的
,还含有少量的 、
、 ,
, 、
、 、
、 )制备氧化钴
)制备氧化钴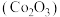 的工艺流程如图所示。
的工艺流程如图所示。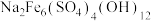 ;②金属钴与铁具有相似的化学性质;③氧化性
;②金属钴与铁具有相似的化学性质;③氧化性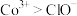 。
。
回答下列问题:
(1)钴元素基态原子的电子排布式为___________ 。
(2)“酸浸”时滤渣的主要成分为___________ (填化学式)。
(3)“除铁”时加入 溶液,
溶液, 的电子式为
的电子式为___________ 。
(4) 在空气中加热煅烧得到
在空气中加热煅烧得到 的化学方程式为
的化学方程式为___________ 。
(5)①钴被称为无机配合物之王,配合物 的中心离子的配位数为
的中心离子的配位数为___________ ,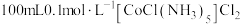 溶液中加入足量
溶液中加入足量 溶液,生成
溶液,生成___________ 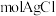 。
。
②钴的一种化合物的晶胞结构如图所示。 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
 主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含 、
、 ,还含有少量的
,还含有少量的 、
、 ,
, 、
、 、
、 )制备氧化钴
)制备氧化钴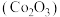 的工艺流程如图所示。
的工艺流程如图所示。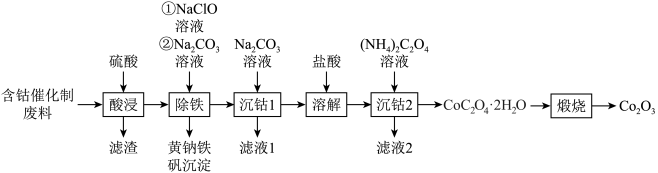
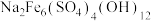 ;②金属钴与铁具有相似的化学性质;③氧化性
;②金属钴与铁具有相似的化学性质;③氧化性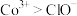 。
。回答下列问题:
(1)钴元素基态原子的电子排布式为
(2)“酸浸”时滤渣的主要成分为
(3)“除铁”时加入
 溶液,
溶液, 的电子式为
的电子式为(4)
 在空气中加热煅烧得到
在空气中加热煅烧得到 的化学方程式为
的化学方程式为(5)①钴被称为无机配合物之王,配合物
 的中心离子的配位数为
的中心离子的配位数为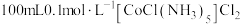 溶液中加入足量
溶液中加入足量 溶液,生成
溶液,生成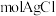 。
。②钴的一种化合物的晶胞结构如图所示。
 周围与其最近的
周围与其最近的 的个数为
的个数为
您最近一年使用:0次
5 . 2,6-二溴吡啶是合成阿伐斯汀(抗组胺药)中间体,实验室制备过程如下:
步骤2:反应完毕,利用如图装置回收乙酸。
步骤3:冷却至室温,析出晶体,过滤。母液回收溶剂,冷却,析出晶体,过滤,合并两次晶体,空气干燥。
已知:乙酸、2,6-二氯吡啶、2,6-二溴吡啶的沸点依次为117.9℃、206℃、249℃。油浴温度:100~250℃;砂浴温度:220~350℃。
下列叙述错误的是
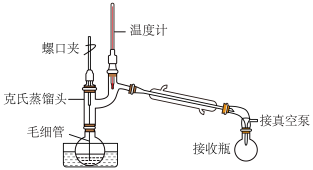
步骤2:反应完毕,利用如图装置回收乙酸。
步骤3:冷却至室温,析出晶体,过滤。母液回收溶剂,冷却,析出晶体,过滤,合并两次晶体,空气干燥。
已知:乙酸、2,6-二氯吡啶、2,6-二溴吡啶的沸点依次为117.9℃、206℃、249℃。油浴温度:100~250℃;砂浴温度:220~350℃。
下列叙述错误的是
| A.步骤1中采用“油浴”加热三颈烧瓶 | B.如图装置中毛细管起防暴沸和搅拌作用 |
| C.接收瓶最先收集到2,6-二溴吡啶 | D.实验中乙酸作溶剂,回收可循环利用 |
您最近一年使用:0次
2024-06-05更新
|
321次组卷
|
3卷引用:甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题
名校
6 . 甲基丙烯酸甲酯是合成有机玻璃的单体,可用如下方法合成:
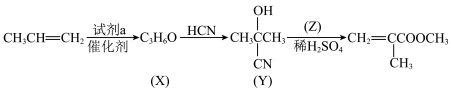
A.试剂a是酸性 溶液 溶液 | B.有机物X不易溶于水 |
C.有机物Z是 | D.催化剂 反应前后质量不变 反应前后质量不变 |
您最近一年使用:0次
2024-06-04更新
|
309次组卷
|
2卷引用:2024届甘肃省白银市靖远县第一中学高三下学期模拟预测化学试题
名校
7 . 冰晶石(Ng3AlF6)是电解铝工业的助熔剂、制造乳白色玻璃和搪瓷的遮光剂。制取冰晶石的反应为 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是
 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是A.基态Al原子的价层电子轨道表示式: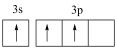 |
B.CO2的电子式: |
C.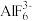 的结构式: 的结构式: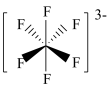 |
D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
2024-06-04更新
|
226次组卷
|
3卷引用:甘肃省兰州市第二中学2023-2024学年高三下学期第十次月考化学试题
名校
解题方法
8 . 下列关于分子的结构和性质的描述中正确的是
| A.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
B.邻羟基苯甲醛(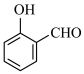 )的沸点低于对羟基苯甲醛( )的沸点低于对羟基苯甲醛(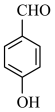 ),是由于对羟基苯甲醛分子间范德华力更强 ),是由于对羟基苯甲醛分子间范德华力更强 |
C.乳酸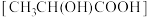 分子不是手性分子 分子不是手性分子 |
D. 的极性比 的极性比 的极性强,因此酸性: 的极性强,因此酸性: |
您最近一年使用:0次
9 . 中科院大连化学物理研究所科学家用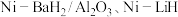 等作催化剂,实现了在常压、
等作催化剂,实现了在常压、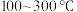 的条件下合成氨,这一成果发表在
的条件下合成氨,这一成果发表在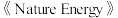 杂志上。
杂志上。
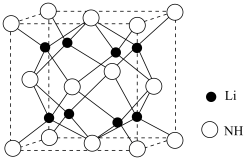
(1)基态Ni2+的价层电子的轨道表示式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸 是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸中C原子的杂化方式为___________ ,晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)NH3分子中的键角为107°,但在 中NH3分子的键角如图所示,导致这种变化的原因是
中NH3分子的键角如图所示,导致这种变化的原因是___________ 。___________ mol-1 (列出表达式)。
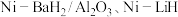 等作催化剂,实现了在常压、
等作催化剂,实现了在常压、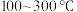 的条件下合成氨,这一成果发表在
的条件下合成氨,这一成果发表在 杂志上。
杂志上。(1)基态Ni2+的价层电子的轨道表示式为
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸
 是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
是组成最简单的氨基酸,熔点为182℃,沸点为233℃。①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸中C原子的杂化方式为
(3)NH3分子中的键角为107°,但在
 中NH3分子的键角如图所示,导致这种变化的原因是
中NH3分子的键角如图所示,导致这种变化的原因是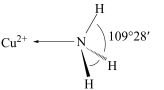
您最近一年使用:0次
解题方法
10 .  可用于有机合成、制氯醋酸及硫酸,T℃时,往恒容密闭容器中加入
可用于有机合成、制氯醋酸及硫酸,T℃时,往恒容密闭容器中加入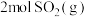 和
和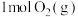 ,发生反应生成
,发生反应生成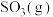 ,下列说法正确的是
,下列说法正确的是
 可用于有机合成、制氯醋酸及硫酸,T℃时,往恒容密闭容器中加入
可用于有机合成、制氯醋酸及硫酸,T℃时,往恒容密闭容器中加入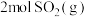 和
和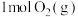 ,发生反应生成
,发生反应生成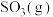 ,下列说法正确的是
,下列说法正确的是| A.当容器内的压强不再改变时,反应达到平衡状态 |
B.使用合适的催化剂,可以使 全部转化为 全部转化为 |
C.某时刻.容器内可能含有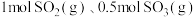 |
D.反应达到平衡时,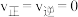 |
您最近一年使用:0次





