1 . 抗炎药物双氯芬酸的分子结构如图所示,下列说法正确的是
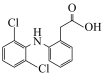
A.该分子的分子式为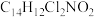 |
| B.该分子与足量氢气加成后有五个手性碳原子 |
| C.该分子可发生取代、加成、消去反应 |
| D.1mol该分子可以与5molNaOH在一定条件下发生反应 |
您最近一年使用:0次
2 . 下列对某溶液中离子检验的方法、现象与结论的描述中,均正确的是
A.取某溶液少量,加入足量盐酸无现象,再加入几滴氯化钡溶液,有白色沉淀,说明原溶液中有 |
| B.取某溶液少量,进行焰色反应,观察到火焰呈黄色,说明原溶液一定是钠盐溶液 |
C.取某无机盐溶液少量,加烧碱溶液并加热,生成使蓝色石蕊试纸变红的气体说明原溶液中有 |
D.加入 溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 存在 存在 |
您最近一年使用:0次
3 . 下列有关实验的说法不正确 的是

| A.利用图①装置可以测算高锰酸钾与草酸反应的速率 |
| B.利用图②的实验操作可观察到钾元素的焰色为紫色 |
| C.利用图③装置可以使用二氧化锰与稀盐酸制备氯气 |
| D.利用图④装置测量乙酸标准溶液的pH值,可以获得乙酸的电离平衡常数 |
您最近一年使用:0次
4 . 根据实验目的设计方案并进行实验,观察到相关现象。其中方案设计或结论均正确的是
| 实验目的 | 实验方案 | 现象 | 结论 | |
| A | 检验Na2SO3固体是否变质 | 将Na2SO3固体溶于水加入少量酸性KMnO4溶液 | 最终溶液无色 | Na2SO3固体未变质 |
| B | 检验木炭与浓硫酸共热后的酸性气体 | 将木炭与浓硫酸加热反应后的气体依次通过品红溶液、澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 木炭与浓硫酸加热反应后的气体中有SO2和CO2 |
| C | 探究1-溴丁烷消去后的有机产物 | 将2.0g NaOH、15mL无水乙醇、5mL 1-溴丁烷和碎瓷片共热后的气体直接通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 1-溴丁烷消去后有不饱和烃生成 |
| D | 探究浓度对化学平衡的影响 | 向5mL 0.005mol/L FeCl3溶液中加入5mL 0.015mol/L KSCN溶液,振荡后再加入4滴1mol/LKSCN溶液 | 溶液红色变深 | 增大反应物浓度,平衡向正方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z、N是原子序数依次增大的5种短周期主族元素。W电子只有一种自旋方向;X原子核外s能级电子总数与p能级相同且第一电离能都低于同周期相邻元素;Y第一电离能都高于同周期相邻元素;Z价电子中,不同形状的原子轨道中运动的电子数相等;N只有一个未成对电子。下列说法不正确 的是
A.还原性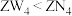 | B.原子半径Y>Z>X |
| C.电负性X>N>W | D.同周期中比X第一电离能大的元素共有3种 |
您最近一年使用:0次
6 . 三氯化六氨合钴 是一种重要的化工产品,实验室用
是一种重要的化工产品,实验室用 氧化
氧化 溶液制备
溶液制备 ,其化学方程式为
,其化学方程式为
 。下列叙述错误的是
。下列叙述错误的是
 是一种重要的化工产品,实验室用
是一种重要的化工产品,实验室用 氧化
氧化 溶液制备
溶液制备 ,其化学方程式为
,其化学方程式为
 。下列叙述错误的是
。下列叙述错误的是A. 、 、 的空间结构相同 的空间结构相同 |
B. 分子中含有极性和非极性共价键 分子中含有极性和非极性共价键 |
C.1 mol 中含6 mol配位键 中含6 mol配位键 |
D. 和 和 分别与 分别与 的配位能力: 的配位能力: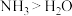 |
您最近一年使用:0次
7 . 从钒铬锰矿渣(主要成分为V2O5、Cr2O3、MnO)中提铬的一种工艺流程如下:
下列说法错误的是

下列说法错误的是
| A.Cr元素位于元素周期表第四周期 VIB 族 |
| B.“沉钒”过程利用了 Fe(OH)3(胶体)的吸附性,使含钒微粒与胶体共沉降 |
| C.“转化”过程中生成MnO2的离子方程式为Mn2++H2O2+2OH-=MnO2+2H2O |
| D.“提纯”过程中Na2S2O3的作用是还原含铬元素的物质 |
您最近一年使用:0次
8 .  是一种钠离子电池正极材料,充、放电过程中正极材料立方晶胞示意图的组成变化如图所示,晶胞内未标出因放电产生的0价
是一种钠离子电池正极材料,充、放电过程中正极材料立方晶胞示意图的组成变化如图所示,晶胞内未标出因放电产生的0价 。
。 呈黄色,
呈黄色, 呈绿色,
呈绿色, 呈蓝色等;预测
呈蓝色等;预测 呈
呈_______ 色,原因是_______ 。
(2) 可以形成多种配合物,其中的甘氨酸铜对于预防和治疗贫血、骨质疏松等疾病具有一定的作用,它有顺式和反式两种同分异构体,结构如图。
可以形成多种配合物,其中的甘氨酸铜对于预防和治疗贫血、骨质疏松等疾病具有一定的作用,它有顺式和反式两种同分异构体,结构如图。_______ (填“ ”或“
”或“ ”)。
”)。
(3)充电时,每个 晶胞完全转化为
晶胞完全转化为 晶胞。每个
晶胞。每个 晶胞中
晶胞中 个数为
个数为_______ (用含 的代数式作答)。当
的代数式作答)。当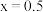 时,
时,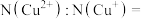
_______ 。 晶胞中互不相邻的
晶胞中互不相邻的 围成的空间结构是
围成的空间结构是_______ 。
(4) 可以与稀硫酸反应生成
可以与稀硫酸反应生成 ,比较
,比较 和
和 键角的大小:
键角的大小: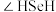
_______ (填“>”或“<”)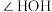 ,说明原因:
,说明原因:_______ 。
(5)立方 晶胞的晶胞参数为
晶胞的晶胞参数为 ,该晶胞的密度为
,该晶胞的密度为_______  (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 是一种钠离子电池正极材料,充、放电过程中正极材料立方晶胞示意图的组成变化如图所示,晶胞内未标出因放电产生的0价
是一种钠离子电池正极材料,充、放电过程中正极材料立方晶胞示意图的组成变化如图所示,晶胞内未标出因放电产生的0价 。
。
 呈黄色,
呈黄色, 呈绿色,
呈绿色, 呈蓝色等;预测
呈蓝色等;预测 呈
呈(2)
 可以形成多种配合物,其中的甘氨酸铜对于预防和治疗贫血、骨质疏松等疾病具有一定的作用,它有顺式和反式两种同分异构体,结构如图。
可以形成多种配合物,其中的甘氨酸铜对于预防和治疗贫血、骨质疏松等疾病具有一定的作用,它有顺式和反式两种同分异构体,结构如图。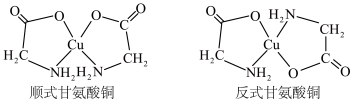
 ”或“
”或“ ”)。
”)。(3)充电时,每个
 晶胞完全转化为
晶胞完全转化为 晶胞。每个
晶胞。每个 晶胞中
晶胞中 个数为
个数为 的代数式作答)。当
的代数式作答)。当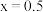 时,
时,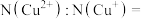
 晶胞中互不相邻的
晶胞中互不相邻的 围成的空间结构是
围成的空间结构是(4)
 可以与稀硫酸反应生成
可以与稀硫酸反应生成 ,比较
,比较 和
和 键角的大小:
键角的大小: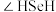
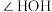 ,说明原因:
,说明原因:(5)立方
 晶胞的晶胞参数为
晶胞的晶胞参数为 ,该晶胞的密度为
,该晶胞的密度为 (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
9 . 设 表示阿伏加德罗常数的数值,下列说法正确的是
表示阿伏加德罗常数的数值,下列说法正确的是
 表示阿伏加德罗常数的数值,下列说法正确的是
表示阿伏加德罗常数的数值,下列说法正确的是A.标准状况下,含有 个氦原子的氦气体积约为 个氦原子的氦气体积约为 |
B.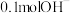 含 含 个电子 个电子 |
C.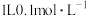 的 的 溶液中, 溶液中, 的数目为 的数目为 |
D.标准状况下, 氟化氢所含的分子数为 氟化氢所含的分子数为 |
您最近一年使用:0次
10 . 中国幅员辽阔,有丰富的金、银、铜、铅等矿产资源。根据所学知识回答下列问题:
(1)已知金的价电子排布式为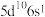 ,则其位于元素周期表
,则其位于元素周期表___________ 区。
(2)某种配合物结构如图(H原子未给出)。___________ (填元素符号)。
②该配合物中N、O、S三种元素的第一电离能由大到小的顺序为___________ 。
③该配合物中键角∠O—S—O___________ (填“>”“<”或“=”)∠C—N—C。
(3)铜及其化合物常用作催化剂,如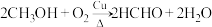 。
。
① 分子中O原子的杂化轨道类型为
分子中O原子的杂化轨道类型为___________ 。
② 易溶于水,原因是
易溶于水,原因是___________ 、___________ 。
③ 的立体构型为
的立体构型为___________ ,其分子中含有的 键与
键与 键数目之比为
键数目之比为___________ 。
(4)Pb、S形成的某种晶体结构示意图如图,设晶胞参数为a pm, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。___________ 。
②该晶体的密度为___________  。
。
(1)已知金的价电子排布式为
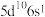 ,则其位于元素周期表
,则其位于元素周期表(2)某种配合物结构如图(H原子未给出)。
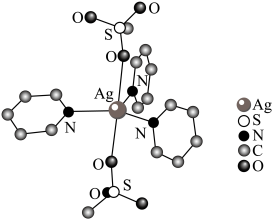
②该配合物中N、O、S三种元素的第一电离能由大到小的顺序为
③该配合物中键角∠O—S—O
(3)铜及其化合物常用作催化剂,如
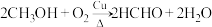 。
。①
 分子中O原子的杂化轨道类型为
分子中O原子的杂化轨道类型为②
 易溶于水,原因是
易溶于水,原因是③
 的立体构型为
的立体构型为 键与
键与 键数目之比为
键数目之比为(4)Pb、S形成的某种晶体结构示意图如图,设晶胞参数为a pm,
 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。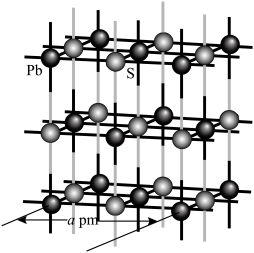
②该晶体的密度为
 。
。
您最近一年使用:0次



