1 . 化学在改变环境与促进发展等方面发挥着重要作用.下列过程涉及氧化还原反应的是
| A.空间站水循环系统使用离子交换树脂脱盐 |
| B.凝胶衍生的多孔超轻气凝胶可以有效去除海洋中泄漏的石油 |
| C.氯化物介导的海洋二氧化碳去除法可以将二氧化碳转化为具有经济价值的有机物 |
D. 回收技术利用废弃 回收技术利用废弃 产生的单体(对苯二甲酸和乙二醇)再聚合,获得全新的塑料 产生的单体(对苯二甲酸和乙二醇)再聚合,获得全新的塑料 |
您最近一年使用:0次
名校
解题方法
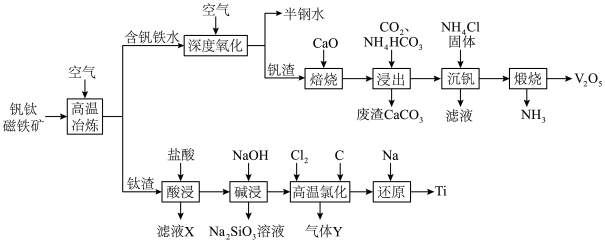
2 . 稀有金属钒和钛在钢铁、化工、航空航天等领域应用广泛。从钒钛磁铁矿中提取钒、钛的工艺流程图如下: 、
、 、
、 和
和 等。
等。
②“高温氯化”后的产物中含少量的 、
、 、
、 、
、 杂质,相关物质的沸点如下表:
杂质,相关物质的沸点如下表:
回答下列问题:
(1)钛在周期表中的位置为___________ ,上述获得钛单质的“还原”工序中需要通入氩气的目的是___________ 。
(2)滤液X中含有的主要金属离子有___________ 。
(3)“高温氯化”工序生成 和一种可燃性气体Y,该反应的化学方程式为
和一种可燃性气体Y,该反应的化学方程式为___________ ; 的粗产品可以通过分馏提纯,但收集的
的粗产品可以通过分馏提纯,但收集的 中总是混有
中总是混有 的原因是
的原因是___________ 。
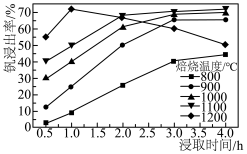
(4)钒的浸出率随焙烧温度和浸取时间的变化如图所示,则“焙烧”时最适合的反应条件为___________ 。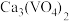 转化成
转化成 进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为
进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为___________ 。
(6)采用USTB工艺电解制备高纯钛,过程以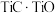 固体为阳极、碳棒为阴极,
固体为阳极、碳棒为阴极, 熔融盐为电解质。阳极产生
熔融盐为电解质。阳极产生 与
与 ,阴极只发生
,阴极只发生 的还原反应。请写出电池阳极反应的电极反应式:
的还原反应。请写出电池阳极反应的电极反应式:___________ 。
 、
、 、
、 和
和 等。
等。②“高温氯化”后的产物中含少量的
 、
、 、
、 、
、 杂质,相关物质的沸点如下表:
杂质,相关物质的沸点如下表:| 化合物 |  |  |  |  |  |
| 沸点/℃ | 136 | 310 | 56.5 | 180 | 127 |
(1)钛在周期表中的位置为
(2)滤液X中含有的主要金属离子有
(3)“高温氯化”工序生成
 和一种可燃性气体Y,该反应的化学方程式为
和一种可燃性气体Y,该反应的化学方程式为 的粗产品可以通过分馏提纯,但收集的
的粗产品可以通过分馏提纯,但收集的 中总是混有
中总是混有 的原因是
的原因是(4)钒的浸出率随焙烧温度和浸取时间的变化如图所示,则“焙烧”时最适合的反应条件为
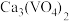 转化成
转化成 进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为
进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为(6)采用USTB工艺电解制备高纯钛,过程以
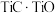 固体为阳极、碳棒为阴极,
固体为阳极、碳棒为阴极, 熔融盐为电解质。阳极产生
熔融盐为电解质。阳极产生 与
与 ,阴极只发生
,阴极只发生 的还原反应。请写出电池阳极反应的电极反应式:
的还原反应。请写出电池阳极反应的电极反应式:
您最近一年使用:0次
2024-05-16更新
|
446次组卷
|
4卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期5月月考化学试题
名校
解题方法
3 . 下列离子方程式与所给事实相符的是
A.向水杨酸溶液中加入碳酸氢钠: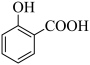 +2HCO +2HCO → →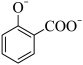 +2H2O+2CO2↑ +2H2O+2CO2↑ |
B.向碳酸氢镁溶液中加入过量澄清石灰水溶液产生白色沉淀: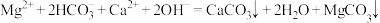 |
C.向 溶液中通入 溶液中通入 气体: 气体: |
D. 溶液滴入 溶液滴入 溶液中: 溶液中: |
您最近一年使用:0次
2024-05-16更新
|
469次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期5月月考化学试题
解题方法
4 . 钛酸钡( )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量CaO、
,含少量CaO、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下:
注:
回答下列问题:
(1)浸渣的主要成分是___________ (填化学式)。
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图所示。___________ 。图2中温度高于65℃,钛浸出率降低的原因可能是___________ 。
(3)“还原”时,主要反应的离子方程式为___________ ,检验“还原”后溶液中是否含 的试剂是
的试剂是___________ (填化学式)。
(4)“沉钛”中,先加入过量 ,溶液,后加入适量
,溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生___________ (填化学式)杂质,影响产率。“调pH”范围为___________ 。
(5)“氧化焙烧”发生反应的化学方程式为___________ 。工业上,还可以直接将 ·4
·4 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是___________ 。
(6)经X射线分析鉴定,钛酸钡的晶胞结构如图所示( 、
、 均与
均与 相接触)。已知晶胞边长为
相接触)。已知晶胞边长为 pm,
pm, 的半径为
的半径为 pm,则
pm,则 的半径为
的半径为___________ pm。
 )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量CaO、
,含少量CaO、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下: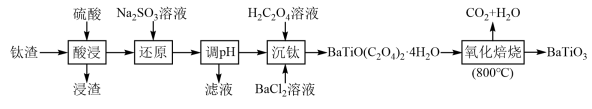
| 金属离子 |  |  |  |
| 开始沉淀/pH | 1.5 | 6.3 | 0.5 |
| 完全沉淀/pH | 2.8 | 8.3 | 2.5 |

回答下列问题:
(1)浸渣的主要成分是
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图所示。

(3)“还原”时,主要反应的离子方程式为
 的试剂是
的试剂是(4)“沉钛”中,先加入过量
 ,溶液,后加入适量
,溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生(5)“氧化焙烧”发生反应的化学方程式为
 ·4
·4 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是(6)经X射线分析鉴定,钛酸钡的晶胞结构如图所示(
 、
、 均与
均与 相接触)。已知晶胞边长为
相接触)。已知晶胞边长为 pm,
pm, 的半径为
的半径为 pm,则
pm,则 的半径为
的半径为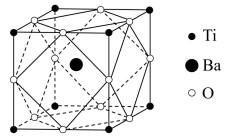
您最近一年使用:0次
5 . 化学与生活、科技、环境密切相关。下列说法错误的是
| A.太阳能电池不属于化学电源 |
B.乙醇汽油的广泛使用不能减少汽车尾气中 的排放 的排放 |
C.月壤中的嫦娥石 属于无机盐 属于无机盐 |
| D.在燃煤中添加生石灰的主要目的是有效减缓温室效应 |
您最近一年使用:0次
6 . 肌红蛋白具有存储氧气的作用,由一个球蛋白和一个血红素基团(a)组成,氧分子和血红素基团结合形成b;当吸入CO时,肌红蛋白失去储氧能力。下列说法错误的是
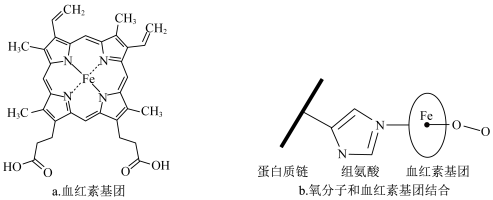
| A.血红素基团中铁元素的化合价为+2价 |
| B.a与b中铁的配位数相同 |
C.血红素基团中元素电负性: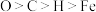 |
D. 与肌红蛋白配位能力弱于CO 与肌红蛋白配位能力弱于CO |
您最近一年使用:0次
解题方法
7 . 硫酸铈铵[ ,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含
,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。
 在空气中易被氧化为
在空气中易被氧化为 ;
; ;
;
回答下列问题:
(1)“滤渣A”的成分除 外,还有
外,还有_____________ (填化学式);
(2)“焙烧”时,下列采取的措施正确的是_____________(填标号);
(3)在另一种工艺中,在氟碳铈矿粉中加入碳酸氢钠固体同时通入氧气焙烧,得到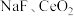 两种固体以及两种高温下的气态物质,该反应的化学方程式为
两种固体以及两种高温下的气态物质,该反应的化学方程式为____________________________ ;
(4)“酸浸”中,铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜条件是_____________(填标号)。
(5) 分子中
分子中 键角
键角_________ (填“大于”“小于”或“等于”)硫脲分子中 键角;
键角;
(6)“溶解”时加入稀盐酸后,还需加入另一种化学试剂X,根据题中信息推测,加入X的作用是__________ ;
(7)含 溶液与足量
溶液与足量 溶液反应生成
溶液反应生成 沉淀的离子方程式为
沉淀的离子方程式为________________ ;
(8)利用硫化锌锂电池电解含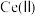 的溶液,可将
的溶液,可将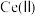 转化为
转化为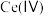 .该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;
.该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示; 中,
中,
________ ;
②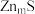 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间最近的核间距为
之间最近的核间距为 ,则
,则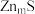 晶体的密度为
晶体的密度为__________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 ,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含
,相对分子质量为596]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。以氟碳铈矿(含 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。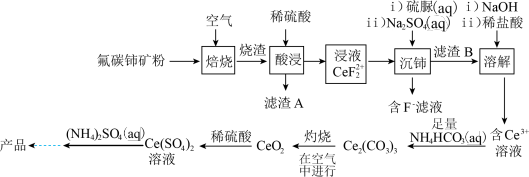
 在空气中易被氧化为
在空气中易被氧化为 ;
;②硫脲的结构简式为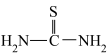 ,具有还原性;
,具有还原性;
 ;
;回答下列问题:
(1)“滤渣A”的成分除
 外,还有
外,还有(2)“焙烧”时,下列采取的措施正确的是_____________(填标号);
| A.采用高压空气,使矿粉呈“沸腾”状 |
| B.空气从焙烧炉上部通入,矿粉从焙烧炉下部加入 |
| C.空气从焙烧炉下部通入,矿粉从焙烧炉上部加入 |
| D.空气、矿粉均从焙烧炉上部通入或加入 |
(3)在另一种工艺中,在氟碳铈矿粉中加入碳酸氢钠固体同时通入氧气焙烧,得到
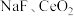 两种固体以及两种高温下的气态物质,该反应的化学方程式为
两种固体以及两种高温下的气态物质,该反应的化学方程式为(4)“酸浸”中,铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜条件是_____________(填标号)。

A.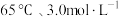 | B.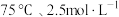 | C. | D. |
(5)
 分子中
分子中 键角
键角 键角;
键角;(6)“溶解”时加入稀盐酸后,还需加入另一种化学试剂X,根据题中信息推测,加入X的作用是
(7)含
 溶液与足量
溶液与足量 溶液反应生成
溶液反应生成 沉淀的离子方程式为
沉淀的离子方程式为(8)利用硫化锌锂电池电解含
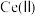 的溶液,可将
的溶液,可将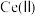 转化为
转化为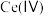 .该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;
.该硫化锌锂电池放电时,负极材料的立方晶胞组成变化如图所示;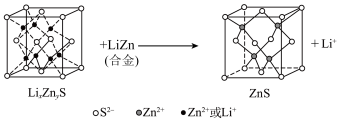
 中,
中,
②
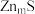 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间最近的核间距为
之间最近的核间距为 ,则
,则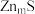 晶体的密度为
晶体的密度为 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
2024-05-14更新
|
106次组卷
|
2卷引用:河南省部分重点高中2023-2024学年高三下学期5月大联考理综试题-高中化学
2024·新疆·三模
解题方法
8 . 化学是现代生产、生活与科技的中心学科之一,下列说法正确的是
| A.中国天眼FAST用到的碳化硅及制作宇航服常用的聚四氟乙烯都属于有机高分子材料 |
| B.“蛟龙”号载人潜水器最关键的部件—耐压球壳是用稀土金属钛(第ⅣB族)制造而成 |
| C.2023年诺贝尔化学奖授予了“发现和合成量子点(纳米级粒子)”的三位科学家,量子点形成分散系后可能具有丁达尔效应 |
| D.超分子内部分子之间通过共价键结合 |
您最近一年使用:0次
2024-05-14更新
|
91次组卷
|
3卷引用:T7-化学与STSE
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 甲苯中含有 甲苯中含有 键和 键和 键的总数为 键的总数为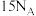 |
B.常温下, 溶液中含有阴离子的数目为 溶液中含有阴离子的数目为 |
C.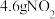 和 和 的混合物中含有电子的数目为 的混合物中含有电子的数目为 |
D. 甲酸和乙醇的混合物中含有原子的数目为 甲酸和乙醇的混合物中含有原子的数目为 |
您最近一年使用:0次
10 . 磷酸铁锂前驱体磷酸铁是一种重要的化工原料,被广泛用于汽车电池。用浓硫酸浸取钛铁矿(主要成分为 ),得到含
),得到含 的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:
的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:___________ 。
(2)先加入磷酸,再加入NaOH,调节pH约为2,生成磷酸铁沉淀。若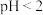 ,会导致
,会导致___________ ;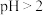 ,会导致
,会导致___________ 。
(3)经陈化、过滤后,所得滤液除少量磷酸铁外还含有的主要成分是___________ 。将滤液收集用于溶解步骤,其目的是___________ (答出两条即可)。
(4)在该流程中,以 、
、 、
、 和NaOH为反应物制得水合磷酸铁
和NaOH为反应物制得水合磷酸铁 总反应的离子方程式为
总反应的离子方程式为___________ 。
(5)煅烧水合磷酸铁过程中的TG(热重)及DSC(反映体系热量变化况,数值已省略)曲线如下图。样品在50~120℃有少量失重,可能是样品吸潮引起的少量游离水的损失(0.7%左右),从120℃开始有明显的失重,到200℃时失重达19.98%,则x值为___________ 。 为正交晶系结构,其晶胞参数为
为正交晶系结构,其晶胞参数为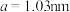 、
、 、
、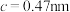 ,
, 。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为
。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为___________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ),得到含
),得到含 的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:
的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下: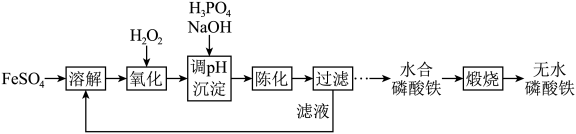
(2)先加入磷酸,再加入NaOH,调节pH约为2,生成磷酸铁沉淀。若
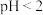 ,会导致
,会导致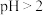 ,会导致
,会导致(3)经陈化、过滤后,所得滤液除少量磷酸铁外还含有的主要成分是
(4)在该流程中,以
 、
、 、
、 和NaOH为反应物制得水合磷酸铁
和NaOH为反应物制得水合磷酸铁 总反应的离子方程式为
总反应的离子方程式为(5)煅烧水合磷酸铁过程中的TG(热重)及DSC(反映体系热量变化况,数值已省略)曲线如下图。样品在50~120℃有少量失重,可能是样品吸潮引起的少量游离水的损失(0.7%左右),从120℃开始有明显的失重,到200℃时失重达19.98%,则x值为

 为正交晶系结构,其晶胞参数为
为正交晶系结构,其晶胞参数为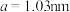 、
、 、
、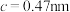 ,
, 。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为
。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。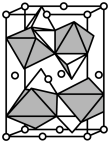
您最近一年使用:0次
2024-05-14更新
|
71次组卷
|
2卷引用:2024届河南省平许济洛四市高三下学期第四次质量检测理科综合试题-高中化学



