解题方法
1 . 氨基磺酸(H2NSO3H)是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。某实验室用尿素和发烟硫酸(溶有SO3的硫酸)制备氨基磺酸的流程如图:
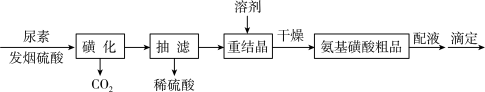
已知“磺化”步骤发生的反应为:
①CO(NH2)2(s)+SO3(g) H2NCONHSO3H(s) ΔH<0
H2NCONHSO3H(s) ΔH<0
②H2NCONHSO3H+H2SO4 2H2NSO3H+CO2↑
2H2NSO3H+CO2↑
发生“磺化”步骤反应的装置如图1所示:请回答下列问题:
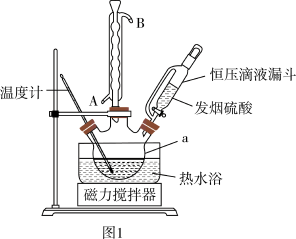
(1)下列关于“磺化”与“抽滤”步骤的说法中正确的是____ 。
A.仪器a的名称是三颈烧瓶
B.冷凝回流时,冷凝水应该从冷凝管的B管口通入
C.抽滤操作前,应先将略小于漏斗内径却又能将全部小孔盖住的滤纸平铺在布氏漏斗中,稍稍润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上,再转移悬浊液
D.抽滤结束后为了防止倒吸,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶之间的橡皮管
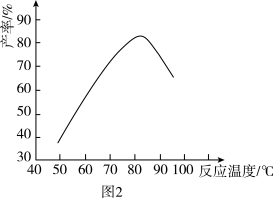
(2)“磺化”过程温度与产率的关系如图2所示,控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,可能的原因是____ 。
(3)“抽滤”时,所得晶体要用乙醇洗涤,则洗涤的具体操作是____ 。
(4)“重结晶”时,溶剂选用10%~12%的硫酸而不用蒸馏水的原因是____ 。
(5)“配液及滴定”操作中,准确称取2.500g氨基磺酸粗品配成250mL待测液。取25.00mL待测液于锥形瓶中,以淀粉-碘化钾溶液做指示剂,用0.08000mol•L-1的NaNO2标准溶液进行滴定,当溶液恰好变蓝时,消耗NaNO2标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2。
①电子天平使用前须____ 并调零校准。称量时,可先将洁净干燥的小烧杯放在称盘中央,显示数字稳定后按____ ,再缓缓加样品至所需质量时,停止加样,读数记录。
②试求氨基磺酸粗品的纯度:____ (用质量分数表示)。
③若以酚酞为指示剂,用0.08000mol•L-1的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比NaNO2法____ (填“偏高”或“偏低”)。

已知“磺化”步骤发生的反应为:
①CO(NH2)2(s)+SO3(g)
 H2NCONHSO3H(s) ΔH<0
H2NCONHSO3H(s) ΔH<0②H2NCONHSO3H+H2SO4
 2H2NSO3H+CO2↑
2H2NSO3H+CO2↑发生“磺化”步骤反应的装置如图1所示:请回答下列问题:

(1)下列关于“磺化”与“抽滤”步骤的说法中正确的是
A.仪器a的名称是三颈烧瓶
B.冷凝回流时,冷凝水应该从冷凝管的B管口通入
C.抽滤操作前,应先将略小于漏斗内径却又能将全部小孔盖住的滤纸平铺在布氏漏斗中,稍稍润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上,再转移悬浊液
D.抽滤结束后为了防止倒吸,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶之间的橡皮管
(2)“磺化”过程温度与产率的关系如图2所示,控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,可能的原因是

(3)“抽滤”时,所得晶体要用乙醇洗涤,则洗涤的具体操作是
(4)“重结晶”时,溶剂选用10%~12%的硫酸而不用蒸馏水的原因是
(5)“配液及滴定”操作中,准确称取2.500g氨基磺酸粗品配成250mL待测液。取25.00mL待测液于锥形瓶中,以淀粉-碘化钾溶液做指示剂,用0.08000mol•L-1的NaNO2标准溶液进行滴定,当溶液恰好变蓝时,消耗NaNO2标准溶液25.00mL。此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2。
①电子天平使用前须
②试求氨基磺酸粗品的纯度:
③若以酚酞为指示剂,用0.08000mol•L-1的NaOH标准溶液进行滴定,也能测定氨基磺酸粗品的纯度,但测得结果通常比NaNO2法
您最近一年使用:0次
19-20高二·浙江·期末
2 . (1)向一定量 和
和 溶液反应后的某溶液中逐滴滴入稀盐酸,开始阶段未产生
溶液反应后的某溶液中逐滴滴入稀盐酸,开始阶段未产生 气体,则该溶液中的溶质组成可能是
气体,则该溶液中的溶质组成可能是_______ 。
(2)某天然碱可以看作是 和
和 反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
ⅰ称取3.98g天然碱样品,加入50mL稀盐酸(足量),产生 896mL(标准状况)。
896mL(标准状况)。
ⅱ称取3.98g天然碱样品,加热至分解完全,产生 224mL(标准状况)和0.36g水。
224mL(标准状况)和0.36g水。
①该稀盐酸的物质的量浓度最小是_______ 。
②天然碱的化学式是_______ 。
 和
和 溶液反应后的某溶液中逐滴滴入稀盐酸,开始阶段未产生
溶液反应后的某溶液中逐滴滴入稀盐酸,开始阶段未产生 气体,则该溶液中的溶质组成可能是
气体,则该溶液中的溶质组成可能是(2)某天然碱可以看作是
 和
和 反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:
反应后的产物组成的一种物质。为了研究该物质的组成,进行如下实验:ⅰ称取3.98g天然碱样品,加入50mL稀盐酸(足量),产生
 896mL(标准状况)。
896mL(标准状况)。ⅱ称取3.98g天然碱样品,加热至分解完全,产生
 224mL(标准状况)和0.36g水。
224mL(标准状况)和0.36g水。①该稀盐酸的物质的量浓度最小是
②天然碱的化学式是
您最近一年使用:0次
名校
解题方法
3 . 某小组为探究K3[Fe(C2O4)3·3H2O(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验。下列有关叙述错误的是
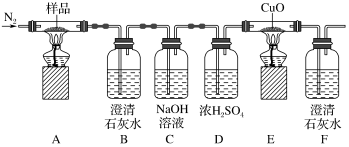

| A.通入氮气的目的有;隔绝空气、使反应产生的气体全部进入后续装置 |
| B.实验中观察到装置F中澄清石灰水变浑浊,装置E中固体变为红色,由此可判断热分解产物中一定含有CO2和CO |
| C.为防止倒吸,停止实验时应进行的操作是:先熄灭装置A、E的酒精灯,冷却后停止通入氮气 |
D.样品完全分解后,取少许装置A中残留物于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,可证明残留物中含有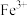 |
您最近一年使用:0次
2020-01-12更新
|
1482次组卷
|
8卷引用:【浙江新东方】绍兴qw78
(已下线)【浙江新东方】绍兴qw78山东省日照一中2020届高三新高考3月份自测化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(二)山东省潍坊昌乐县第二中学2020届高三下学期3月阶段测试化学试题北京市第一七一中学 2020-2021学年高一上学期期中考试化学试题【省级联考】湖北省2020年第五届高考测评活动高三元月调考(一模)理综化学试题福建省厦门双十中学2022-2023学年高一上学期第二次月考化学试题福建省三明第一中学2023-2024学年高一上学期12月月考化学试题
4 . 氯化亚铜(CuCl)广泛应用于有机合成、染料、颜料、催化剂等工业。它是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸,可溶于氨水、浓盐酸,并生成配合物NH4[CuCl2];能在空气中迅速被氧化成绿色;见光则分解,变成褐色。下图是实验室制备氯化亚铜的流程图及实验装置图。
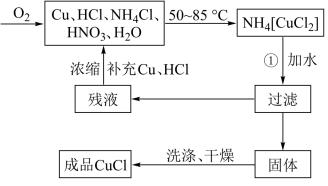
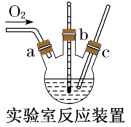
实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
(1)请写出①的化学方程式____________________________________ 。
(2)本实验中通入O2的速率不宜过大,宜选择下图中的____ (填字母序号)方案,并说明选择该装置的理由__________________________________________ 。
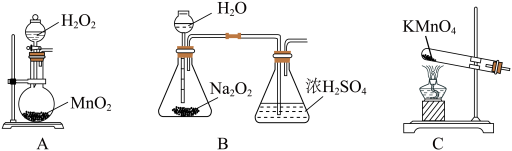
(3)电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为_____ 时,停止通入氧气,打开瓶塞,沿C口倾出反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出。
(4)关于该实验过程中,下列说法正确的是_________________ 。
A 实验开始时,温度计显示反应液温度可能低于室温。
B 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。
C 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。
D 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
(5)氯化亚铜的定量分析:
①称取成品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2,Fe2+ + Ce4+ = Fe3+ + Ce3+)
④数据处理:计算得CuCl的纯度为__________ 。


实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
(1)请写出①的化学方程式
(2)本实验中通入O2的速率不宜过大,宜选择下图中的

(3)电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为
(4)关于该实验过程中,下列说法正确的是
A 实验开始时,温度计显示反应液温度可能低于室温。
B 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。
C 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。
D 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
(5)氯化亚铜的定量分析:
①称取成品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2,Fe2+ + Ce4+ = Fe3+ + Ce3+)
| 实验序号 | 1 | 2 | 3 |
| 滴定起始读数(mL) | 0.75 | 0.50 | 0.80 |
| 滴定终点读数(mL) | 24.70 | 24.95 | 24.85 |
您最近一年使用:0次
2019-08-10更新
|
853次组卷
|
3卷引用:浙江省诸暨中学2018-2019学年高二(实验班)下学期期中考试化学试题
名校
5 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。利用“KClO3氧化法”制备 KIO3工艺流程如下图所示,回答下列问题:
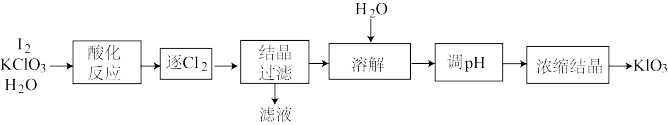
(1)“酸化反应”所得产物有 KH(IO3)2、Cl2 和 KCl。“逐 Cl2”采用的方法是________ ;
(2)“滤液”中的溶质主要是_______ ;“调 pH”中发生反应的化学方程式为_____________________ ;
(3)结晶过滤时工人发现 KH(IO3)2为悬浮絮状沉淀,以下可以采用的方法是________ ;
A.倾析法 B.重结晶法 C.抽滤法 D. 离心分离法
(4)生产中,如果省去“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂 X 调整反应后溶液的 pH,对生产碘酸钾有什么具体影响_________________________________________________________________ ;
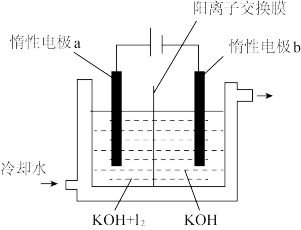
(5)KIO3也可采用“电解法”制备,装置如图所示。与“电解法”相比,“KClO3氧化法”的主要不足之处有_____________________________________ ;(写出一点)
(6)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-。测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取 w g 食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量 KI 溶液,使 KIO3与 KI 反应完全;
c.以淀粉为指示剂,加入物质的量浓度为2.0×10-3mol·L-1的 Na2S2O3 溶液 10.0mL 恰好反应。 则加碘食盐样品中的碘元素含量是______________ mg/kg;(以含 w 的代数式表示)
(7)学生乙又对纯净的 NaCl(不含 KIO3)进行了下列实验:
根据学生乙的实验结果,请对学生甲的实验结果作出简要评价___________________________ 。

(1)“酸化反应”所得产物有 KH(IO3)2、Cl2 和 KCl。“逐 Cl2”采用的方法是
(2)“滤液”中的溶质主要是
(3)结晶过滤时工人发现 KH(IO3)2为悬浮絮状沉淀,以下可以采用的方法是
A.倾析法 B.重结晶法 C.抽滤法 D. 离心分离法
(4)生产中,如果省去“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂 X 调整反应后溶液的 pH,对生产碘酸钾有什么具体影响
(5)KIO3也可采用“电解法”制备,装置如图所示。与“电解法”相比,“KClO3氧化法”的主要不足之处有

(6)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-。测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取 w g 食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量 KI 溶液,使 KIO3与 KI 反应完全;
c.以淀粉为指示剂,加入物质的量浓度为2.0×10-3mol·L-1的 Na2S2O3 溶液 10.0mL 恰好反应。 则加碘食盐样品中的碘元素含量是
(7)学生乙又对纯净的 NaCl(不含 KIO3)进行了下列实验:
| 操作步骤 | 实验现象 |
| 取 1g 纯净的 NaCl,加 3mL 水配成溶液。 | 溶液无变化 |
| 滴入 5 滴淀粉溶液和 1mL 0.1 mol·L-1KI 溶液,振荡。 | 溶液无变化 |
| 然后再滴入 1 滴 1mol·L-1的 H2SO4,振荡。 | 溶液变蓝色 |
您最近一年使用:0次
18-19高二下·浙江宁波·期中
名校
解题方法
6 . Fe2O3俗称氧化铁红,常用作油漆等着色剂。某实验小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁并进行铁含量的测定,实验过程中的主要操作步骤如下:
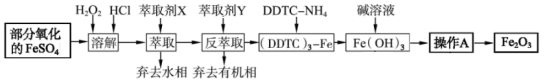
已知:①在盐酸浓度较高时,Fe3+与甲基异丁基甲酮形成可溶性的化合物,当盐酸浓度降低时,该化合物解离。
②3DDTC—NH4+Fe3+=(DDTC)3—Fe↓+3NH4+。
请回答下列问题:
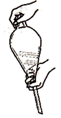
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是_________。
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是__________。
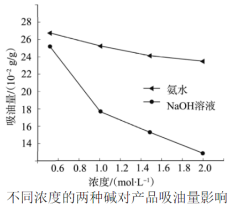
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图所示,则上述实验过程中选用的碱溶液为_________ (填“NaOH”或“NH3·H2O”),反应的化学方程式为___________ 。
(4)①操作A为抽滤、______ 、____ ;
②有关抽滤,下列说法正确的是____ 。

A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 滤纸应比漏斗内径略小,且能盖住所有小孔
C. 抽滤得到的滤液应从吸滤瓶的支管口倒出
D. 右图所示的抽滤装置中,只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
E. 抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
F. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
(5)现准确称取4.000 g,样品,经酸溶、还原为Fe2+,用容量瓶配成100 mL溶液。用移液管移取25.00 mL溶液于锥形瓶中,用0.l200 mol·L-1的KMnO4溶液进行滴定(还原产物是Mn2+,假设杂质不与KMnO4反应),记录数据如下:
①用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为______ ;
②所用的指示剂为____ ;KMnO4溶液置于_____ (酸式、碱式)滴定管中。
A. 酚酞 B. 甲基橙 C. 石蕊 D. 不需要

已知:①在盐酸浓度较高时,Fe3+与甲基异丁基甲酮形成可溶性的化合物,当盐酸浓度降低时,该化合物解离。
②3DDTC—NH4+Fe3+=(DDTC)3—Fe↓+3NH4+。
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是_________。

| A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中 |
| B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液 |
| C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图用力振摇 |
| D.振摇几次后需打开分液漏斗上口的玻璃塞放气 |
| E.经几次振摇并放气后,手持分液漏斗静置待液体分层 |
| F.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体 |
| A.高纯水 | B.盐酸 | C.稀硫酸 | D.酒精 |

(4)①操作A为抽滤、
②有关抽滤,下列说法正确的是

A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 滤纸应比漏斗内径略小,且能盖住所有小孔
C. 抽滤得到的滤液应从吸滤瓶的支管口倒出
D. 右图所示的抽滤装置中,只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
E. 抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
F. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
(5)现准确称取4.000 g,样品,经酸溶、还原为Fe2+,用容量瓶配成100 mL溶液。用移液管移取25.00 mL溶液于锥形瓶中,用0.l200 mol·L-1的KMnO4溶液进行滴定(还原产物是Mn2+,假设杂质不与KMnO4反应),记录数据如下:
| 滴定序号 | 待测溶液体积/mL | 消耗KMnO4标准溶液体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 1 | 25.00 | 1.15 | 21.98 |
| 2 | 25.00 | 0.50 | 21.96 |
| 3 | 25.00 | 0 | 20.77 |
①用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为
②所用的指示剂为
A. 酚酞 B. 甲基橙 C. 石蕊 D. 不需要
您最近一年使用:0次
13-14高三下·浙江宁波·阶段练习
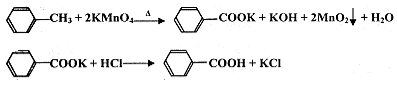
7 . 苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)
已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL,甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举:
请回答:
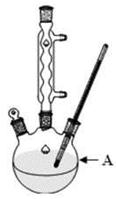
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为 。
(3)操作I的名称 。
(4)步骤③中用到的定量仪器有 ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果 (填“偏大”、“偏小”或“不变”)。

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。

实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL,甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为 。
(3)操作I的名称 。
(4)步骤③中用到的定量仪器有 ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果 (填“偏大”、“偏小”或“不变”)。
您最近一年使用:0次
真题
名校
8 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]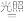 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是________________________________________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________ 、___________ 。
③为防止倒吸,停止实验时应进行的操作是_____________________________ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________ 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________ 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
2018-06-09更新
|
13241次组卷
|
19卷引用:考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题四川省攀枝花市第十二中学2019届高三上学期10月月考化学试题广东省惠州市第一中学2019届高三上学期理科综合测试(二)化学试题云南省马关县二中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题云南省大理白族自治州漾濞二中2019—2020学年9月份高三化学考试试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)西藏自治区拉萨中学2022届高三第六次月考理综化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题
9 . 由某精矿石(MCO3·ZCO3)可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,取该矿石样品1.84g,高温灼烧至恒重,得到0.96g仅含两种金属氧化物的固体,其中m(M)︰m(Z)=3:5,请回答:
(1)该矿石的化学式为_______ 。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式_______ 。
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是_______ 。
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g) CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
反应3:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。

则△H3_______ △H2 (填“大于”、“小于”、“等于”),理由是_______ 。
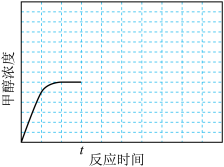
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。_______
(1)该矿石的化学式为
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1反应2:CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2反应3:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。

则△H3
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。

您最近一年使用:0次
名校
解题方法
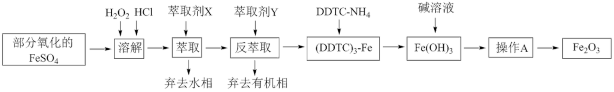
10 . Fe2O3俗称氧化铁红,常用作油漆等着色剂。某实验小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁并进行铁含量的测定。实验过程中的主要操作步骤如下:
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
② 3DDTC-NH4+Fe3+= (DDTC) 3-Fe↓+3NH4+
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是____________ 。
A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中
B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液
C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图用力振摇
D.振摇几次后需打开分液漏斗上口的玻璃塞放气
E.经几次振摇并放气后,手持分液漏斗静置待液体分层
F.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是_______________ 。
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图所示,则上述实验过程中选用的碱溶液为_______________ (填“NaOH”或“NH3·H2O”),反应的化学方程式为_________________ 。
(4)操作A为______________________ 。
(5)现准确称取4.000g , 样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定(还原产物是Cr3+),消耗K2Cr2O7溶液20.80mL。
① 用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为_____ 。
② 产品中铁的含量为_______ (假设杂质不与K2Cr2O7反应)。
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
② 3DDTC-NH4+Fe3+= (DDTC) 3-Fe↓+3NH4+
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是
A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中
B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液
C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图用力振摇

D.振摇几次后需打开分液漏斗上口的玻璃塞放气
E.经几次振摇并放气后,手持分液漏斗静置待液体分层
F.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图所示,则上述实验过程中选用的碱溶液为
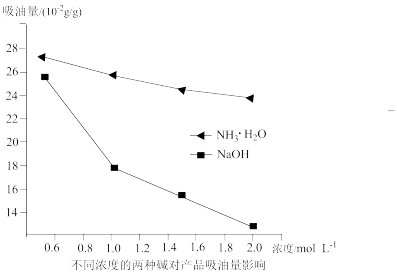
(4)操作A为
(5)现准确称取4.000g , 样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定(还原产物是Cr3+),消耗K2Cr2O7溶液20.80mL。
① 用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为
② 产品中铁的含量为
您最近一年使用:0次
2017-03-15更新
|
522次组卷
|
3卷引用:2017届浙江省宁波市高三新高考选考适应性考试化学试卷



