名校
1 . Ⅰ.回答下列问题:
(1)(NH4)2SO4溶液可以用来除铁锈的原因:_______ (用离子方程式说明)。
(2)部分弱酸的电离平衡常数如表:
室温下①0.1mol·L-1HCOONa②0.1 mol·L-1 NaClO③0.1 mol·L-1Na2CO3④ 0.1 mol·L-1NaHCO3溶液的pH由大到小的关系为_______ 。
(3)根据上述电离平衡常数,试写出下列化学反应的离子方程式:
①向碳酸钠溶液中通入少量二氧化硫气体_______
②向碳酸钠溶液中滴入过量甲酸_______
Ⅱ.常温下,HNO2的电离平衡常数Ka =2.6×10-4,亚硝酸钠(NaNO2)是一种重要的食品添加剂,由于其外观及味道都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生。
(4)亚硝酸钠有毒,不能随意丢弃,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,其产物之一为无色无味气体,则反应的化学方程式为_______ 。
(5)某活动小组同学设计实验方案鉴别NaCl溶液和NaNO2溶液,请填写下列表格。
Ⅲ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。

已知:①2NO+Na2O2=2NaNO2,
②酸性条件下,NO、NO2都能与 反应生成
反应生成 和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
(6)实验装置的连接顺序为A→_______→_______→_______→_______→B;_
(7)C瓶内发生反应的离子方程式为_______ 。
(8)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol·L-1的酸性KMnO4溶液进行滴定,实验所得数据如下表。
①第一组实验数据出现较明显异常,造成异常的原因可能是_______ (填字母序号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.判断终点时,滴入一滴酸性KMnO4溶液,锥形瓶内溶液呈浅红色,振荡后立即褪色
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为_______ 。
(1)(NH4)2SO4溶液可以用来除铁锈的原因:
(2)部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka =1.77×10-4 | Ka= 4.0×10-8 | Ka1=4.3 ×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(3)根据上述电离平衡常数,试写出下列化学反应的离子方程式:
①向碳酸钠溶液中通入少量二氧化硫气体
②向碳酸钠溶液中滴入过量甲酸
Ⅱ.常温下,HNO2的电离平衡常数Ka =2.6×10-4,亚硝酸钠(NaNO2)是一种重要的食品添加剂,由于其外观及味道都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生。
(4)亚硝酸钠有毒,不能随意丢弃,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,其产物之一为无色无味气体,则反应的化学方程式为
(5)某活动小组同学设计实验方案鉴别NaCl溶液和NaNO2溶液,请填写下列表格。
| 选用药品 | 实验现象(NaNO2溶液) | 利用NaNO2的性质 |
| ①酚酞试液 | ||
| ②淀粉-KI试纸 |
Ⅲ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。

已知:①2NO+Na2O2=2NaNO2,
②酸性条件下,NO、NO2都能与
 反应生成
反应生成 和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。(6)实验装置的连接顺序为A→_______→_______→_______→_______→B;
(7)C瓶内发生反应的离子方程式为
(8)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol·L-1的酸性KMnO4溶液进行滴定,实验所得数据如下表。
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.判断终点时,滴入一滴酸性KMnO4溶液,锥形瓶内溶液呈浅红色,振荡后立即褪色
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为
您最近一年使用:0次
解题方法
2 . 钛合金是建造神舟十二号与天和核心舱的重要材料,钛的化合物钛酸锶(SrTiO3)广泛应用于高压电容器、压敏电阻、热敏电阻等电子元件。一种“溶胶-沉淀”一步法合成钛酸锶纳米粉体的工艺流程如图所示。
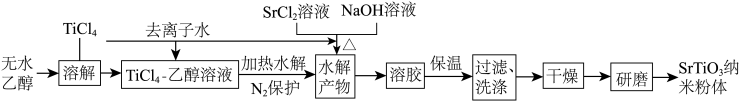
已知:TiCl4易溶于无水乙醇,Ti4+加热水解生成TiO2·xH2O;SrSO4在1580℃以上分解。
回答下列问题:
(1) 中
中 的化合价为
的化合价为_______ 。
(2)写出生成 溶胶的化学方程式:
溶胶的化学方程式:_______ 。
(3)对 溶胶进行保温的目的是
溶胶进行保温的目的是_______ 。
(4)检验 沉淀是否洗涤干净的操作为
沉淀是否洗涤干净的操作为_______ 。
(5) 溶液的浓度、钛液浓度、反应时间对
溶液的浓度、钛液浓度、反应时间对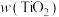 、产物纯度的影响如表所示。
、产物纯度的影响如表所示。
合成高纯 纳米粉体的最佳工艺条件为
纳米粉体的最佳工艺条件为_______ 。
(6)钛酸锶中钛锶比的测定。
①测定 的含量:称取
的含量:称取 样品,经一系列处理除去
样品,经一系列处理除去 后,配制成
后,配制成 溶液,移取
溶液,移取 溶液于锥形瓶中,准确加入
溶液于锥形瓶中,准确加入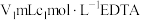 标准溶液(过量),充分反应后,加入指示剂,用
标准溶液(过量),充分反应后,加入指示剂,用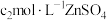 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗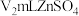 溶液。则钛酸锶中
溶液。则钛酸锶中 的质量分数为
的质量分数为_______ (列出计算式即可,已知滴定计量关系: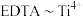 ,
,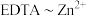 )。
)。
②测定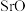 的含量:称取
的含量:称取 样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成
样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成 溶液,用氨水调节溶液
溶液,用氨水调节溶液 ,完全沉淀后过滤得到
,完全沉淀后过滤得到 沉淀,于
沉淀,于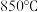 时灼烧至恒重,质量为
时灼烧至恒重,质量为 。则钛酸锶中钛锶比为
。则钛酸锶中钛锶比为_______ [钛锶比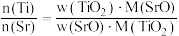 ]。
]。

已知:TiCl4易溶于无水乙醇,Ti4+加热水解生成TiO2·xH2O;SrSO4在1580℃以上分解。
回答下列问题:
(1)
 中
中 的化合价为
的化合价为(2)写出生成
 溶胶的化学方程式:
溶胶的化学方程式:(3)对
 溶胶进行保温的目的是
溶胶进行保温的目的是(4)检验
 沉淀是否洗涤干净的操作为
沉淀是否洗涤干净的操作为(5)
 溶液的浓度、钛液浓度、反应时间对
溶液的浓度、钛液浓度、反应时间对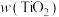 、产物纯度的影响如表所示。
、产物纯度的影响如表所示。| 反应条件 | 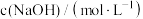 | 钛液浓度/ | 反应时间/h | ||||||
| 3.30 | 5.30 | 7.30 | 1.60 | 2.20 | 2.80 | 4 | 5 | 6 | |
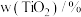 | 32.31 | 32.79 | 33.34 | 32.33 | 32.79 | 33.34 | 32.07 | 33.34 | 32.35 |
| 产物纯度/% | 94.69 | 96.36 | 97.69 | 92.77 | 97.00 | 97.69 | 95.12 | 97.69 | 97.52 |
 纳米粉体的最佳工艺条件为
纳米粉体的最佳工艺条件为(6)钛酸锶中钛锶比的测定。
①测定
 的含量:称取
的含量:称取 样品,经一系列处理除去
样品,经一系列处理除去 后,配制成
后,配制成 溶液,移取
溶液,移取 溶液于锥形瓶中,准确加入
溶液于锥形瓶中,准确加入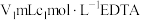 标准溶液(过量),充分反应后,加入指示剂,用
标准溶液(过量),充分反应后,加入指示剂,用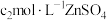 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗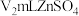 溶液。则钛酸锶中
溶液。则钛酸锶中 的质量分数为
的质量分数为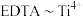 ,
,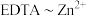 )。
)。②测定
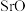 的含量:称取
的含量:称取 样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成
样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成 溶液,用氨水调节溶液
溶液,用氨水调节溶液 ,完全沉淀后过滤得到
,完全沉淀后过滤得到 沉淀,于
沉淀,于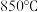 时灼烧至恒重,质量为
时灼烧至恒重,质量为 。则钛酸锶中钛锶比为
。则钛酸锶中钛锶比为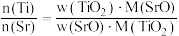 ]。
]。
您最近一年使用:0次
名校
解题方法
3 . 下列方案设计、现象和结论有不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验海带中是否含有碘元素 | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量新制氯水,充分反应后加入1~2滴淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| B | 鉴定淀粉是否完全水解 | 取少量淀粉于锥形瓶中,以固液比1∶10加入稀硫酸,牛皮纸封口,在120℃下水解30min,取适量水解液于试管中,加入少量碘-碘化钾溶液 | 溶液未变蓝,则证明淀粉已完全水解 |
| C | 检验CO还原 的生成物中是否含有 的生成物中是否含有 | 将适量反应后的固体溶于稀盐酸中,取少量溶解液于试管中,滴加硫氰化钾溶液 | 溶液变血红色,则证明还原产物中含有 |
| D | 检验食盐中是否混有少量亚硝酸钠 | 取适量食盐样品于试管中,加水溶解后加入硝酸银溶液,过滤后取滤渣,滴加稀硝酸 | 若沉淀部分溶解,则证明食盐中混有亚硝酸钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-14更新
|
790次组卷
|
7卷引用:浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题
浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题(已下线)2022年浙江省6月高考真题变式题21-25(已下线)押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)江苏省淮安市钦工中学2022-2023学年高三上学期第一次月考化学试题江苏省徐州市第七中学2022-2023学年高三上学期9月摸底学情调研化学试题湖南省攸县第二中学2022-2023学年高三第六次月考化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题
解题方法
4 . 硫氰化钾(KSCN)是一种用途广泛的化学药品。某小组以二疏化碳(CS2)和氨水为原料制备KSCN晶体,按如下流程开展了实验:

已知:①CS2不溶于水,密度比水的大; 不溶于CS2;
不溶于CS2;
②
请回答:
(1)步骤Ⅰ中判断反应已经完全的实验现象是_______
(2)步骤Ⅱ的脱硫蒸发的目的是除去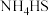 ,产生的气体用上图1进行吸收。
,产生的气体用上图1进行吸收。

①采用多孔球泡的作用是_______
②吸收硫化氢的离子反应方程式是_______
(3)下列说法不正确的是_______
(4)步骤Ⅴ提纯的方法是KSCN粗品在沸腾的乙醇中重结晶。请给出合理的操作排序:(下列提供的部分步骤可不用,也可重复使用) _______
_______→_______→_______→_______→_______→_______→纯品
a.趁热过滤 b.粗品溶于乙醇制热饱和溶液 c.粗品溶于水制热饱和溶液 d.缓慢冷却 e.加入活性炭回流脱色 f.100℃减压干燥 h.抽滤
(5)测定产品中KSCN的含量:称取10.0g样品,配成1000mL溶液。量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 溶液,用
溶液,用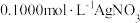 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 溶液20.00mL。
溶液20.00mL。
滴定时发生的反应: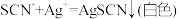 )
)
①判断到达滴定终点的方法是_______
②样品中KSCN的质量分数为_______ (计算结果精确至0.1%)。

已知:①CS2不溶于水,密度比水的大;
 不溶于CS2;
不溶于CS2;②

请回答:
(1)步骤Ⅰ中判断反应已经完全的实验现象是
(2)步骤Ⅱ的脱硫蒸发的目的是除去
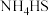 ,产生的气体用上图1进行吸收。
,产生的气体用上图1进行吸收。
①采用多孔球泡的作用是
②吸收硫化氢的离子反应方程式是
(3)下列说法不正确的是_______
A.步骤Ⅲ可以用 溶液潜换KOH溶液 溶液潜换KOH溶液 |
| B.步骤Ⅳ中减压蒸发可以加快蒸发速率及防止产物的分解 |
| C.步骤Ⅳ中采取冰水快速冷却溶液以得到颗粒比较大的晶体 |
| D.步骤Ⅳ中采用的离心分离是借助于离心力,使密度不同的物质进行分离的方法 |
_______→_______→_______→_______→_______→_______→纯品
a.趁热过滤 b.粗品溶于乙醇制热饱和溶液 c.粗品溶于水制热饱和溶液 d.缓慢冷却 e.加入活性炭回流脱色 f.100℃减压干燥 h.抽滤
(5)测定产品中KSCN的含量:称取10.0g样品,配成1000mL溶液。量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
 溶液,用
溶液,用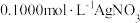 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 溶液20.00mL。
溶液20.00mL。滴定时发生的反应:
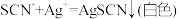 )
)①判断到达滴定终点的方法是
②样品中KSCN的质量分数为
您最近一年使用:0次
解题方法
5 . 下列实验方案设计、预期现象和结论都正确的是
| 目的 | 实验方案设计 | 现象和结论 | |
| A | 比较AgCl和AgI的 大小 大小 | 向NaCl和NaI的混合溶液中滴加少量 溶液,观察现象 溶液,观察现象 | 若溶液中产生黄色沉淀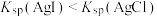 |
| B | 比较C和Si元素的非金属性强弱 | 将碳单质和二氧化硅固体混合置于硬质玻璃管内高温加热,并检验反应后产物 | 若反应后有灰黑色金属光泽的硅单质生成,则非金属性:C>Si |
| C | 检验苯中是否含有苯酚 | 取少量样品于试管中,滴加适量的浓溴水,观察现象 | 若未观察到有白色沉淀产生,则说明苯中不含有苯酚 |
| D | 验证 溶液中含有的含碘微粒 溶液中含有的含碘微粒 | 向两支盛有 溶液的试管中,分别滴加淀粉溶液和 溶液的试管中,分别滴加淀粉溶液和 溶液,观察现象 溶液,观察现象 | 若前者溶液变蓝,后者有黄色沉淀,则 溶液中存在 溶液中存在 和 和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
名校
6 . 某同学设计实验确定Al(NO3)3·xH2O的结晶水数目。称取样品7.50g,经热分解测得气体产物中有NO2、O2、HNO3、H2O,其中H2O的质量为3.06g;残留的固体产物是Al2O3,质量为1.02g。计算:
(1)x=_______ (写出计算过程)。
(2)气体产物中n(O2)_______ mol。
(1)x=
(2)气体产物中n(O2)
您最近一年使用:0次
2022-01-12更新
|
4660次组卷
|
7卷引用:2022 年1月浙江省普通高校招生选考科目考试化学试题
2022 年1月浙江省普通高校招生选考科目考试化学试题浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题(已下线)2022年浙江1月高考真题变式题(26-31)(已下线)微专题04 以物质的量为中心的计算-备战2023年高考化学一轮复习考点微专题河南省濮阳市第一高级中学2022-2023学年高三上学期第一次月考化学试题(已下线)微专题 化学计算的思想方法(已下线)第03讲 物质的量在化学方程式计算中的应用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
7 . 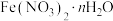 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。
(1)n=_______ (写出计算过程)。
(2)在标准状况下气体产物中 的体积为
的体积为_______ L。
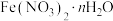 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。(1)n=
(2)在标准状况下气体产物中
 的体积为
的体积为
您最近一年使用:0次
解题方法
8 . 淀粉作为天然高分子材料,通过化学改性可以具有新的、独特的性能,其中接枝共聚改性是近来发展较快的一种重要的手段和方法,所得到的接枝改性淀粉兼有天然和合成高分子两者的优点,性能优异,在纺织、造纸、降解塑料、水处理工业等方面得到广泛的应用。某化学小组在实验室中进行了丙烯酸乙酯接枝淀粉的制备实验。
实验装置:
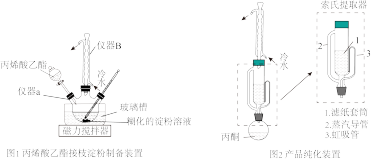
实验步骤:
步骤Ⅰ:加入 乙醚于仪器a中,并用塞子封堵其中两个瓶口,缓慢加热至
乙醚于仪器a中,并用塞子封堵其中两个瓶口,缓慢加热至 ,使乙醚全部挥发。
,使乙醚全部挥发。
步骤Ⅱ:向仪器a中加入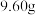 可溶性淀粉
可溶性淀粉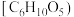 和
和 无氧水,
无氧水, 下使淀粉糊化
下使淀粉糊化 。
。
步骤Ⅲ:糊化完成后,加入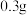 硝酸铈铵作引发剂,静置。
硝酸铈铵作引发剂,静置。
步骤Ⅳ:调节玻璃槽内温度为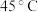 ,加入丙烯酸乙酯
,加入丙烯酸乙酯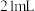 ,继续反应
,继续反应 。
。
步骤V:反应完成后,用无水乙醇洗涤、抽滤,干燥至恒重,得接枝淀粉粗品。
步骤Ⅵ:将得到的接枝淀粉粗品用滤纸包好置于滤纸筒内,在烧瓶中加入 易挥发和易燃的丙酮,加入几粒沸石,控制温度为
易挥发和易燃的丙酮,加入几粒沸石,控制温度为 ,蒸汽于侧管上升,经冷凝回流后滴入样品中,当浸液积满一定量时即由虹吸管溢出,全部流入下部的烧瓶中,如此反复回流
,蒸汽于侧管上升,经冷凝回流后滴入样品中,当浸液积满一定量时即由虹吸管溢出,全部流入下部的烧瓶中,如此反复回流 ,然后将其置于真空干燥箱干燥至恒重得到纯接枝产物
,然后将其置于真空干燥箱干燥至恒重得到纯接枝产物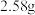 。
。
回答下列问题:
(1)图1中仪器a和仪器b的名称分别为___________ 、___________ 。玻璃槽中的液体适宜选用___________ (填“水”或“植物油”)。
(2)氧气是丙烯酸乙酯和淀粉共聚接枝的阻聚剂,不利于共聚接枝反应的进行。除步骤I中用乙醚排出装置中的空气外,实验中采取的消除氧气对反应影响的措施还有___________ 。
(3)步骤Ⅱ中淀粉糊化过程中有部分淀粉发生水解反应生成葡萄糖,该水解反应的化学方程式为___________ 。
(4)步骤Ⅲ中加入的引发剂硝酸铈铵的化学式为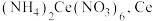 元素的化合价为
元素的化合价为___________ 。
(5)步骤Ⅵ的提取过程不可选用明火直接加热,原因是___________ 。与常规的萃取相比,本实验中采用索氏提取器的优点是___________ 。
实验装置:

实验步骤:
步骤Ⅰ:加入
 乙醚于仪器a中,并用塞子封堵其中两个瓶口,缓慢加热至
乙醚于仪器a中,并用塞子封堵其中两个瓶口,缓慢加热至 ,使乙醚全部挥发。
,使乙醚全部挥发。步骤Ⅱ:向仪器a中加入
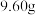 可溶性淀粉
可溶性淀粉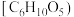 和
和 无氧水,
无氧水, 下使淀粉糊化
下使淀粉糊化 。
。步骤Ⅲ:糊化完成后,加入
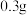 硝酸铈铵作引发剂,静置。
硝酸铈铵作引发剂,静置。步骤Ⅳ:调节玻璃槽内温度为
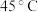 ,加入丙烯酸乙酯
,加入丙烯酸乙酯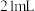 ,继续反应
,继续反应 。
。步骤V:反应完成后,用无水乙醇洗涤、抽滤,干燥至恒重,得接枝淀粉粗品。
步骤Ⅵ:将得到的接枝淀粉粗品用滤纸包好置于滤纸筒内,在烧瓶中加入
 易挥发和易燃的丙酮,加入几粒沸石,控制温度为
易挥发和易燃的丙酮,加入几粒沸石,控制温度为 ,蒸汽于侧管上升,经冷凝回流后滴入样品中,当浸液积满一定量时即由虹吸管溢出,全部流入下部的烧瓶中,如此反复回流
,蒸汽于侧管上升,经冷凝回流后滴入样品中,当浸液积满一定量时即由虹吸管溢出,全部流入下部的烧瓶中,如此反复回流 ,然后将其置于真空干燥箱干燥至恒重得到纯接枝产物
,然后将其置于真空干燥箱干燥至恒重得到纯接枝产物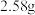 。
。回答下列问题:
(1)图1中仪器a和仪器b的名称分别为
(2)氧气是丙烯酸乙酯和淀粉共聚接枝的阻聚剂,不利于共聚接枝反应的进行。除步骤I中用乙醚排出装置中的空气外,实验中采取的消除氧气对反应影响的措施还有
(3)步骤Ⅱ中淀粉糊化过程中有部分淀粉发生水解反应生成葡萄糖,该水解反应的化学方程式为
(4)步骤Ⅲ中加入的引发剂硝酸铈铵的化学式为
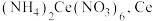 元素的化合价为
元素的化合价为(5)步骤Ⅵ的提取过程不可选用明火直接加热,原因是
您最近一年使用:0次
9 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 探究甲烷气体中是否含有氢气 | 将气体样品通入灼热的氧化铜,然后再通过CuSO4粉末 | 氧化铜固体变为红色,CuSO4粉末变蓝色,说明含有氢气 |
| B | 探究Fe与水蒸气高温反应的固体产物中铁元素的化合价 | 取少量反应后固体于试管中,加足量的稀盐酸溶解,分成两份:一份中滴加硫氰化钾溶液,另一份中滴加酸性高锰酸钾溶液 | 若前者溶液变血红色,后者溶液紫色褪去,则固体产物中铁元素有+2、+3两种化合价 |
| C | 探究乙烯能否被酸性高锰酸钾氧化 | 向乙醇中加入适量浓硫酸制备乙烯,将产生的气体通入酸性高锰酸钾溶液中 | 溶液紫红色褪去,说明乙烯能被酸性高锰酸钾氧化 |
| D | 探究Fe3+、Cu2+对H2O2溶液分解的催化效果强弱 | 在a、b两支试管中各加2mL 5% H2O2溶液,分别滴入0.2mol/L FeCl3溶液和0.3mol/L CuCl2溶液各0.5mL | 若a中产生气泡快于b中,则说明Fe3+的催化效果强于Cu2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021高三·全国·专题练习
名校
解题方法
10 . 高纯氧化铁性能稳定,无毒、无臭、无味,是食品、药品、化妆品常用着色剂。
某实验小组用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)为原料,以萃取剂Y(甲基异丁基甲酮)萃取法制取高纯氧化铁。实验过程中的主要操作步骤如下:
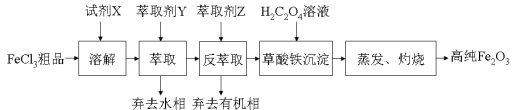
已知:试剂X是浓盐酸,HCl(浓)+FeCl3⇌HFeCl4
请回答下列问题:
(1)据上述实验操作过程判断,下列实验装置中,没有用到的是_______ (填序号)
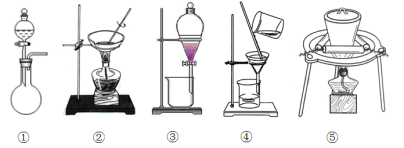
(2)用萃取剂Y萃取的步骤中:
①Ca、Mn、Cu等杂质离子几乎都在_______ (填“水”或“有机”)相中。
②实验时分3次萃取并合并萃取液,这样操作的目的是_______ 。
③以下关于萃取分液操作的叙述中,不正确 的是_______ 。
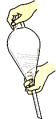
a.溶液中加入Y,转移至分液漏斗中,塞上玻璃塞,如图用力振摇
b.振摇几次后需打开分液漏斗上口的玻璃塞放气
c.经几次振摇并放气后,手持分液漏斗静置待液体分层
d.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体
(3)下列试剂中,作反萃取剂Z的最佳选择是_______ ,反萃取能发生的原因是_______ 。
a.高纯水b.盐酸c.稀硫酸d.酒精
(4)据上述实验操作过程判断,本实验若用适量Na2C2O4溶液代替H2C2O4溶液,是否合理并请说明理由_______ 。
(5)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定(还原产物是Cr3+)。现准确称取Wg样品经酸溶、还原为Fe2+,用0.1000mol•L-1的标准溶液进行滴定。
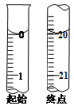
①滴定起始和终点的液面位置如图,则消耗K2Cr2O7标准溶液体积为_______ mL。
②产品中铁的含量为_______ (假设杂质不与K2Cr2O7反应)。
某实验小组用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)为原料,以萃取剂Y(甲基异丁基甲酮)萃取法制取高纯氧化铁。实验过程中的主要操作步骤如下:

已知:试剂X是浓盐酸,HCl(浓)+FeCl3⇌HFeCl4
请回答下列问题:
(1)据上述实验操作过程判断,下列实验装置中,没有用到的是

(2)用萃取剂Y萃取的步骤中:
①Ca、Mn、Cu等杂质离子几乎都在
②实验时分3次萃取并合并萃取液,这样操作的目的是
③以下关于萃取分液操作的叙述中,

a.溶液中加入Y,转移至分液漏斗中,塞上玻璃塞,如图用力振摇
b.振摇几次后需打开分液漏斗上口的玻璃塞放气
c.经几次振摇并放气后,手持分液漏斗静置待液体分层
d.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体
(3)下列试剂中,作反萃取剂Z的最佳选择是
a.高纯水b.盐酸c.稀硫酸d.酒精
(4)据上述实验操作过程判断,本实验若用适量Na2C2O4溶液代替H2C2O4溶液,是否合理并请说明理由
(5)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定(还原产物是Cr3+)。现准确称取Wg样品经酸溶、还原为Fe2+,用0.1000mol•L-1的标准溶液进行滴定。

①滴定起始和终点的液面位置如图,则消耗K2Cr2O7标准溶液体积为
②产品中铁的含量为
您最近一年使用:0次
2021-08-10更新
|
349次组卷
|
5卷引用:考点28 化学实验仪器与基本操作-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点28 化学实验仪器与基本操作-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点29 化学实验基础-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点49 化学实验基础-备战2023年高考化学一轮复习考点帮(全国通用)河南省南阳市第一中学校2022-2023学年高三上学期第一次月考化学试题河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题



