1 . 如图所示为硫元素在自然界中的循环示意图。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.0.1 硫酸溶液含有的 硫酸溶液含有的 数目约为0.2 数目约为0.2 |
B.2.24L 中含有的孤电子对数目为0.2 中含有的孤电子对数目为0.2 |
C.2mol 与1mol 与1mol 充分反应后转移的电子数目为2 充分反应后转移的电子数目为2 |
D.1mol 晶体中所含阳离子数目为 晶体中所含阳离子数目为 |
您最近一年使用:0次
名校
2 . 磷烷 是集成电路、太阳能电池等电子工业生产的原材料。工业上制备
是集成电路、太阳能电池等电子工业生产的原材料。工业上制备 的反应原理为:
的反应原理为: 。
。 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 是集成电路、太阳能电池等电子工业生产的原材料。工业上制备
是集成电路、太阳能电池等电子工业生产的原材料。工业上制备 的反应原理为:
的反应原理为: 。
。 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A. 的 的 溶液中 溶液中 的数目小于0.2 的数目小于0.2 |
B.常温下 的 的 溶液中水电离出的 溶液中水电离出的 |
C.每转移3个电子,生成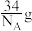 磷烷 磷烷 |
D.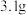 白磷中共价键的数目为0.6 白磷中共价键的数目为0.6 |
您最近一年使用:0次
名校
3 . 设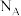 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
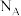 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol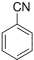 最多消耗 最多消耗 的个数为 的个数为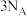 |
B.25℃,101kPa下,44.8LCO和 的混合气体的分子数等于 的混合气体的分子数等于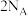 |
| C.80gNaOH溶解在1L水中,所得溶液中溶质的物质的量浓度是2mol/L |
D.铅酸蓄电池的正极质量增加3.2g时,电路中通过的电子数目为 |
您最近一年使用:0次
2024-06-06更新
|
205次组卷
|
2卷引用:辽宁省大连市2023-2024学年高三下学期第二次模拟考试化学试卷
解题方法
4 . TiCl4是制备金属钛的重要中间体,工业制备原理为
 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是

 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.12gC中共价键数目最多为4NA |
B. 中单电子数目为6NA 中单电子数目为6NA |
C.若生成的CO体积为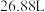 (已换算成标准状况)时,转移电子数目为2.8NA (已换算成标准状况)时,转移电子数目为2.8NA |
D. 溶液中含 溶液中含 数目为3NA 数目为3NA |
您最近一年使用:0次
名校
5 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下,11.2 L  与11.2 L 与11.2 L  在光照下充分反应后,气体分子数为 在光照下充分反应后,气体分子数为 |
B.46 g乙醇中含有的 键的数目为 键的数目为 |
C.1 mol⋅L 的NaClO溶液中含有的 的NaClO溶液中含有的 数目小于 数目小于 |
D.1 mol 完全转化为 完全转化为 转移电子数为 转移电子数为 |
您最近一年使用:0次
名校
6 . 工业上用接触法制备硫酸的流程如图所示,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
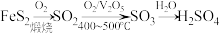
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是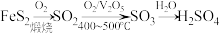
A.流程涉及的元素中,1mol基态原子的未成对电子数最多为 |
B.1mol冰晶体中含有的氢键数目为 |
C. 的 的 溶液中含有的 溶液中含有的 数目为 数目为 |
D.煅烧时,22.4L 参与反应,转移的电子数为 参与反应,转移的电子数为 |
您最近一年使用:0次
2024-05-31更新
|
71次组卷
|
2卷引用:河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)
名校
7 . 《天工开物》记载:“凡火药以硝石、硫磺为主,草木灰为辅……而后火药成声”,涉及的主要反应为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4 L  中含有的π键数为 中含有的π键数为 |
B.1 mol  分子中的电子总数为 分子中的电子总数为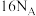 |
C.常温下,1 mol⋅L  溶液中 溶液中 数为 数为 |
D.12 g C完全反应转移电子数为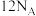 |
您最近一年使用:0次
2024-05-27更新
|
171次组卷
|
2卷引用:2024届贵州省遵义市高三下学期三模化学试题
名校
8 . CaS与 反应可制备
反应可制备 ,反应方程式为
,反应方程式为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 反应可制备
反应可制备 ,反应方程式为
,反应方程式为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4L  含有的质子数为16 含有的质子数为16 |
B.2g由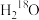 和 和 组成的物质中含有的质子数为 组成的物质中含有的质子数为 |
C.17g  与足量 与足量 溶液充分反应后,将生成96g难溶物 溶液充分反应后,将生成96g难溶物 |
D.0.1mol/L  溶液中的 溶液中的 数目小于0.1 数目小于0.1 |
您最近一年使用:0次
9 . 一种电池的总反应为4Li+2SOCl2=SO2↑+4LiCl+S,设NA为阿伏加德罗常数的值。下列说法错误的是
| A.1molSOCl2中所含的共价键数目为4NA |
| B.每生成1molS,转移2NA个电子 |
| C.标准状况下,22.4LSO2中电子的数目为32NA |
| D.1.0L1.0mol•L-1LiCl溶液中Cl-数目为1.0NA |
您最近一年使用:0次
解题方法
10 . 过量 NaOH 浓溶液和白磷加热煮沸可发生反应: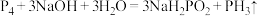 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
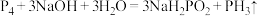 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是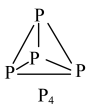
A.46.5g 所含σ键数为9 NA 所含σ键数为9 NA |
B. 为一元酸, 为一元酸, 为酸式盐 为酸式盐 |
C.生成0.2mol P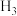 时, 转移电子数为0.6 NA 时, 转移电子数为0.6 NA |
D.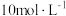 的 NaOH 溶液所含 OH⁻的数目为10 NA 的 NaOH 溶液所含 OH⁻的数目为10 NA |
您最近一年使用:0次



