名校
解题方法
1 . 某河道两旁建有甲、乙两化工厂,某兴趣小组的同学分别收集了两厂排放的污水带回学校进行实验探究,工厂的师傅告诉同学们甲、乙厂排放的工业废水中含有下列离子中的三种(各不相同)
(1)甲同学用pH计(一种测量溶液酸碱性的仪器)测得甲厂的废水明显呈碱性,然后就判断了甲厂中所含有的离子_______ ,乙厂中所含有的离子:_______ 。
(2)乙同学看到工厂师傅给出的离子后,认为可以在某工厂的废水中加入一种金属,从而回收另一种金属。请写出反应过程中的离子方程式:_______ 。
(3)丙同学认为将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子完全转化为沉淀,写出甲、乙两厂废水混合过程中反应的离子方程式_______ ,_______ ,并简述经上述处理后废水的主要作用:_______ 。
| 阳离子 |  、 、 、 、 |
| 阴离子 |  、 、 、 、 |
(2)乙同学看到工厂师傅给出的离子后,认为可以在某工厂的废水中加入一种金属,从而回收另一种金属。请写出反应过程中的离子方程式:
(3)丙同学认为将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子完全转化为沉淀,写出甲、乙两厂废水混合过程中反应的离子方程式
您最近一年使用:0次
2022-11-03更新
|
122次组卷
|
2卷引用:安徽省合肥市第六中学2020-2021学年高一上学期第一次月考化学试题
名校
解题方法
2 . 下列离子方程式改写成化学方程式正确的是
A.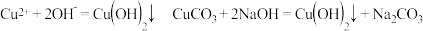 |
B.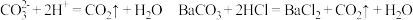 |
C. |
D.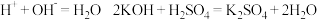 |
您最近一年使用:0次
名校
解题方法
3 . 由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有_______ 。
(2)在进行滴定操作时,KMnO4溶液盛装在_______ (填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,_______ 时达到滴定终点。
(3)滴定过程中发生反应的离子方程式是_______ ;测得该样品中NaNO2的质量分数为_______ 。
(4)以下操作造成测定结果偏高的是_______。
(5)大量的碘富集在海藻中,用水浸取后浓缩。浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中 =
=_______ 。(结果保留两位有效数字)(已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17)
(6)已知: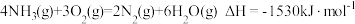 ,
,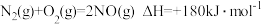 ,写出
,写出 还原
还原 的热化学方程式:
的热化学方程式:_______ 。
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有
(2)在进行滴定操作时,KMnO4溶液盛装在
(3)滴定过程中发生反应的离子方程式是
(4)以下操作造成测定结果偏高的是_______。
| A.滴定管未用KMnO4标准溶液润洗 |
| B.锥形瓶未用待测液润洗 |
| C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失 |
| D.若滴定过程中刚出现颜色变化就停止滴定 |
 =
=(6)已知:
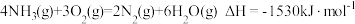 ,
,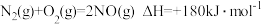 ,写出
,写出 还原
还原 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 下列离子共存或离子方程式的书写正确的是
A.加入KSCN显红色的溶液:K+、NH 、Cl-、S2- 、Cl-、S2- |
| B.“84”消毒液的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
C.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3=2 +3Cl−+4H++H2O +3Cl−+4H++H2O |
D.用热的NaOH溶液溶解S:3S+6OH- 2S2-+ 2S2-+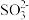 +3H2O +3H2O |
您最近一年使用:0次
名校
解题方法
5 . 化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。某化学兴趣小组用氯气和金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解(易与水反应生成氢氧化铁),受热易升华。装置如下:

(1)仪器a的名称是_______ 。
(2)A中反应的离子方程式是_______ ,D中反应的化学方程式是_______ 。
(3)反应开始时,先点燃_______ 处的酒精灯(填“A”或“D”)。
(4)若无B、C两装置,所得产物中可能含有的杂质是_______ (写化学式)。
(5)F中碱石灰的作用是_______ 。
(6)某学习小组用图E装置收集产品,其缺点为:_______ 。


(1)仪器a的名称是
(2)A中反应的离子方程式是
(3)反应开始时,先点燃
(4)若无B、C两装置,所得产物中可能含有的杂质是
(5)F中碱石灰的作用是
(6)某学习小组用图E装置收集产品,其缺点为:

您最近一年使用:0次
名校
解题方法
6 . “84消毒液”是生活中常见的消毒液,向NaOH溶液中通入氯气可制得该溶液。下列相关叙述不合理的是
| A.该消毒液的有效成分是NaClO |
| B.向装有该消毒液的试管中加入适量稀H2SO4溶液,光照管壁有无色气泡 |
| C.该消毒液与洁厕灵(主要成分为浓HCl)混用,产生有毒Cl2:2H++Cl-+ClO-=Cl2↑+H2O |
D.该消毒液也可用于漂白,漂白原理为:CO2+2ClO-+H2O=2HClO+CO |
您最近一年使用:0次
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
| A.次氯酸钙溶液中通入过量的CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| B.数目相等的溴化亚铁跟氯气反应:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
C.Ca(HCO3)2溶液中加入少量NaOH:Ca2++2HCO +2OH-=CaCO3↓+CO +2OH-=CaCO3↓+CO +2H2O +2H2O |
D.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO =BaSO4↓+H2O =BaSO4↓+H2O |
您最近一年使用:0次
名校
解题方法
8 . 向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断正确的是(不计CO2溶解)


| A.若OB=0,则溶液M为Na2CO3溶液 |
B.若OB=BC,则形成溶液M所发生反应的离子方程式为OH-+CO2=HCO |
C.若3OB=BC,则溶液M中HCO 的数目是CO 的数目是CO 数目的2倍 数目的2倍 |
D.若OB>BC,则溶液M中大量存在的阴离子为CO 和HCO 和HCO |
您最近一年使用:0次
名校
解题方法
9 . 下列离子反应方程式,书写正确的是
A.向碳酸钠溶液中加醋酸: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.向稀硫酸溶液中投入铁粉:2Fe+6H+=2Fe3++3H2↑ |
C.向盐酸中投入碳酸钙: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
D.硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++ +Ba2++2OH﹣=BaSO4↓+2H2O +Ba2++2OH﹣=BaSO4↓+2H2O |
您最近一年使用:0次
2022-10-30更新
|
109次组卷
|
7卷引用:2016-2017学年黑龙江省鹤岗一中高一上期中化学试卷
名校
解题方法
10 . 能正确表示下列变化的离子方程式是
| A.BaCO3溶于盐酸:BaCO3+2H+=Ba2++CO2↑+H2O |
| B.FeCl3溶液腐蚀铜板:2Fe3++3Cu=2Fe+3Cu2+ |
C.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| D.Na与CuSO4水溶液反应:2Na+Cu2+=Cu+2Na+ |
您最近一年使用:0次
2022-10-30更新
|
187次组卷
|
5卷引用:浙江省湖州市吴兴高级中学2020-2021学年高一上学期12月月考化学试题



