名校
1 . 物质因相互融合精彩纷呈,又因独具特色独领风骚。现有下列七种物质:①Cl2②CO2气体③冰醋酸④NaHCO3固体⑤NH4NO3固体⑥红褐色的氢氧化铁胶体⑦氢氧化钡溶液。
(1)上述物质中属于强电解质的有:____ (填序号,以下同)。属于弱电解质的是:____ 。属于非电解质的是:____ 。在该状态下能导电的是:____ 。
(2)将新制氯水滴到pH试纸上,实验现象如图所示,该实验说明H+的扩散速度比HClO分子___ (填“慢”或“快”)。

(3)在土壤胶体中用NH4NO3施肥,研究发现,NO 容易随雨水流失,而NH
容易随雨水流失,而NH 保肥效果好,由此得出土壤胶体的结论是
保肥效果好,由此得出土壤胶体的结论是____ 。
(4)在NaHCO3溶液中加入NaHSO4溶液,反应的离子方程式:____ 。
(5)将NaHCO3溶液加入到氢氧化钡溶液中,至沉淀量最大,写出离子方程式:___ 。
(1)上述物质中属于强电解质的有:
(2)将新制氯水滴到pH试纸上,实验现象如图所示,该实验说明H+的扩散速度比HClO分子

(3)在土壤胶体中用NH4NO3施肥,研究发现,NO
 容易随雨水流失,而NH
容易随雨水流失,而NH 保肥效果好,由此得出土壤胶体的结论是
保肥效果好,由此得出土壤胶体的结论是(4)在NaHCO3溶液中加入NaHSO4溶液,反应的离子方程式:
(5)将NaHCO3溶液加入到氢氧化钡溶液中,至沉淀量最大,写出离子方程式:
您最近一年使用:0次
2022-10-28更新
|
159次组卷
|
2卷引用:山东省青岛第二中学2019-2020学年高一上学期期中考试化学试题
名校
2 . 下列反应的离子方程式书写正确的是
A.用碳酸氢钠治疗胃酸过多:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
B.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢钠溶液混合:Ba2++OH-+HCO =BaCO3↓+H2O =BaCO3↓+H2O |
| C.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
D.用氨水吸收烟气中的二氧化硫:SO2+2OH-=SO +H2O +H2O |
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=____ 。
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)____ c(CH3COO-)(填“>”、“<”或“=”)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显____ 性(填“酸”、“中”或“碱”)。
(4)已知T℃时:CH3COOH CH3COO-+H+Ka=m
CH3COO-+H+Ka=m
H2O=H++OH-Kw=n
则: =
=____ 。
(5)电离常数(25℃):CH3COOH:Ka=1.8 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:____ 。
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显
(4)已知T℃时:CH3COOH
 CH3COO-+H+Ka=m
CH3COO-+H+Ka=mH2O=H++OH-Kw=n
则:
 =
=(5)电离常数(25℃):CH3COOH:Ka=1.8
 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
您最近一年使用:0次
4 . 现有下列十种物质:
①H2②铝③CaO④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH−=H2O,该离子反应对应的化学方程式为___________ 。
(2)⑩在水中的电离方程式为___________ 。
(3)少量的④通入⑥的溶液中反应的离子方程式为___________ 。
(4)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的离子方程式为___________ 。
①H2②铝③CaO④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH−=H2O,该离子反应对应的化学方程式为
(2)⑩在水中的电离方程式为
(3)少量的④通入⑥的溶液中反应的离子方程式为
(4)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是
| A.Cu(OH)2和盐酸;Cu(OH)2和CH3COOH |
| B.BaCl2和Na2SO4;Ba(OH)2和(NH4)2SO4 |
| C.NaHCO3和NaHSO4;Na2CO3和NaHSO4 |
| D.NaHCO3和Ca(OH)2;Ca(HCO3)2和NaOH |
您最近一年使用:0次
2022-10-26更新
|
145次组卷
|
2卷引用:山东省青岛市第十七中学2020-2021学年高一上学期期中考试化学试题
名校
解题方法
6 . 氯气可与强碱反应生成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是_______ ,A管的作用是_______ 。
(2)a中的试剂是_______ ,b中化学反应的离子方程式是_______ ,采用加热的目的是_______ 。
(3)d中的试剂可选用是_______ (填标号),作用是_______ 。
A.CaCl2 B.碱石灰 C.硅胶 D.CuSO4
(4)反应结束后,取出b中试管,经冷却结晶,_______ ,_______ ,干燥,得到KClO3晶体。
(5)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显_______ 色。由此可知该条件下NaClO的氧化能力_______ KClO3(填“大于”或“小于”)。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)a中的试剂是
(3)d中的试剂可选用是
A.CaCl2 B.碱石灰 C.硅胶 D.CuSO4
(4)反应结束后,取出b中试管,经冷却结晶,
(5)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近一年使用:0次
解题方法
7 . 已知A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Cu2+、Na+中的一种,阴离子分别是CO 、NO
、NO 、SO
、SO 、Cl-中的一种(离子不能重复),进行如下实验:
、Cl-中的一种(离子不能重复),进行如下实验:
①分别溶于水,只有C溶液呈蓝色;
②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;
根据①②的实验事实,可推断它们的化学式为:
(1)A_______ ;B_______ 。
(2)加入足量盐酸后D中反应的离子方程式:_______ 。
(3)写出C与NaOH溶液反应的离子方程式:_______ 。
 、NO
、NO 、SO
、SO 、Cl-中的一种(离子不能重复),进行如下实验:
、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;
②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;
根据①②的实验事实,可推断它们的化学式为:
(1)A
(2)加入足量盐酸后D中反应的离子方程式:
(3)写出C与NaOH溶液反应的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 向amolNaOH的溶液中通入bmolCO2,下列说法不正确的是
A.当0.5a<b<a时,溶液中HCO 与CO 与CO 的物质的量之比为(a-b):(2b-a) 的物质的量之比为(a-b):(2b-a) |
B.当a<b时,发生的离子反应为:OH-+CO2=HCO |
C.当a>2b时,发生的离子反应为:2OH-+CO2=CO +H2O +H2O |
D.当2a=3b时,发生的离子反应为:3OH-+2CO2═CO +HCO +HCO +H2O +H2O |
您最近一年使用:0次
2022-10-22更新
|
125次组卷
|
3卷引用:浙江省金华市东阳中学2019-2020学年高一上学期期中考试化学试题
名校
9 . 某兴趣小组对NaHSO4的性质进行了如下的探究,从组成上看,它与NaHCO3类似,应该属于_______ (填“酸”“碱”或“盐”)。
【做出预测】
a.NaHSO4溶液呈碱性
b.NaHSO4溶液能与盐酸反应
c.NaHSO4溶液能与NaOH溶液反应
【对比讨论】
小组内有的同学对比NaHSO4与NaHCO3的组成及复分解反应的条件,认为预测b不正确,它的理由是_______ 。
【实验设计】
【得出结论】
上述预测a、c中,正确的是_______ (填序号)。
【查阅资料】
为了弄清原因,他们查阅了资料,发现NaHSO4在溶液中的电离方程式是NaHSO4=Na++H++ ,他们根据资料又设计了如下三个实验。
,他们根据资料又设计了如下三个实验。
【补充实验】
a.上述实验③中的现象是_______ 。
b.实验④中发生反应的离子方程式为_______ 。
c.对上述实验⑤中发生反应的离子方程式,小组内同学分别写出了解释:
解释I:Ba2++OH-+H++ =BaSO4↓+H2O
=BaSO4↓+H2O
解释II:Ba2++2OH-+2H++ =BaSO4↓+2H2O
=BaSO4↓+2H2O
他们相互争论不下,请教于老师,老师说两个解释都是正确的,一个代表刚开始滴加Ba(OH)2溶液时的反应的离子方程式,另一个代表后来的反应的离子方程式。你认为刚开始滴加时的反应离子方程式应该是_______ (填“解释I”或“解释II”)。
【做出预测】
a.NaHSO4溶液呈碱性
b.NaHSO4溶液能与盐酸反应
c.NaHSO4溶液能与NaOH溶液反应
【对比讨论】
小组内有的同学对比NaHSO4与NaHCO3的组成及复分解反应的条件,认为预测b不正确,它的理由是
【实验设计】
| 序号 | 实验操作 | 实验现象 |
| ① | 取少量的NaHSO4溶液,滴加2-3滴石蕊试液。 | 溶液变红 |
| ② | 向①中溶液中逐滴加入NaOH溶液。 | 溶液先变成紫色,后变成蓝色 |
上述预测a、c中,正确的是
【查阅资料】
为了弄清原因,他们查阅了资料,发现NaHSO4在溶液中的电离方程式是NaHSO4=Na++H++
 ,他们根据资料又设计了如下三个实验。
,他们根据资料又设计了如下三个实验。【补充实验】
| 序号 | 实验操作 | 实验现象 |
| ③ | 向NaHSO4溶液中滴加NaHCO3溶液。 | _______ |
| ④ | 向NaHSO4溶液滴加BaCl2溶液。 | 有白色沉淀生成 |
| ⑤ | 向NaHSO4溶液滴加Ba(OH)2溶液。 | 有白色沉淀生成 |
b.实验④中发生反应的离子方程式为
c.对上述实验⑤中发生反应的离子方程式,小组内同学分别写出了解释:
解释I:Ba2++OH-+H++
 =BaSO4↓+H2O
=BaSO4↓+H2O解释II:Ba2++2OH-+2H++
 =BaSO4↓+2H2O
=BaSO4↓+2H2O他们相互争论不下,请教于老师,老师说两个解释都是正确的,一个代表刚开始滴加Ba(OH)2溶液时的反应的离子方程式,另一个代表后来的反应的离子方程式。你认为刚开始滴加时的反应离子方程式应该是
您最近一年使用:0次
2022-10-18更新
|
105次组卷
|
3卷引用:湖北省蕲春县2020-2021学年高一上学期期中教学质量检测化学试题
名校
解题方法
10 . 下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | 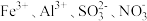 | 过量的盐酸 |  |
| B | 透明溶液中: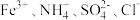 | 过量的铜粉 | 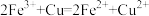 |
| C |  |  溶液 溶液 | 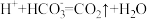 |
| D |  的溶液中: 的溶液中: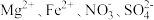 | 双氧水 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-10更新
|
194次组卷
|
14卷引用:陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题
陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题河北省衡水市衡水中学2019届高三上学期期中考试化学试题宁夏石嘴山市第三中学2020届高三上学期期中考试化学试题福建省三明第一中学2020届高三上学期第二次月考化学试题四川省宜宾市叙州区第二中学2020届高三下学期第二次高考适应性考试理综化学试题(已下线)小题必刷04 离子共存——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷06 与量有关的离子方程式书写——2021年高考化学一轮复习小题必刷(通用版)山西省运城市永济涑北中学2020-2021学年高三上学期10月月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二下学期期末考试化学试题(已下线)第05讲 离子共存 离子的检验和推断(精练)-2022年高考化学一轮复习讲练测山西省太原市第五中学2021-2022学年高三上学期11月化学月考试题四川省内江市第六中学2022-2023学年高三上学期入学考试化学试题 广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题陕西省渭南市2023-2024学年高三上学期期中检测化学试题



