20-21高一·全国·课时练习
解题方法
1 . 某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:

(1)补全上述①②③④各步反应的离子方程式
①Mg+2H+═Mg2++H2↑,________________________
②__________________ ,____________________ ;Mg2++2OH-═Mg(OH)2↓
③_____________________ ,CO2+2H2O+ ═Al(OH)3↓+
═Al(OH)3↓+
④________________________ ;
(2)该样品中铝的质量分数是________________________
(3)第②步中加入NaOH溶液不足时,会使测定结果_____________ 第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果________________________ 第④步对沉淀灼烧不充分时,会使测定结果_____________ 。
A.偏高 B.偏低 C.不影响。

(1)补全上述①②③④各步反应的离子方程式
①Mg+2H+═Mg2++H2↑,
②
③
 ═Al(OH)3↓+
═Al(OH)3↓+
④
(2)该样品中铝的质量分数是
(3)第②步中加入NaOH溶液不足时,会使测定结果
A.偏高 B.偏低 C.不影响。
您最近一年使用:0次
名校
2 . KMnO4是化工生产中的一种重要氧化剂。实验室制备并对产品含量进行测定。请回答下列问题:
(一)制备K2MnO4碱性溶液
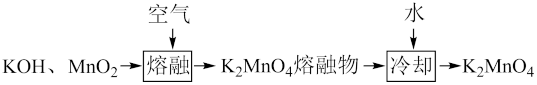 碱性溶液
碱性溶液
(1)“熔融"时应选用的仪器为______ (填选项字母);原因为_____________ 。
a.蒸发皿 b. 普通坩埚 c.铁坩埚 d.烧杯
(2)制备K2MnO4过程中消耗氧化剂和还原剂的物质的量之比为_____________ 。
(二)制备KMnO4
向所得K2MnO4溶液中通入过量CO2,溶液由墨绿色逐渐变为紫黑色并产生黑色沉淀,待反应完全,静置、抽滤,将所得溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得产品。
(3)实验室常用下图装置制备CO2。实验过程中,石灰石应放在装置的______ 部位(填“甲”、“乙”或“丙”);制取CO2时以下操作步骤正确的排列顺序是_______ (填序号)。
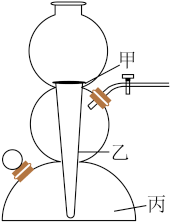
①注入稀盐酸②检查装置气密性③装入大理石
(4)制备KMnO4的离子方程式为_______________________
(三) KMnO4纯度检验
称取2.0gKMnO4产品,配成1000mL溶液,取20.00mL于锥形瓶中,并加入足量稀硫酸酸化,然后用0.02mol·L-1的亚硫酸氢钠(NaHSO3)标准溶液滴定,达到滴定终点时消耗标准溶液的体积为25.00mL。
(5)滴定时发生反应的离子方程式为______________ ;滴定到终点的现象为_____ 产品中KMnO4的质量分数为_______________
(一)制备K2MnO4碱性溶液
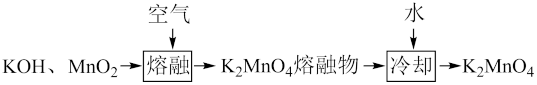 碱性溶液
碱性溶液(1)“熔融"时应选用的仪器为
a.蒸发皿 b. 普通坩埚 c.铁坩埚 d.烧杯
(2)制备K2MnO4过程中消耗氧化剂和还原剂的物质的量之比为
(二)制备KMnO4
向所得K2MnO4溶液中通入过量CO2,溶液由墨绿色逐渐变为紫黑色并产生黑色沉淀,待反应完全,静置、抽滤,将所得溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得产品。
(3)实验室常用下图装置制备CO2。实验过程中,石灰石应放在装置的

①注入稀盐酸②检查装置气密性③装入大理石
(4)制备KMnO4的离子方程式为
(三) KMnO4纯度检验
称取2.0gKMnO4产品,配成1000mL溶液,取20.00mL于锥形瓶中,并加入足量稀硫酸酸化,然后用0.02mol·L-1的亚硫酸氢钠(NaHSO3)标准溶液滴定,达到滴定终点时消耗标准溶液的体积为25.00mL。
(5)滴定时发生反应的离子方程式为
您最近一年使用:0次
2020-10-03更新
|
477次组卷
|
3卷引用:陕西省西安市第一中学2021届高三上学期模拟调研考试化学试题
陕西省西安市第一中学2021届高三上学期模拟调研考试化学试题陕西省宝鸡市凤翔中学2021届高三上学期期中考试化学试题(已下线)专题27 物质制备类综合性实验题(学生版)-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
3 . 为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含 、
、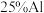 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为______  得到滤渣1的主要成分为
得到滤渣1的主要成分为______ 。
 第
第 步中加入
步中加入 的作用是
的作用是______ ,使用 的优点是
的优点是______ ;调溶液pH的目的是______ 。
 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是______ 。
 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:
甲:滤渣 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
乙:滤渣 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
丙:滤渣2 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
上述三种方案中,______ 方案不可行,原因是______ ;从原子利用率角度考虑,______ 方案更合理。
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式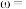
______ 。
 、
、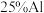 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:  |
| 方法Ⅲ | 用肼 还原新制 还原新制 |
 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为 得到滤渣1的主要成分为
得到滤渣1的主要成分为 第
第 步中加入
步中加入 的作用是
的作用是 的优点是
的优点是 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:甲:滤渣
 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O乙:滤渣
 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O丙:滤渣2
 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O上述三种方案中,
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式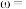
您最近一年使用:0次
名校
解题方法
4 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(C1O2)就是其中一种高效消毒灭菌剂。但其稳定性较差,可转化为NaClO2保存。分别利用吸收法和电解法两种方法得到较稳定的NaClO2。其工艺流程示意图如图所示:

已知:1.纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2.长期放置或高于60℃时NaClO2易分解生成NaClO3和NaCl
(1)步骤1中,生成C1O2的离子方程式是___ ,通入空气的作用是___ 。
(2)方法1中,反应的离子方程式是___ ,利用方法1制NaClO2时,温度不能超过20℃,可能的原因是___ 。
(3)方法2中,NaClO2在___ 生成(选填“阴极”或“阳极”)。
(4)NaClO2的溶解度曲线如图所示,步骤3中从NaClO2溶液中获得NaClO2的操作是___ 。

(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a克样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用bmol•L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为cmL(已知:I2+2S2O32-=2I-+S4O62-)。样品中NaClO2的质量分数为___ 。(用含a、b、c的代数式表小)。在滴定操作正确无误的情况下,测得结果偏高,可能的原因是___ (用离子方程式和文字表示)。
(6)NaClO2使用时,加入稀盐酸即可迅速得到C1O2。但若加入盐酸浓度过大,则气体产物中Cl2的含量会增大,原因是___ 。

已知:1.纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2.长期放置或高于60℃时NaClO2易分解生成NaClO3和NaCl
(1)步骤1中,生成C1O2的离子方程式是
(2)方法1中,反应的离子方程式是
(3)方法2中,NaClO2在
(4)NaClO2的溶解度曲线如图所示,步骤3中从NaClO2溶液中获得NaClO2的操作是

(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a克样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用bmol•L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为cmL(已知:I2+2S2O32-=2I-+S4O62-)。样品中NaClO2的质量分数为
(6)NaClO2使用时,加入稀盐酸即可迅速得到C1O2。但若加入盐酸浓度过大,则气体产物中Cl2的含量会增大,原因是
您最近一年使用:0次
2020-05-15更新
|
529次组卷
|
6卷引用:北京市顺义区2020届高三第二次模拟化学试题
名校
解题方法
5 . 高纯硝酸锶 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:

已知: 滤渣1的成分为
滤渣1的成分为 、
、 ;
; 铬酸
铬酸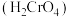 为弱酸。
为弱酸。
 酸浸不能采用高温的原因是
酸浸不能采用高温的原因是____________ ,滤液1的主要溶质是________ 。
 相对于水洗,用浓硝酸洗涤的优点是
相对于水洗,用浓硝酸洗涤的优点是___________ 。
 滤液2中过量的
滤液2中过量的 被
被 还原为
还原为 ,同时放出无污染的气体,写出发生反应的离子方程式:
,同时放出无污染的气体,写出发生反应的离子方程式:________ 。
 已知
已知 类似氢氧化铝,还原后溶液的pH不能大于8的原因是
类似氢氧化铝,还原后溶液的pH不能大于8的原因是 结合离子方程式说明理由
结合离子方程式说明理由
__________ 。
 为了测定滤渣2中
为了测定滤渣2中 的含量,进行以下实验:
的含量,进行以下实验:
mg滤渣2 溶液
溶液
滴定终点时消耗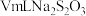 溶液
溶液 已知:
已知: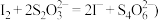 。
。
 滤渣2中
滤渣2中 摩尔质量为
摩尔质量为 的质量分数为
的质量分数为___________  用代数式表示
用代数式表示 。
。
 若加入的HI溶液过量太多,测定结果会
若加入的HI溶液过量太多,测定结果会_________  “偏高”“偏低”或“无影响”
“偏高”“偏低”或“无影响” 。
。
 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
已知:
 滤渣1的成分为
滤渣1的成分为 、
、 ;
; 铬酸
铬酸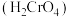 为弱酸。
为弱酸。 酸浸不能采用高温的原因是
酸浸不能采用高温的原因是 相对于水洗,用浓硝酸洗涤的优点是
相对于水洗,用浓硝酸洗涤的优点是 滤液2中过量的
滤液2中过量的 被
被 还原为
还原为 ,同时放出无污染的气体,写出发生反应的离子方程式:
,同时放出无污染的气体,写出发生反应的离子方程式: 已知
已知 类似氢氧化铝,还原后溶液的pH不能大于8的原因是
类似氢氧化铝,还原后溶液的pH不能大于8的原因是 结合离子方程式说明理由
结合离子方程式说明理由
 为了测定滤渣2中
为了测定滤渣2中 的含量,进行以下实验:
的含量,进行以下实验:mg滤渣2
 溶液
溶液
滴定终点时消耗
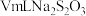 溶液
溶液 已知:
已知: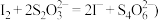 。
。 滤渣2中
滤渣2中 摩尔质量为
摩尔质量为 的质量分数为
的质量分数为 用代数式表示
用代数式表示 。
。 若加入的HI溶液过量太多,测定结果会
若加入的HI溶液过量太多,测定结果会 “偏高”“偏低”或“无影响”
“偏高”“偏低”或“无影响” 。
。
您最近一年使用:0次
2020-02-04更新
|
350次组卷
|
2卷引用:2020届高考化学二轮复习大题精准训练 ——侧重提纯类无机工艺流程题
解题方法
6 . 实验题
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙,氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
I.摩擦剂中氢氧化铝的定性检验:取适量牙膏样品,加水充足搅拌,过滤.
(1)往滤渣中加入过量NaOH溶液,过滤. 氢氧化铝与NaOH溶液反应的离子方程式是_______ .
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.这一过程发生反应的化学方程式依次为:__________________________________ ,__________________________________ .
Ⅱ.牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
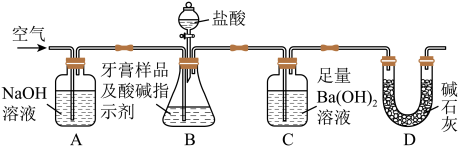
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B,C中的反应物外,还有:_________ .
(4)C中反应生成BaCO3的离子方程式是___________________________________ .
(5)下列各项措施中,不能提高测定准确度的是( ) (填标号).
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A~B之间增添盛有浓硫酸的洗气装置
D.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为________ .
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是_________________ .
(8)装置中U形管D中的碱石灰的作用是_____________________________ .
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙,氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
I.摩擦剂中氢氧化铝的定性检验:取适量牙膏样品,加水充足搅拌,过滤.
(1)往滤渣中加入过量NaOH溶液,过滤. 氢氧化铝与NaOH溶液反应的离子方程式是
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.这一过程发生反应的化学方程式依次为:
Ⅱ.牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B,C中的反应物外,还有:
(4)C中反应生成BaCO3的离子方程式是
(5)下列各项措施中,不能提高测定准确度的是
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A~B之间增添盛有浓硫酸的洗气装置
D.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是
(8)装置中U形管D中的碱石灰的作用是
您最近一年使用:0次
真题
7 . 息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1) 第①步Cu与酸反应的离子方程为______ ;得到滤渣1的主要成分为______ 。
(2) 第②步加H2O2的作用是______ ,使用H2O2的优点是______ ;调溶液pH的目的是使______ 生成沉淀。
(3) 用第③步所得CuSO4·5H2O制备无水CuSO4的方法是______ 。
(4) 由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:

上述三种方案中,______ 方案不可行,原因是______ ;从原子利用率角度考虑,______ 方案更合理。
(5) 探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2+ + H2Y2- = CuY2- + 2H+
①写出计算CuSO4·5H2O质量分数的表达式ω=______ ;
②下列操作会导致CuSO4·5H2O含量的测定结果偏高的是______ 。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子

请回答下列问题:
(1) 第①步Cu与酸反应的离子方程为
(2) 第②步加H2O2的作用是
(3) 用第③步所得CuSO4·5H2O制备无水CuSO4的方法是
(4) 由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:

上述三种方案中,
(5) 探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2+ + H2Y2- = CuY2- + 2H+
①写出计算CuSO4·5H2O质量分数的表达式ω=
②下列操作会导致CuSO4·5H2O含量的测定结果偏高的是
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
您最近一年使用:0次
解题方法
8 .
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象_____ ,写出两步主要反应的离子方程式______
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分_____ 。
(3)第二步失重后的固态残渣是______ ,解释理由______ 。
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分
(3)第二步失重后的固态残渣是
您最近一年使用:0次
解题方法
9 . I.水中溶解氧气的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,反应方程式为2S2O +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 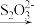 S4O
S4O 。
。
(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:____________________ 。
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为_________ mg·L-1。
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为________ mol/L(保留一位小数),需用量筒量取30%的双氧水_________ mL。
(2)该实验在酸性条件下进行,则实验设计的反应原理是_____________ (用离子方程式表示)。
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为_________ (用含a、b的式子表示)。
 +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 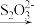 S4O
S4O 。
。(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为
(2)该实验在酸性条件下进行,则实验设计的反应原理是
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
您最近一年使用:0次
名校
10 . 向50g质量分数为10.6%的Na2CO3溶液中,逐滴加入CaCl2稀溶液。测得溶液中离子的数量变化如图。请据此分析以下问题:
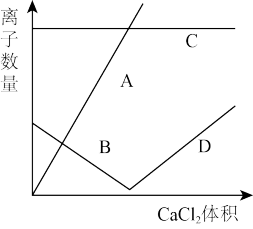
(1)请指出以下曲线表示的离子化学式:
A___________________
C___________________
D___________________
(2)反应的化学反应方程式为_______________________________________ 。
(3)当A、C曲线相交时,生成的沉淀质量为____________ g。

(1)请指出以下曲线表示的离子化学式:
A
C
D
(2)反应的化学反应方程式为
(3)当A、C曲线相交时,生成的沉淀质量为
您最近一年使用:0次
2020-11-19更新
|
226次组卷
|
4卷引用:安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题
安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题江西省南昌市进贤一中2020-2021学年高一上学期第二次月考化学试题(已下线)2.2.2 离子方程式的书写-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)(已下线)1.2.2 离子反应和离子方程式(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)?



