名校
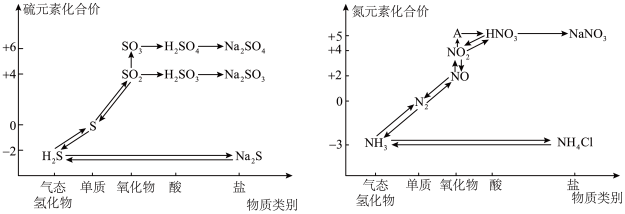
1 . 硫、氮的氧化物都会引起环境问题,越来越引起人们的重视。如图是硫、氮元素的各种价态与物质类别的对应关系:
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为_________ 。
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:_________________________ ;若要除去 中的
中的 可以使用
可以使用_________ (填试剂名称)。
(3)根据A对应的化合价和物质类别,A为_________ (写分子式)。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_________ ,反应的离子方程式为__________________ 。
(5)工业生产中利用氨水吸收 和
和 ,流程如图所示:
,流程如图所示: 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______________________ 。
(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: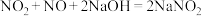
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为________  。若所得溶液
。若所得溶液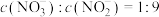 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=_____ 。
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:
 中的
中的 可以使用
可以使用(3)根据A对应的化合价和物质类别,A为
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(5)工业生产中利用氨水吸收
 和
和 ,流程如图所示:
,流程如图所示: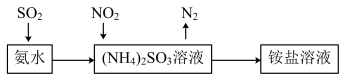
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
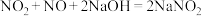
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为 。若所得溶液
。若所得溶液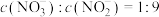 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=
您最近一年使用:0次
2024-03-26更新
|
319次组卷
|
2卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
名校
2 . 大气中 主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将
主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
 主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将
主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是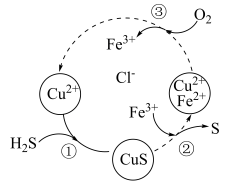
A.过程①中,生成CuS的反应为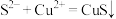 |
B.过程②中, 作还原剂 作还原剂 |
C.过程③中,每消耗1mol  ,转移2mol ,转移2mol  |
D.回收S的总反应为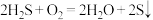 |
您最近一年使用:0次
2024-03-26更新
|
62次组卷
|
3卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
名校
3 . 生活离不开化学。化学与生产生活密切相关,利用所学知识回答下列问题。
I.家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的主要成分。
①食盐(NaCl)②料酒(乙醇)③食醋(乙酸)④碱面( )⑤发酵粉(
)⑤发酵粉( 和明矾)⑥84消毒液(NaClO)⑦洁厕灵(HCl)
和明矾)⑥84消毒液(NaClO)⑦洁厕灵(HCl)
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是___________ 。
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填正确答案标号)。
(3)写出过量③和④反应的离子方程式___________ 。
(4)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________ 。
(5)某同学用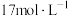 的浓硫酸配制
的浓硫酸配制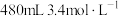 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为___________ mL。
Ⅱ.汽车安全气囊内装有、和 等物质
等物质
(6)当汽车发生严重碰撞时,引发 分解:
分解: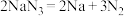 ,
, 的电子式为
的电子式为___________ ,若安全气囊内有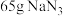 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为___________ L,产生的Na立即与 发生置换反应生成
发生置换反应生成 ,其中氧化剂和还原剂的物质的量比是
,其中氧化剂和还原剂的物质的量比是___________ 。
I.家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的主要成分。
①食盐(NaCl)②料酒(乙醇)③食醋(乙酸)④碱面(
 )⑤发酵粉(
)⑤发酵粉( 和明矾)⑥84消毒液(NaClO)⑦洁厕灵(HCl)
和明矾)⑥84消毒液(NaClO)⑦洁厕灵(HCl)(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)②③的主要成分可以归为一类物质,其分类的依据是___________(填正确答案标号)。
| A.两种物质都是非电解质 | B.两种物质都是电解质 |
| C.两种物质都是氧化物 | D.两种物质都是含碳化合物 |
(4)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
(5)某同学用
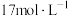 的浓硫酸配制
的浓硫酸配制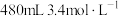 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为Ⅱ.汽车安全气囊内装有、和
 等物质
等物质(6)当汽车发生严重碰撞时,引发
 分解:
分解: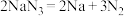 ,
, 的电子式为
的电子式为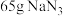 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为 发生置换反应生成
发生置换反应生成 ,其中氧化剂和还原剂的物质的量比是
,其中氧化剂和还原剂的物质的量比是
您最近一年使用:0次
2024-01-25更新
|
98次组卷
|
2卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
解题方法
4 . 黄铁矿(主要成分是 )在细菌和空气的作用下风化,发生以下两个反应过程:
)在细菌和空气的作用下风化,发生以下两个反应过程:

下列说法正确的是
 )在细菌和空气的作用下风化,发生以下两个反应过程:
)在细菌和空气的作用下风化,发生以下两个反应过程:
下列说法正确的是
A. 的 的 模型与空间结构不一致 模型与空间结构不一致 |
B.反应I和Ⅱ中,元素 和 和 都被氧化 都被氧化 |
C.反应Ⅱ中参加反应的 |
D.反应I和Ⅱ中,氧化 转移的电子数之比为 转移的电子数之比为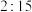 |
您最近一年使用:0次
名校
5 . H3PO2是精细磷化工产品。P4和过量的Ba(OH)2可制备:
①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
②Ba(H2PO2)2+H2SO4=BaSO4↓+2H3PO2
下列推断正确的是
①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
②Ba(H2PO2)2+H2SO4=BaSO4↓+2H3PO2
下列推断正确的是
| A.H3PO2是二元酸 |
| B.H3PO2具有强还原性,在空气中可能被还原成磷酸(H3PO4) |
| C.反应①中氧化剂与还原剂的质量之比为3∶1 |
| D.标况下,反应①中,每生成44.8LPH3分子转移6摩尔电子 |
您最近一年使用:0次
名校
解题方法
6 . 化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(3)SO2是一种酸性氧化物,有类似CO2的性质,写出过量的SO2与NaOH溶液反应的离子方程式:
(4)有人误把洁厕灵(主要成分为盐酸)和“84”消毒液(主要成分为NaClO)一起倒在马桶里,结果产生大量的黄绿色气体。该反应的离子方程式为
(5)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为
 。该反应中被还原的元素是
。该反应中被还原的元素是(6)安全气囊弹出时发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑,该反应中氧化产物与还原产物的物质的量之比为
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-12-21更新
|
195次组卷
|
3卷引用:山西省大同市2023-2024学年高一上学期12月月考化学试题
名校
7 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,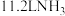 中含有的氢原子数为 中含有的氢原子数为 |
B.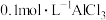 溶液中含有的 溶液中含有的 数目为 数目为 |
C.标准状况下, 完全溶于水形成氯水时,转移电子数小于 完全溶于水形成氯水时,转移电子数小于 |
D.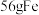 与足量的 与足量的 反应,转移的电子数为 反应,转移的电子数为 |
您最近一年使用:0次
2023-12-21更新
|
481次组卷
|
3卷引用:山西省大同市2023-2024学年高一上学期12月月考化学试题
8 . 向 溶液中逐渐通入
溶液中逐渐通入 ,溶液中某些离子的物质的量随
,溶液中某些离子的物质的量随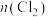 的变化如图所示。
的变化如图所示。

下列说法错误的是
 溶液中逐渐通入
溶液中逐渐通入 ,溶液中某些离子的物质的量随
,溶液中某些离子的物质的量随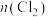 的变化如图所示。
的变化如图所示。
下列说法错误的是
A. 、 、 、 、 、 、 的还原性依次增强 的还原性依次增强 |
B.原溶液的物质的量浓度为 |
C.当 时,溶液中 时,溶液中 |
D.当溶液中 时,反应中共转移0.8mol电子 时,反应中共转移0.8mol电子 |
您最近一年使用:0次
2023-10-28更新
|
204次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期10月月考化学试题
名校
9 .  可作高能燃料的氧化剂,它可由以下反应制得:
可作高能燃料的氧化剂,它可由以下反应制得: (未配平)。下列说法错误的是
(未配平)。下列说法错误的是
 可作高能燃料的氧化剂,它可由以下反应制得:
可作高能燃料的氧化剂,它可由以下反应制得: (未配平)。下列说法错误的是
(未配平)。下列说法错误的是A.氧化性: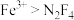 |
B.上述反应中,氧化剂与还原剂的物质的量之比为 |
C.若生成标准状况下 ,转移电子 ,转移电子 |
D. 作氧化剂时,其还原产物可能是 作氧化剂时,其还原产物可能是 和 和 |
您最近一年使用:0次
名校
10 . 污水处理厂处理含 废水的过程分两步进行:①向含
废水的过程分两步进行:①向含 的废水中加入过量
的废水中加入过量 将
将 转化为
转化为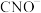 ;②调节①所得溶液为酸性,使
;②调节①所得溶液为酸性,使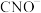 继续被
继续被 转化为两种无污染的气体。下列关于上述过程的叙述错误的是
转化为两种无污染的气体。下列关于上述过程的叙述错误的是
 废水的过程分两步进行:①向含
废水的过程分两步进行:①向含 的废水中加入过量
的废水中加入过量 将
将 转化为
转化为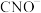 ;②调节①所得溶液为酸性,使
;②调节①所得溶液为酸性,使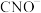 继续被
继续被 转化为两种无污染的气体。下列关于上述过程的叙述错误的是
转化为两种无污染的气体。下列关于上述过程的叙述错误的是A. 的电子式为 的电子式为 |
B.过程①中,生成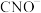 的反应中氧化剂与还原剂的物质的量之比为 的反应中氧化剂与还原剂的物质的量之比为 |
C.过程②中,生成的两种无污染的气体为 和 和 |
D.氧化性: |
您最近一年使用:0次



