解题方法
1 . 今年春晚长沙分会场的焰火璀璨夺目,燃放烟花时发生反应: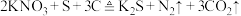 ,同时在火药中会加入
,同时在火药中会加入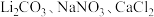 等物质。下列说法正确的是
等物质。下列说法正确的是
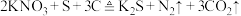 ,同时在火药中会加入
,同时在火药中会加入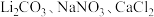 等物质。下列说法正确的是
等物质。下列说法正确的是A.该反应中,氧化产物与还原产物物质的量之比为 |
B.每生成 ,被S氧化的C的物质的量为 ,被S氧化的C的物质的量为 |
C.火药中的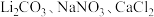 均不参与化学反应 均不参与化学反应 |
| D.燃放烟花对环境没有污染 |
您最近一年使用:0次
名校
解题方法
2 . 中国科学院理化所发现利用Pd-CdS可使PLA(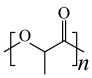 )转化为丙酮酸(
)转化为丙酮酸(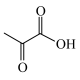 )的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
)的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
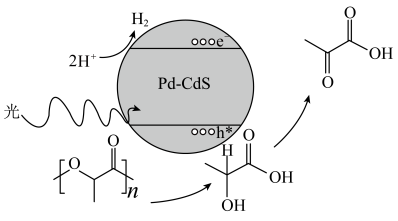
| A.Pd-CdS可作乳酸制备丙酮酸的催化剂 |
| B.在相同条件下,适当增加光的强度有利于加快反应速率 |
| C.整个过程中,氧化产物与还原产物的物质的量之比为1:1 |
| D.当180gPLA完全转化成丙酮酸时,理论上Pd-CdS中至少产生4molh+ |
您最近一年使用:0次
2024-03-27更新
|
593次组卷
|
2卷引用:2024届湖南省益阳市安化县第二中学高三下学期三模化学试题
3 . 重铬酸钾(K2Cr2O7)是一种橘红色结晶性粉末,易溶于水。重铬酸钾是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。常用于制铬矾、火柴、铬颜料、电镀、有机合成等。试回答下列问题:
(1)重铬酸钾中铬元素的化合价___________ ;
(2)工业废水中含有的 ,必须处理达标后才能排放。工业上常用FeSO4做处理剂,反应的离子方程式为6Fe2++2
,必须处理达标后才能排放。工业上常用FeSO4做处理剂,反应的离子方程式为6Fe2++2 +14H+=6Fe3++2Cr3++7H2O,在该反应中被氧化的是
+14H+=6Fe3++2Cr3++7H2O,在该反应中被氧化的是___________ (填离子符号),每处理1mol 时,该反应电子转移的物质的量为
时,该反应电子转移的物质的量为___________ mol。
(1)重铬酸钾中铬元素的化合价
(2)工业废水中含有的
 ,必须处理达标后才能排放。工业上常用FeSO4做处理剂,反应的离子方程式为6Fe2++2
,必须处理达标后才能排放。工业上常用FeSO4做处理剂,反应的离子方程式为6Fe2++2 +14H+=6Fe3++2Cr3++7H2O,在该反应中被氧化的是
+14H+=6Fe3++2Cr3++7H2O,在该反应中被氧化的是 时,该反应电子转移的物质的量为
时,该反应电子转移的物质的量为
您最近一年使用:0次
4 . 为了让宇航员在飞船中得到一个稳定良好的生存环境,一般在飞船内安装盛有Na2O2颗粒的装置产生氧气。下列关于Na2O2的叙述错误的是
| A.Na2O2是一种淡黄色粉末 |
| B.Na2O2与CO2反应时Na2O2只作氧化剂 |
| C.Na2O2与CO2反应若在标准状况下产生2.24LO2,则反应过程中转移电子的物质的量为0.2mol |
| D.Na2O2分别与水和CO2反应产生相同量的O2,需要水和CO2的物质的量相等 |
您最近一年使用:0次
解题方法
5 . BaTiO3是一种压电材料。以BaSO4为原料,采用下列路线可制备粉状BaTiO3。已知“焙烧”后固体产物有BaCl2、易溶于水的BaS和微溶于水的CaS;“沉淀”步骤中生成的沉淀化学式为BaTiO(C2O4)2。

下列说法中错误的是

下列说法中错误的是
| A.“焙烧”步骤中碳粉的主要作用是做还原剂 |
| B.“浸取”步骤中的滤渣为CaS:“酸化”步骤中的酸可用盐酸或稀硫酸 |
C.“沉淀”步骤中发生反应的化学方程式为 |
| D.“热分解”过程中产生的CO和CO2的物质的量之比为1:1 |
您最近一年使用:0次
2023-09-10更新
|
100次组卷
|
2卷引用:湖南省益阳市2024届高三上学期9月教学质量检测化学试题
6 . 实验室中利用固体KClO3和MnO2进行如图实验,下列说法正确的是
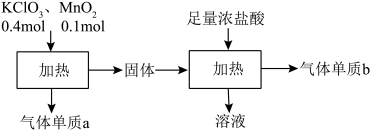

| A.氯元素最多参与了2个氧化还原反应 |
| B.气体a是氧化产物,气体b是还原产物 |
| C.整个过程转移电子数可能为2.6NA |
| D.若用足量浓H2SO4代替浓盐酸,b的物质的量不变 |
您最近一年使用:0次
2023-09-10更新
|
85次组卷
|
2卷引用:湖南省益阳市2024届高三上学期9月教学质量检测化学试题
7 . 中科院发现深海处在微生物作用下的含硫物质的变化过程如图所示(已略去部分不含硫物质)。有关转化过程说法错误的是
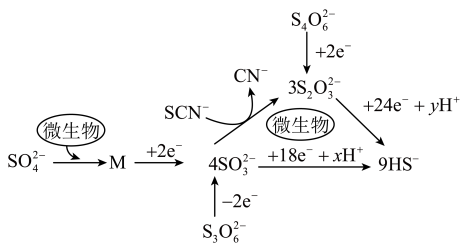

A. 中含有的 中含有的 键与 键与 键的数目之比为 键的数目之比为 |
B.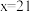 , ,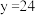 |
C. 既被氧化又被还原 既被氧化又被还原 |
D.理论上每产生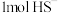 ,转移 ,转移 |
您最近一年使用:0次
名校
解题方法
8 . Na2FeO4具有强氧化性,是一种新型的绿色非氯净水消毒剂,碱性条件下可以稳定存在,酸性条件下会自身分解生成Fe(OH)3。可用Fe(OH)3与NaClO在强碱性条件下制取,某实验小组利用如图所示实验装置,制取Na2FeO4,并验证其处理含CN-废水的能力。

Ⅰ.制取Na2FeO4
(1)仪器D的名称为_____ 。洗气瓶B中盛有的试剂为_____ 。实验开始,先打开分液漏斗_____ (填“A”或“C”)的活塞。
(2)写出大试管中发生反应的离子方程式:_____ 。
(3)三颈烧瓶中的红褐色固体基本消失,得到紫色溶液时,停止通入Cl2。通入氯气的过程中三颈烧瓶中发生反应的离子方程式有:Cl2+2OH-=Cl-+ClO-+H2O、______ 。
Ⅱ.模拟并验证Na2FeO4处理含CN-废水的能力
(4)取一定量Na2FeO4加入试管中,向其中加入0.2mol•L-1的NaCN溶液10mL,CN-被氧化为CO 和N2。充分反应后测得试管中仍有Na2FeO4剩余,过滤。向滤液中加入足量BaCl2溶液,生成白色沉淀,将沉淀过滤干燥后称量,得白色沉淀0.3546g。
和N2。充分反应后测得试管中仍有Na2FeO4剩余,过滤。向滤液中加入足量BaCl2溶液,生成白色沉淀,将沉淀过滤干燥后称量,得白色沉淀0.3546g。
①配制0.2mol•L-1的NaCN溶液,需要的玻璃仪器有______ (填序号,下同)。

②计算NaCN溶液中CN-的去除率为______ (保留两位有效数字)。

Ⅰ.制取Na2FeO4
(1)仪器D的名称为
(2)写出大试管中发生反应的离子方程式:
(3)三颈烧瓶中的红褐色固体基本消失,得到紫色溶液时,停止通入Cl2。通入氯气的过程中三颈烧瓶中发生反应的离子方程式有:Cl2+2OH-=Cl-+ClO-+H2O、
Ⅱ.模拟并验证Na2FeO4处理含CN-废水的能力
(4)取一定量Na2FeO4加入试管中,向其中加入0.2mol•L-1的NaCN溶液10mL,CN-被氧化为CO
 和N2。充分反应后测得试管中仍有Na2FeO4剩余,过滤。向滤液中加入足量BaCl2溶液,生成白色沉淀,将沉淀过滤干燥后称量,得白色沉淀0.3546g。
和N2。充分反应后测得试管中仍有Na2FeO4剩余,过滤。向滤液中加入足量BaCl2溶液,生成白色沉淀,将沉淀过滤干燥后称量,得白色沉淀0.3546g。①配制0.2mol•L-1的NaCN溶液,需要的玻璃仪器有

②计算NaCN溶液中CN-的去除率为
您最近一年使用:0次
2023-03-15更新
|
581次组卷
|
4卷引用:湖南省益阳市安化县第二中学2023届高三三模化学试题
9 . 某强氧化剂XO(OH)2+可将亚硫酸钠氧化成硫酸钠。如果还原2.4×10-3 mol XO(OH)2+,需用30mL0.20mol∙L-1的亚硫酸钠溶液,还原后X的最终化合价为
A. | B. | C. | D.0 |
您最近一年使用:0次
解题方法
10 . 根据金属钠与水(滴有酚酞)反应的现象,下列有关说法错误的是
| A.钠熔化成闪亮的小球,说明钠的熔点低 |
| B.反应后溶液的颜色逐渐变红,说明反应生成了碱 |
| C.该反应中每消耗1mol的钠得到1mol的电子 |
| D.当火灾现场存放有大量金属钠时不能用水来灭火 |
您最近一年使用:0次



