名校
解题方法
1 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,从氧化还原反应的角度探究它们的性质。
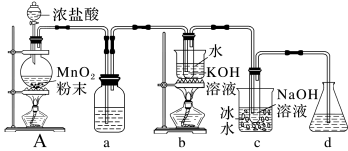
回答下列问题:
(1)A中盛放MnO2粉末的仪器名称是___________ ,A中发生化学反应的方程式是___________ ;
(2)a中盛放的是饱和食盐水,其作用是___________ ;
(3)b中采用的加热方式是___________ ,A中产生的气体与c中NaOH反应的离子方程式___________ ;
(4)d的作用是___________ ;
(5)A中产生气体与b中的KOH反应产生KClO3、KCl和 H2O的方程式___________ 。

回答下列问题:
(1)A中盛放MnO2粉末的仪器名称是
(2)a中盛放的是饱和食盐水,其作用是
(3)b中采用的加热方式是
(4)d的作用是
(5)A中产生气体与b中的KOH反应产生KClO3、KCl和 H2O的方程式
您最近半年使用:0次
2 . 水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)沉淀A的主要成分是__ 。
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__ ,请写出相应的离子方程式:__ 。
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500mol•L-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
___ MnO +
+___ H++___ H2C2O4——___ Mn2++___ CO2+___ H2O
②求该水泥样品中钙的质量分数为___ 。

回答下列问题:
(1)沉淀A的主要成分是
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500mol•L-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
 +
+②求该水泥样品中钙的质量分数为
您最近半年使用:0次
名校
3 . I.下列物质:①氢氧化钠溶液、②铝片、③液态HCl 、④葡萄糖、⑤熔融的NaCl、⑥SO2 气体、⑦碳酸氢钠、 ⑧氧化铝
(1)属于电解质的是______________________ 。(填编号)
(2)能导电的是____________________________________ 。(填编号)
(3)①和②反应的离子方程式________________________________ 。
II.实验室可通过K2Cr2O7溶液测定补铁剂中FeSO4的含量,反应如下K2Cr2O7 +□FeSO4 +□H2SO4 =□Cr2(SO4)3+□Fe2(SO4)3+□K2SO4+□H2O
(1)配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目。_______________
(2)该反应的还原产物为__________ 。若反应中消耗1 mol K2Cr2O7,则转移电子数为______ 。
(1)属于电解质的是
(2)能导电的是
(3)①和②反应的离子方程式
II.实验室可通过K2Cr2O7溶液测定补铁剂中FeSO4的含量,反应如下K2Cr2O7 +□FeSO4 +□H2SO4 =□Cr2(SO4)3+□Fe2(SO4)3+□K2SO4+□H2O
(1)配平上述方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目。
(2)该反应的还原产物为
您最近半年使用:0次
2019-12-29更新
|
81次组卷
|
2卷引用:西藏山南市第二高级中学2021届高三上学期第二次月考理综化学试题
解题方法
4 . 2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢气体。氰化氢的沸点只有26摄氏度,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题
(1)写出氰化钠遇水产生氰化氢的离子方程式________________________________ 。
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式______________________________________________ 。
(3)氰化钠遇到亚硝酸钠能生成两种气体发生爆炸,写出化学反应方程式________________ 。
(4)爆炸残留在废水中的CN- 可以用 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
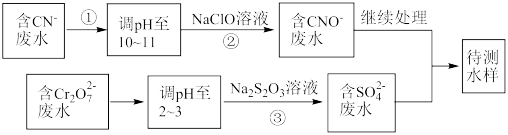
①上述处理废水流程中主要使用的方法是_______ ;
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
②过程②中反应后无气体放出,该反应的离子方程式为_______________________ ;
③步骤③中,每处理0.4 mol 时转移电子2.4 mol,该反应的离子方程式为
时转移电子2.4 mol,该反应的离子方程式为____________ ;
④处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将 还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol
还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol ,需加入amol FeSO4·7H2O,下列结论正确的是
,需加入amol FeSO4·7H2O,下列结论正确的是_______ 。
A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10
(1)写出氰化钠遇水产生氰化氢的离子方程式
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式
(3)氰化钠遇到亚硝酸钠能生成两种气体发生爆炸,写出化学反应方程式
(4)爆炸残留在废水中的CN- 可以用
 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
①上述处理废水流程中主要使用的方法是
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
②过程②中反应后无气体放出,该反应的离子方程式为
③步骤③中,每处理0.4 mol
 时转移电子2.4 mol,该反应的离子方程式为
时转移电子2.4 mol,该反应的离子方程式为④处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将
 还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol
还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol ,需加入amol FeSO4·7H2O,下列结论正确的是
,需加入amol FeSO4·7H2O,下列结论正确的是A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10
您最近半年使用:0次
2016-12-09更新
|
238次组卷
|
2卷引用:2016届西藏山南第二高级中学高三下一模理综化学试卷



