名校
解题方法
1 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:
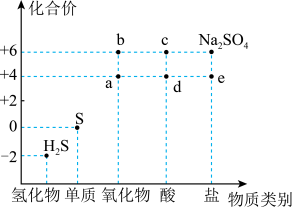
(1)质量相同的a和b,物质的量之比为___________ 。
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为___________ 。
(3)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理: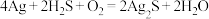 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。
(4)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是___________ (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(5)已知e为正盐,且能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:___________ 。

(1)质量相同的a和b,物质的量之比为
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为
(3)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:
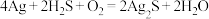 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
(4)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(5)已知e为正盐,且能被酸性
 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:
您最近半年使用:0次
名校
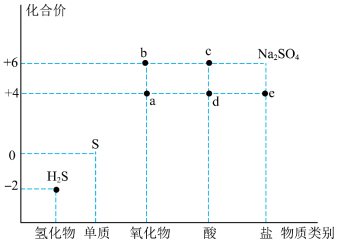
2 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ 。
(2)c的浓溶液能与 反应的化学方程为
反应的化学方程为_____
(3)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(4)实验室洗涤试管壁上附着的硫单质可用热的 溶液洗涤,该反应原理为
溶液洗涤,该反应原理为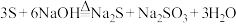
①在该反应中,氧化剂和还原剂的物质的量之比为_____ 。
②向上述反应的溶液中再加入适量的稀 ,会产生淡黄色沉淀,写出该反应的离子方程式:
,会产生淡黄色沉淀,写出该反应的离子方程式:_____ 。
(5)已知e为正盐,能被酸性 氧化为
氧化为 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_____ 。
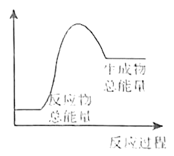
(6)下列反应过程中的能量变化可用图表示的是_____ 。(填序号)
⑤食物因氧化而腐败;⑥ 与
与 反应;⑦氧化钙与水反应
反应;⑦氧化钙与水反应
(2)c的浓溶液能与
 反应的化学方程为
反应的化学方程为(3)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(4)实验室洗涤试管壁上附着的硫单质可用热的
 溶液洗涤,该反应原理为
溶液洗涤,该反应原理为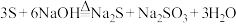
①在该反应中,氧化剂和还原剂的物质的量之比为
②向上述反应的溶液中再加入适量的稀
 ,会产生淡黄色沉淀,写出该反应的离子方程式:
,会产生淡黄色沉淀,写出该反应的离子方程式:(5)已知e为正盐,能被酸性
 氧化为
氧化为 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(6)下列反应过程中的能量变化可用图表示的是
⑤食物因氧化而腐败;⑥
 与
与 反应;⑦氧化钙与水反应
反应;⑦氧化钙与水反应
您最近半年使用:0次
名校
3 . 利用元素的化合价物质类别的坐标系,可以对含某元素的各物质性质有整体的认识。如图是硫元素的常见化合价与部分物质类别的对应关系。______ ;检验其阴离子的方法是______ 。
(2)化石燃料的燃烧可产生 ,在上述图表中它是
,在上述图表中它是______ (图中的字母),为避免过多 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为______ 。
②氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH______ (填“升高”“不变”或“降低”)。
③排放海水与原海水相比,减少的 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为______ 。
(3)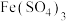 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为______ ;每脱除170kg X,消耗标准状况下 的体积为
的体积为______ L。
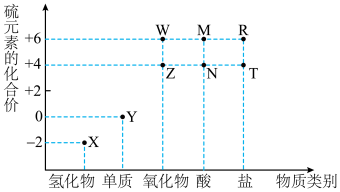
(2)化石燃料的燃烧可产生
 ,在上述图表中它是
,在上述图表中它是 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。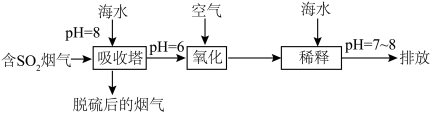
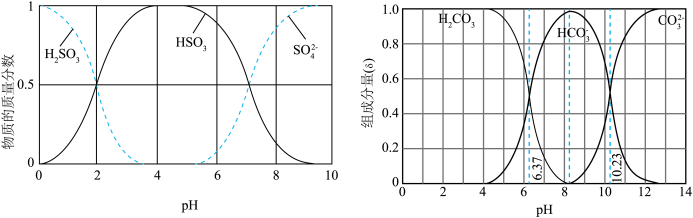
 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为②氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH③排放海水与原海水相比,减少的
 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为(3)
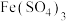 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为 的体积为
的体积为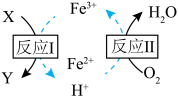
您最近半年使用:0次
4 . 通过“价类二维图”研究物质性质是化学研究的重要方法,下图是氯元素的部分化合价与物质类别的对应关系。

请回答:
(1)X化学式为___________ 。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为 ,则
,则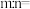
___________ 。
(3) 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率
___________ Z(填“<”或“=”或“>”,消毒效率以单位物质的量得到的电子数表示)。
(4)Y可用于实验室制取 ,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式___________ 。

请回答:
(1)X化学式为
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为
 ,则
,则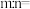
(3)
 与Z都可用于消毒,等物质的量的两种物质,消毒效率
与Z都可用于消毒,等物质的量的两种物质,消毒效率
(4)Y可用于实验室制取
 ,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
,其焰色试验为紫色(透过蓝色钴玻璃观察),请写出由Y与盐酸在加热条件下制备Z的离子方程式
您最近半年使用:0次
名校
5 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
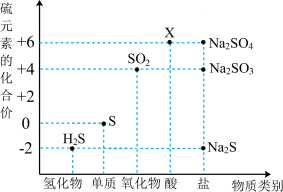
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的___________ 性。从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。小登觉得可以设计实验验证这一推论,具体操作是___________ 。
(3)配平下列反应:___________
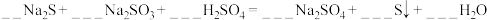 。
。
(4)如图是验证二氧化硫性质的实验装置。
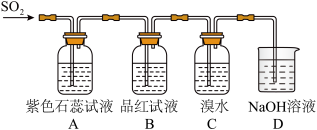
二氧化硫具有:①漂白性、②酸性氧化物性质、③还原性、④氧化性,上述装置中对应表现出的性质是:A中___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(3)配平下列反应:
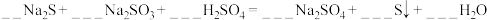 。
。(4)如图是验证二氧化硫性质的实验装置。

二氧化硫具有:①漂白性、②酸性氧化物性质、③还原性、④氧化性,上述装置中对应表现出的性质是:A中
您最近半年使用:0次
名校
解题方法
6 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:
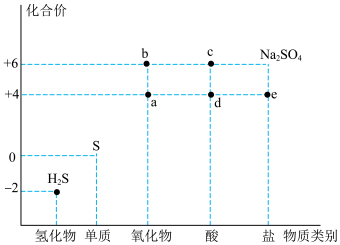
(1)质量相同的a和b,物质的量之比为_______ 。
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为_______ 。
(3)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是_______ (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(4)根据“价类二维图”,下列能与a反应且使a表现还原性的物质是_______ (填序号)。
①NaOH溶液 ② 溶液 ③
溶液 ③ 溶液 ④酸性
溶液 ④酸性 溶液
溶液
(5)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是: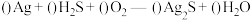 。配平该反应方程式并用单线桥法表示该反应电子转移情况
。配平该反应方程式并用单线桥法表示该反应电子转移情况_______ 。
(6)已知e为正盐,且能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_______ 。

(1)质量相同的a和b,物质的量之比为
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为
(3)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(4)根据“价类二维图”,下列能与a反应且使a表现还原性的物质是
①NaOH溶液 ②
 溶液 ③
溶液 ③ 溶液 ④酸性
溶液 ④酸性 溶液
溶液(5)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是:
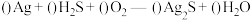 。配平该反应方程式并用单线桥法表示该反应电子转移情况
。配平该反应方程式并用单线桥法表示该反应电子转移情况(6)已知e为正盐,且能被酸性
 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:
您最近半年使用:0次
名校
7 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
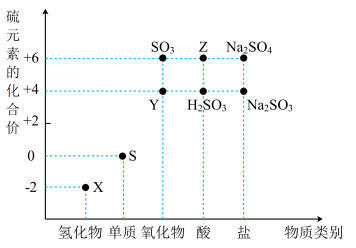
(1)写出化学式:Y______ ,Z______ 。
(2)X与Y能否共存______ (填“能”或“不能”),若不能请写出化学方程式若能请说明理由______ 。
(3) 与足量Z反应的离子方程式
与足量Z反应的离子方程式______ 。
(4)写出Z的浓溶液与木炭发生反应的化学方程式______ 。
(5)Y与稀硝酸反应,硝酸的还原产物为NO,写出反应的化学方程式:______ 。

(1)写出化学式:Y
(2)X与Y能否共存
(3)
 与足量Z反应的离子方程式
与足量Z反应的离子方程式(4)写出Z的浓溶液与木炭发生反应的化学方程式
(5)Y与稀硝酸反应,硝酸的还原产物为NO,写出反应的化学方程式:
您最近半年使用:0次
8 . 太阳能光伏产业蓬勃发展,推动了高纯硅的生产和应用。工业上以硅石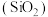 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
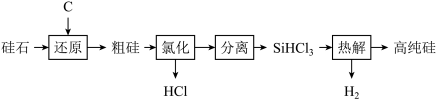
已知: 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。
(1)Si在元素周期表中的位置是_______ 。
(2)“还原”需在高温条件下进行,该反应的化学方程式是_______ 。
(3)“氯化”时的还原产物是_______ (填化学式)。
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是_______ 。
(5)该流程中能循环利用的物质是_______ (填两种)。
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。

①氢氟酸不能用玻璃试剂瓶保存的原因是_______ 。
②酸性条件下,羟胺与 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为_______ 。
③高纯硅样品中铁的质量为_______ 。
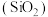 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
已知:
 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。(1)Si在元素周期表中的位置是
(2)“还原”需在高温条件下进行,该反应的化学方程式是
(3)“氯化”时的还原产物是
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是
(5)该流程中能循环利用的物质是
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺
 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。
①氢氟酸不能用玻璃试剂瓶保存的原因是
②酸性条件下,羟胺与
 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为③高纯硅样品中铁的质量为
您最近半年使用:0次
9 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
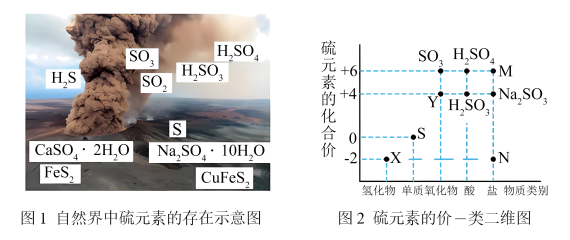
(1)图1中与图2中M、N对应的物质分别是
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)已知
 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与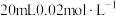 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:(5)过二硫酸钠
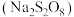 有强氧化性,在碱性条件下
有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为(6)雌黄
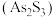 和雄黄
和雄黄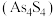 在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。
在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。① 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为
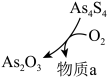
② 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若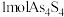 参加反应时,转移
参加反应时,转移 电子,则物质
电子,则物质 为
为
您最近半年使用:0次
10 . 回答下列问题
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为_______ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(3) 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为_______ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为_______ ;若要证明该反应产物有 ,需要采取的操作是
,需要采取的操作是_______ 。
(Ⅱ)氮氧化物( )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。
方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式_______ 。
方案2:
在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
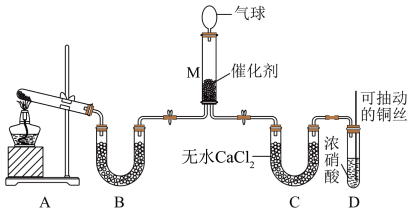
(6)用装置A制备 ,反应的化学方程式为
,反应的化学方程式为_______ ;装置B内的试剂是_______ 。
(7)装置D中发生反应的离子方程式是_______ ;可抽动铜丝的优点是_______ 。
(8)在装置M中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为_______ 。
方案3:
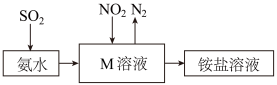
(9)工业生产中利用氨水吸收少量 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______ 。
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为(4)铜和M的浓溶液反应生成Z的化学方程式为
 ,需要采取的操作是
,需要采取的操作是(Ⅱ)氮氧化物(
 )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式
方案2:
在一定条件下
 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
(6)用装置A制备
 ,反应的化学方程式为
,反应的化学方程式为(7)装置D中发生反应的离子方程式是
(8)在装置M中
 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为方案3:
(9)工业生产中利用氨水吸收少量
 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是
您最近半年使用:0次



