解题方法
1 . 利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4,向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(4)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(5)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液,选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4,向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:
(4)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(5)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液,选择合适试剂,并安排合理的顺序
您最近半年使用:0次
名校
2 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。

(1)A、B、C三种物质中,属于电解质的是_______ (填化学式)。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)C可与HCl反应生成A,写出该反应的化学方程式_______ 。
(4)已知D可用于实验室制 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式_______ 。

(1)A、B、C三种物质中,属于电解质的是
(2)写出
 的电离方程式
的电离方程式(3)C可与HCl反应生成A,写出该反应的化学方程式
(4)已知D可用于实验室制
 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式
您最近半年使用:0次
名校
解题方法
3 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

已知:g为钠盐。
(1)按物质性质分类,c、d均属于___________ 氧化物。
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
(3)若将a与c混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)f的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为___________ 。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)c→e→f是硫酸型酸雨的形成途径之一、某地收集的雨水样品在不同时间测得pH如表所示,请用化学方程式解释该雨水样品随时间变化酸性逐渐增强的原因___________ 。

已知:g为钠盐。
(1)按物质性质分类,c、d均属于
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(3)若将a与c混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(4)f的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)c→e→f是硫酸型酸雨的形成途径之一、某地收集的雨水样品在不同时间测得pH如表所示,请用化学方程式解释该雨水样品随时间变化酸性逐渐增强的原因
| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
您最近半年使用:0次
名校
解题方法
4 . I.硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
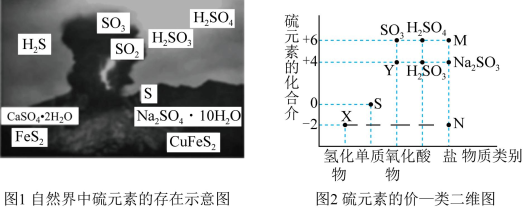
(1)图1中与图2中M、N对应的物质分别是____ 、____ 。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为____ 。
(3)SO2和氯水都有漂白性,为了增强漂白效果,有人将氯水和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为____ 。
II.为探究影响H2O2分解速率的因素,设计如表实验:
(4)实验①③研究的是____ 对H2O2分解速率的影响。
(5)记录实验①在第5min时收集到气体22.4mL(已折算成标准状况),则5min内,v(H2O2)=____ 。
(6)实验①②研究的是____ 对H2O2分解速率的影响。
(7)若向0.4mol/LH2O2中加入少量KI,H2O2的分解机理为:
第一步:H2O2+I-→H2O+IO-
第二步:H2O2+IO-→H2O+O2+I-
据此说明KI在H2O2的分解中起____ 作用。

(1)图1中与图2中M、N对应的物质分别是
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)SO2和氯水都有漂白性,为了增强漂白效果,有人将氯水和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为
II.为探究影响H2O2分解速率的因素,设计如表实验:
| 编号 | 温度 | c(H2O2)/mol·L−1 | V(H2O2)/mL | 催化剂 |
| ① | 20℃ | 0.4 | 10 | 无 |
| ② | 20℃ | 0.8 | 10 | 无 |
| ③ | 30℃ | 0.4 | 10 | 无 |
| ④ | 30℃ | 0.4 | 10 | MnO2 |
(5)记录实验①在第5min时收集到气体22.4mL(已折算成标准状况),则5min内,v(H2O2)=
(6)实验①②研究的是
(7)若向0.4mol/LH2O2中加入少量KI,H2O2的分解机理为:
第一步:H2O2+I-→H2O+IO-
第二步:H2O2+IO-→H2O+O2+I-
据此说明KI在H2O2的分解中起
您最近半年使用:0次
名校
5 . 受疫情影响,自2020年底,芯片短缺就一直占据汽车行业话题榜首。回答相关问题:
Ⅰ.制备高纯硅的主要工艺流程如图所示:
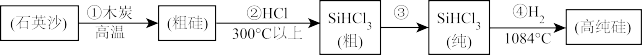
(1)流程①的化学反应方式为___________ 。
(2)流程④的化学反应为置换反应,其化学方程式为___________ 。
Ⅱ.“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(3)硫酸工业排出的尾气(主要含 )有多种处理方式。其中一种方式便是用软锰矿浆
)有多种处理方式。其中一种方式便是用软锰矿浆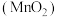 吸收,如图所示。写出“反应1”的化学方程式:
吸收,如图所示。写出“反应1”的化学方程式:___________ 。
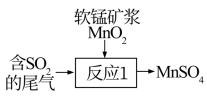
为测定排放气中 的含量,可进行了如下实验:将排放气匀速通入一定量酸性高锰酸钾溶液中,进行相关计算,试写出该反应的离子方程式:
的含量,可进行了如下实验:将排放气匀速通入一定量酸性高锰酸钾溶液中,进行相关计算,试写出该反应的离子方程式:___________ 。
(4)在一定条件下, 可将
可将 转化为无污染的物质。写出
转化为无污染的物质。写出 与
与 在一定条件下反应的化学方程式:
在一定条件下反应的化学方程式:___________ 。
Ⅲ.如图是氮元素的几种化合价与物质类别的对应关系:
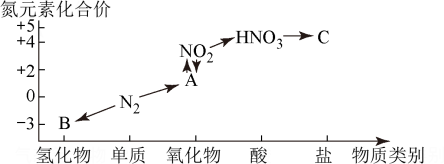
回答下列问题:
(5)实验室制取物质B的化学方程式为___________ 。
(6) 与水反应生成物质A的离子方程式为
与水反应生成物质A的离子方程式为___________ 。
Ⅰ.制备高纯硅的主要工艺流程如图所示:
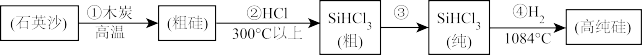
(1)流程①的化学反应方式为
(2)流程④的化学反应为置换反应,其化学方程式为
Ⅱ.“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(3)硫酸工业排出的尾气(主要含
 )有多种处理方式。其中一种方式便是用软锰矿浆
)有多种处理方式。其中一种方式便是用软锰矿浆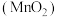 吸收,如图所示。写出“反应1”的化学方程式:
吸收,如图所示。写出“反应1”的化学方程式:
为测定排放气中
 的含量,可进行了如下实验:将排放气匀速通入一定量酸性高锰酸钾溶液中,进行相关计算,试写出该反应的离子方程式:
的含量,可进行了如下实验:将排放气匀速通入一定量酸性高锰酸钾溶液中,进行相关计算,试写出该反应的离子方程式:(4)在一定条件下,
 可将
可将 转化为无污染的物质。写出
转化为无污染的物质。写出 与
与 在一定条件下反应的化学方程式:
在一定条件下反应的化学方程式:Ⅲ.如图是氮元素的几种化合价与物质类别的对应关系:

回答下列问题:
(5)实验室制取物质B的化学方程式为
(6)
 与水反应生成物质A的离子方程式为
与水反应生成物质A的离子方程式为
您最近半年使用:0次
名校
6 . 利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:
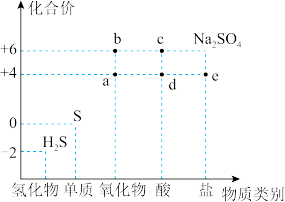
(1)将H2S与a混合,每生成9.6g固体,反应中转移的电子的物质的量为_______ mol。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)将a排入大气中会引起_______ 。
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4.该反应中的氧化剂是_______ (填化学式)。向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序:_______ (填序号)。

(1)将H2S与a混合,每生成9.6g固体,反应中转移的电子的物质的量为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)将a排入大气中会引起
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4.该反应中的氧化剂是
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序:
您最近半年使用:0次
7 . 利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:
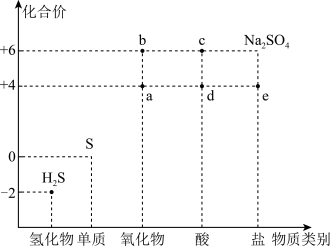
(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)将a排入大气中会引起_______ 。
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是_______ (填化学式)。向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)将a排入大气中会引起
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序
您最近半年使用:0次
名校
8 . 非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硫和氮等元素的踪迹。
Ⅰ.利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b,物质的量之比为_______ 。
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______。
(3)已知e为正盐,且能被酸性K2Cr2O7氧化为Na2SO4,Cr2O 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:_______ 。
Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
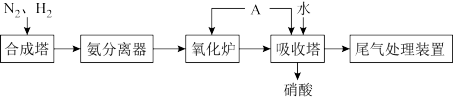
(4)写出氧化炉中的化学反应方程式_______ 。
(5)向吸收塔中通入A的作用_______ 。
(6)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用_______ (填化学式)溶液吸收。
(7)取一定量制取的硝酸加水稀释到50mL,加入过量的铜充分反应,再向溶液中加入足量的稀硫酸,最终共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),铜仍有剩余,将气体充入0.125molO2并倒扣于水槽中,水刚好充满整支试管,则原稀释后的硝酸的物质的量浓度是_______ mol/L,反应溶解的铜有_______ g。
Ⅰ.利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b,物质的量之比为
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______。
| A.H2S溶液 | B.CaCl2溶液 |
| C.H2O2溶液 | D.饱和Na2CO3溶液 |
 被还原为Cr3+,写出此反应的离子方程式:
被还原为Cr3+,写出此反应的离子方程式:Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(4)写出氧化炉中的化学反应方程式
(5)向吸收塔中通入A的作用
(6)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用
(7)取一定量制取的硝酸加水稀释到50mL,加入过量的铜充分反应,再向溶液中加入足量的稀硫酸,最终共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),铜仍有剩余,将气体充入0.125molO2并倒扣于水槽中,水刚好充满整支试管,则原稀释后的硝酸的物质的量浓度是
您最近半年使用:0次
名校
9 . 下列物质应用和所涉及的反应均正确且有对应关系的是
| 选项 | 物质应用 | 涉及反应 |
| A | 纯碱溶液浸泡锅炉水垢 |  |
| B | 硫化氢除去水中的 | 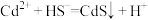 |
| C | 四氯化钛溶液制备二氧化钛水合物 | 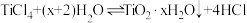 |
| D | 酸性 溶液滴定双氧水 溶液滴定双氧水 | 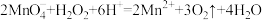 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 下列古诗或古文中的描述与化学方程式对应关系不正确的是
A.丹砂烧之成水银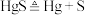 |
B.爆竹声中一岁除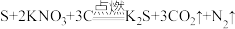 |
C.炉火照天地红星乱紫烟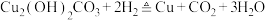 |
D.曾青得铁化为铜 |
您最近半年使用:0次



