名校
1 . 已知A常温常压下为无色液体,A为气体时与R反应生成B和E,M、R是两种常见的金属,M是地壳中含量最多的金属元素的单质,T是淡黄色固体,B. C是无色无味的气体,E是具有磁性的黑色晶体,H是红褐色固体。
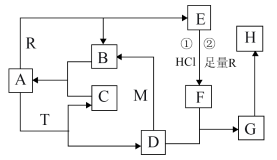
(1)物质T的化学式为___________ 。15.6g T与足量的A反应电子转移数为___________ 个(已知:阿伏伽德罗常数为NA)。
(2)D和M在溶液中反应生成B的离子反应方程式为___________ 。
(3)G在潮湿空气中转化为H的化学方程式为___________ 。
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为_________ 。
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为___________ g。

(1)物质T的化学式为
(2)D和M在溶液中反应生成B的离子反应方程式为
(3)G在潮湿空气中转化为H的化学方程式为
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近一年使用:0次
2023-12-15更新
|
409次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
名校
解题方法
2 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
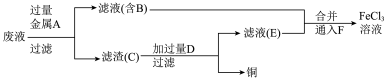
滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
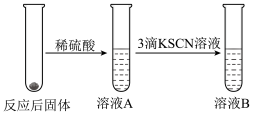
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(2)实验I中反应的化学方程式是___________ 。
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(4)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验I | 实验II |
 |  |
(2)实验I中反应的化学方程式是
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是
(4)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
名校
解题方法
3 . 下列有关铁和铁的化合物的叙述中,正确的是

| A.铁的化学性质比较活泼,它能与许多物质发生化学反应,因此铁在自然界中只能以化合态存在 |
| B.Fe3O4是一种红棕色粉末,俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料 |
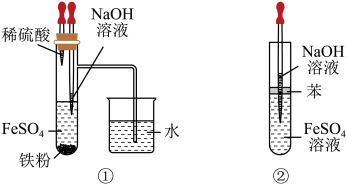
| C.Fe(OH)2在空气中容易被氧化,如图①②都能较长时间看到Fe(OH)2白色沉淀 |
| D.往某溶液中先加入氯水,再加入KSCN溶液,发现溶液变成红色,证明原溶液中含有Fe3+ |
您最近一年使用:0次
2023-04-06更新
|
377次组卷
|
4卷引用:新疆乌鲁木齐市第四中学2022-2023学年高一下学期期中阶段诊断测试化学试题
新疆乌鲁木齐市第四中学2022-2023学年高一下学期期中阶段诊断测试化学试题云南省玉溪第一中学2022-2023学年高一上学期第一月考化学试题 (已下线)第14讲 铁的氢氧化物和铁盐、亚铁盐-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)
名校
4 . 如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2被氧化时的颜色变化,实验时必须使用铁屑、6mol/L硫酸,其他试剂任选。回答下列问题:
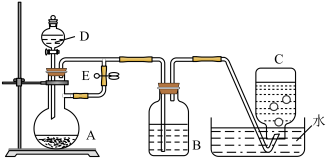
(1)仪器D的名称为________ ,该仪器中需要放入__________ ,装置B中盛有一定量的NaOH溶液,装置A中应预先加入的试剂是______ ,装置A中发生反应的离子方程式为___________ 。
(2)实验开始时应先将止水夹E______ (填“打开”或“关闭”),装置C中收集到的气体主要为______ ;待装置中空气排尽后,将止水夹E______ (填“打开”或“关闭”),此时装置B中可能发生的化学反应是:__________ (用离子方程式表示)。
(3)拔去装置B中的橡胶塞,使空气进入,此时B中发生反应的化学方程式为_________ 。

(1)仪器D的名称为
(2)实验开始时应先将止水夹E
(3)拔去装置B中的橡胶塞,使空气进入,此时B中发生反应的化学方程式为
您最近一年使用:0次
2023-01-11更新
|
130次组卷
|
2卷引用:新疆生产建设兵团第二中学2022-2023学年高一上学期期末考试化学试题
5 . 部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取黄绿色气体的主要方法之一,H的焰色呈黄色,请完成下列填空。
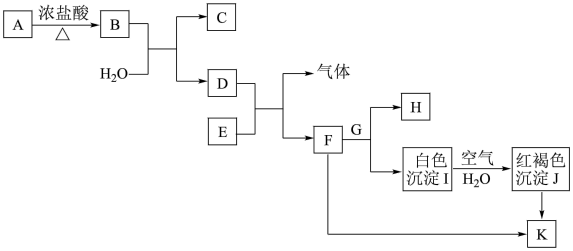
(1)检验F溶液中阳离子的试剂是_______ 。若Cu2+中含有F中阳离子的杂质,应加入_______ (填化学式)除杂。
(2)Ⅰ转化为J的化学方程式为_______ 。
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
(4)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为_______ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是_______ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式_______ 。
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为_______ 。

(1)检验F溶液中阳离子的试剂是
(2)Ⅰ转化为J的化学方程式为
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
| A.胶体L具有丁达尔效应 | B.胶体L的分散质粒子直径为 |
| C.胶体L是均一的分散系 | D.胶体L比K的饱和溶液颜色深 |
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
解题方法
6 . A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,相关物质间的关系如下图所示。
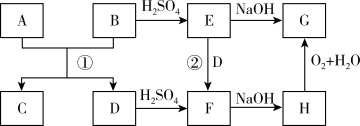
(1)H的化学式是_______ 。
(2)反应①的化学方程式是_______ 。
(3)H转化为G的实验现象是_______ ;化学方程式为:_______
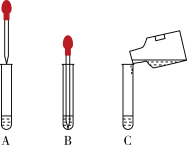
(4)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是_______ (填下图字母)

(1)H的化学式是
(2)反应①的化学方程式是
(3)H转化为G的实验现象是
(4)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是

您最近一年使用:0次
2022-04-05更新
|
165次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第一中学2021--2022学年高一上学期期末考试化学试题
名校
7 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
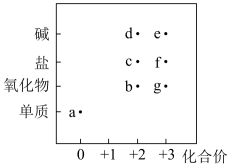

| A.向c溶液中滴加KSCN溶液,可证明c溶液是否变质 |
B.固体g溶于氢碘酸的离子方程式为 |
| C.通过化合反应或复分解反应均能直接得到e |
| D.可存在c→d→e→f→c的循环转化关系 |
您最近一年使用:0次
2021-11-26更新
|
686次组卷
|
5卷引用:新疆维吾尔自治区乌鲁木齐市第一中学2021--2022学年高一上学期期末考试化学试题
名校
8 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现血红色。

(1)物质A的化学式为___________ ,F化学式为___________ ;
(2)B和R在溶液中反应生成F的离子方程式为___________ ;
(3)H在潮湿空气中变成M的实验现象是___________ ;
(4)A和水反应生成B和C的化学方程式为_____ ,由此反应可知A有作为____ 的用途;

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的化学方程式为
您最近一年使用:0次
名校
9 . 下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、6 mol/L硫酸溶液、NaOH溶液。下列说法错误的是( )
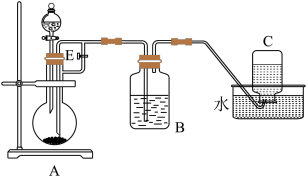
| A.B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑 |
| B.实验开始时应先将活塞E关闭 |
| C.生成Fe(OH)2的操作为:关闭E,使A中溶液压入B瓶中 |
| D.取下装置B中的橡皮塞,使空气进入,有关反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
您最近一年使用:0次
2016-12-09更新
|
1830次组卷
|
16卷引用:新疆乌鲁木齐市第四中学2021-2022学年高一上学期期末考试化学试题
新疆乌鲁木齐市第四中学2021-2022学年高一上学期期末考试化学试题2015-2016学年重庆市第一中学高一上学期期末化学试卷2016-2017学年河北省石家庄市第一中学高一上学期期末考试化学试卷河北省阜城中学2017-2018学年高一上学期第四次月考化学试题(已下线)第5单元 常见的金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题浙江省绍兴市2021-2022学年高一上学期期末调测化学试题(已下线)【教材实验热点】04 Fe(OH)2与Fe(OH)3胶体的制备(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)湖南省长沙市实验中学2022-2023学年高一上学期期末考试化学试题(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)四川省绵阳市南山中学2022-2023学年高一上学期12月线上测试化学试题天津市新华中学2023-2024学年高一上学期第二次月考化学试卷广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷四川省雅安市天立学校2023-2024学年高一上学期第三次教学质量检测化学试题
名校
解题方法
10 . 铁及其化合物在日常生活中很常见
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
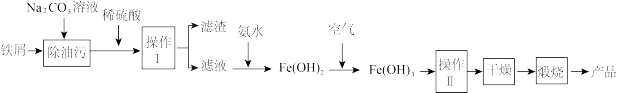
回答下列问题:
①操作II所包含的两项主要基本操作是____________ 。上述流程中,Fe(OH)2转化成Fe(OH)3时的化学方程式为__________________________________ 。
②将FeCl2溶液高温水解、氧化也可直接制得氧化铁,请写出反应的化学方程式:_______________ 。
(2)有些同学认为用KMnO4溶液能进行绿矾(FeSO4·7H2O)产品中铁元素含量的测定,反应的离子方程式为:___________ ,该滴定过程中_____ (填“是”或“否”)还需要指示剂。
实验步骤如下:
a.考虑绿矾产品可能因为保存不当被空气中氧气所氧化,所以事先取少量绿矾产品溶于水,滴加_____ 溶液进行验证。
b.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
c.量取25.00mL待测溶液于锥形瓶中;
d.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
请完成下列问题:
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需__________________________ 。
②某同学设计的下列滴定方式,最合理的是________ (夹持部分略去)(填字母序号)。
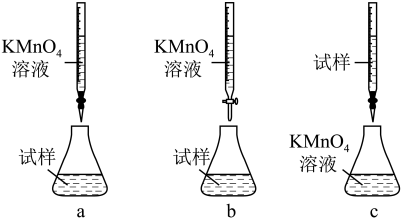
③计算上述样品中FeSO4·7H2O的质量分数为_____________ 。
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
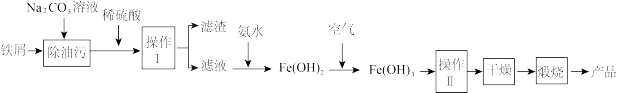
回答下列问题:
①操作II所包含的两项主要基本操作是
②将FeCl2溶液高温水解、氧化也可直接制得氧化铁,请写出反应的化学方程式:
(2)有些同学认为用KMnO4溶液能进行绿矾(FeSO4·7H2O)产品中铁元素含量的测定,反应的离子方程式为:
实验步骤如下:
a.考虑绿矾产品可能因为保存不当被空气中氧气所氧化,所以事先取少量绿矾产品溶于水,滴加
b.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
c.量取25.00mL待测溶液于锥形瓶中;
d.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
请完成下列问题:
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②某同学设计的下列滴定方式,最合理的是

③计算上述样品中FeSO4·7H2O的质量分数为
您最近一年使用:0次
2016-12-09更新
|
340次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2022-2023学年高三上学期11月月考化学试题



