1 . 氢元素的单质及其化合物与人们的日常生活及化工生产息息相关。回答下列问题:
(1)已知氢气与氧气反应生成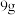 液态水时放出的热量为
液态水时放出的热量为 ,生成
,生成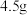 气态水时放出的热量为
气态水时放出的热量为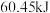 。
。
①写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:__________ 。
②

__________  。
。
(2)利用甲烷将氮的氧化物转化为 和
和 ,有关反应的热化学方程式为:
,有关反应的热化学方程式为:
ⅰ.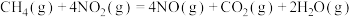
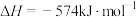 ;
;
ⅱ.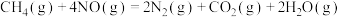
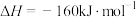
①反应ⅰ中生成物的总键能______ (填“>”“<”或“=”)反应物的总键能,利于该反应自发进行的条件为__________ (填“高温”“低温”或“任意条件”)。
② 直接将
直接将 还原为
还原为 并生成气态水的热化学方程式为
并生成气态水的热化学方程式为__________ 。
(3)在25℃、 下,
下,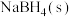 与
与 反应生成
反应生成 和
和 ,已知每消耗
,已知每消耗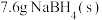 放热
放热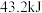 ,该反应的热化学方程式为
,该反应的热化学方程式为__________ 。
(1)已知氢气与氧气反应生成
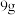 液态水时放出的热量为
液态水时放出的热量为 ,生成
,生成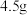 气态水时放出的热量为
气态水时放出的热量为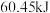 。
。①写出表示
 燃烧热的热化学方程式:
燃烧热的热化学方程式:②


 。
。(2)利用甲烷将氮的氧化物转化为
 和
和 ,有关反应的热化学方程式为:
,有关反应的热化学方程式为:ⅰ.
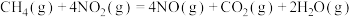
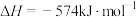 ;
;ⅱ.
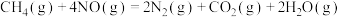
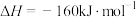
①反应ⅰ中生成物的总键能
②
 直接将
直接将 还原为
还原为 并生成气态水的热化学方程式为
并生成气态水的热化学方程式为(3)在25℃、
 下,
下,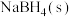 与
与 反应生成
反应生成 和
和 ,已知每消耗
,已知每消耗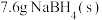 放热
放热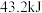 ,该反应的热化学方程式为
,该反应的热化学方程式为
您最近一年使用:0次
2023-05-24更新
|
176次组卷
|
2卷引用:江西省部分学校2023-2024学年高二上学期10月月考化学试题
名校
2 . 已知:CO2氧化C2H6制C2H4的主反应热化学方程式为:
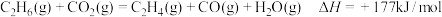
该反应的历程分为如下两步:
反应①: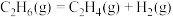 (快反应)
(快反应) 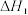
反应②: (慢反应)
(慢反应) 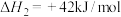
下列说法正确的是
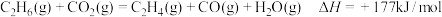
该反应的历程分为如下两步:
反应①:
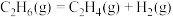 (快反应)
(快反应) 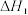
反应②:
 (慢反应)
(慢反应) 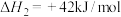
下列说法正确的是
A.反应①的活化能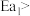 反应②的活化能 反应②的活化能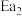 |
B.相比于提高 ,提高 ,提高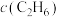 对主反应速率影响更大 对主反应速率影响更大 |
C.将 液化分离,可以提高反应物的转化率 液化分离,可以提高反应物的转化率 |
D.若反应①的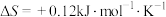 ,则该反应自发进行的最高温度T=1125K ,则该反应自发进行的最高温度T=1125K |
您最近一年使用:0次
2023-05-15更新
|
299次组卷
|
2卷引用:江西省丰城中学2023-2024学年高二创新班上学期开学考试化学试题
名校
3 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法错误的是
| A.氢能有可能成为人类未来的主要能源 |
B.反应 的 的 |
C.氢氧燃料电池放电过程中消耗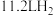 ,则转移电子的数目约为 ,则转移电子的数目约为 |
D.反应 的 的 反应中断裂旧共价键的键能之和一反应中形成新共价键的键能之和 反应中断裂旧共价键的键能之和一反应中形成新共价键的键能之和 |
您最近一年使用:0次
2023-04-23更新
|
133次组卷
|
3卷引用:江西省吉安市多校联考2023-2024学年高二下学期3月月考化学试题
4 . 下列叙述中正确的是
A.向饱和的AgCl、AgBr混合液中加入少量AgNO3,溶液中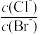 不变 不变 |
| B.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| C.在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu |
D.反应2A(g)+B(s)=C(g)+D(s)在一定条件下可自发进行,则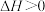 |
您最近一年使用:0次
解题方法
5 . 下列说法错误的是
| A.合成氨反应采取循环操作主要是为了提高化学反应速率 |
B.  、 、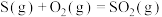  ,则 ,则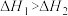 |
C.反应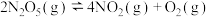  ,能自发进行的原因是 ,能自发进行的原因是 |
D.一定温度下,对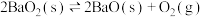 平衡体系缩小体积,再次达到平衡时 平衡体系缩小体积,再次达到平衡时 不变 不变 |
您最近一年使用:0次
2023-02-21更新
|
191次组卷
|
6卷引用:江西省部分学校2023-2024学年高二下学期开学考试化学试题
江西省部分学校2023-2024学年高二下学期开学考试化学试题河南省商开大联考2022~2023学年高二上学期期末考试化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)河北省沧州市2023-2024学年高二上学期12月月考化学试题陕西省榆林市府谷县府谷中学2023-2024学年高二下学期开学化学试题安徽省明光市第二中学2023-2024学年高二上学期期中考试化学试卷
解题方法
6 . 下列说法正确的是
| A.在合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
B.恒温下进行的反应2NO2(g) N2O4(g)达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大 N2O4(g)达平衡时,缩小容器体积再达平衡时,气体的颜色比第一次平衡时的深,NO2的体积分数比原平衡大 |
| C.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0 |
| D.增大反应物浓度可增大活化分子百分数,所以反应速率增大 |
您最近一年使用:0次
14-15高二上·湖北武汉·期末
名校
解题方法
7 . 分析下列反应,在任何温度下均能自发进行的是
| A.2N2(g)+O2(g)=2N2O(g) ΔH=+163 kJ·mol-1 |
| B.2Ag(s)+Cl2(g)= 2AgCl(s) ΔH=-127 kJ·mol-1 |
| C.2HgO(s)=2Hg(l)+O2(g) ΔH=+91 kJ·mol-1 |
| D.2H2O2(l)=O2(g)+2H2O(l) ΔH=-98 kJ·mol-1 |
您最近一年使用:0次
2023-02-21更新
|
677次组卷
|
76卷引用:2016-2017学年江西省新余市第一中学高二下学期入学考试化学试卷
2016-2017学年江西省新余市第一中学高二下学期入学考试化学试卷江西省宜春九中(外国语学校)2019-2020学年高二上学期期中考试化学试题江西省赣州市于都二中2019-2020学年高二上学期第三次月考化学试题江西省上高二中2020-2021学年高二上学期第二次月考化学试题江西省抚州创新实验学校2021-2022学年高二上学期期末考试化学试题(已下线)2013-2014学年湖北省武汉市部分学校高二上学期期末考试化学试卷(已下线)2014秋河北省成安一中、临漳一中、永年二中高二上学期期中联考化学试卷2015-2016学年甘肃省张掖二中高二上学期10月月考化学试卷2015-2016学年黑龙江哈尔滨六中高二上期中测试化学试卷2015-2016学年浙江台州中学高二上第三次统练化学试卷2015-2016学年贵州省大方一中高二上学期期末化学试卷2016-2017学年河南省洛阳高级中学高二上9月月考化学卷2016-2017学年河北省唐山市开滦一中高二上10月月考化学试卷 2016-2017学年陕西西安中学高二实验班上期中化学卷2016-2017学年西藏拉萨中学高二上月考三化学卷2016-2017学年广西桂林市桂林中学高二下学期开学考试化学试卷辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷河南省林州市第一中学分校(林虑中学)2017-2018学年高二上学期开学检测化学试题河北省故城县高级中学2017-2018学年高二9月月考化学试题湖北省襄阳市第四中学2017-2018学年高二10月月考化学试题湖北省沙市中学2017-2018学年高二上学期第三次双周考试化学试题【全国百强校】内蒙古自治区集宁一中2018-2019学年高二上学期第一次阶段测试化学试题【全国百强校】河北省衡水市武邑中学2018-2019学年高二上学期第一次月考化学试题2017-2018学年鲁科版高二化学选修4第二章第一节化学反应的方向作业题【校级联考】湖南省浏阳市六校联考2018-2019学年高二上学期期中考试化学试题广东省惠州市惠东县燕岭学校2018-2019学年高二上学期期中考试化学试题【全国百强校】湖北省沙市中学2018-2019学年高二上学期期中考试化学试题云南省育能高级中学2018-2019学年高二上学期期中考试化学试题湖北省公安县第三中学2018-2019学年高二上学期12月质量检测考试化学试题河北省保定市2019-2020学年高二上学期期末调研考试化学试题湖南省株洲市第二中学2019-2020学年高二下学期第一次月考化学试题甘肃省武威市古浪县第二中学2019-2020学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向黑吉两省十校2020-2021学年高二上学期期中联考(吉雅2校用)化学试题内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题四川广元川师大万达中学2020-2021学年高二上学期期中考试化学试题甘肃省张掖市2020-2021学年高二上学期期末学业水平质量检测化学试题海南省海口市琼山中学2019-2020学年度高二上学期第二次月考化学试题湖北省宜昌市人文艺术高中2020-2021学年高二上学期期中考试化学试题陕西省咸阳市泾干中学2021-2022学年高二上学期第二次月考化学试题河南省新郑市2021-2022学年高二上学期第一次阶段性检测化学试卷宁夏海原第一中学2021-2022学年高二上学期第一次月考化学试题天津市第三中学2021-2022学年高二上学期10月阶段性检测化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题浙江省宁波市咸祥中学2021-2022学年高二上学期期中考试化学试题天津市和平区2021-2022学年高二上学期线上期末质量检测化学试题(已下线)2.2.1 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省丽江市第一高级中学2021-2022学年高二上学期期中考试化学试题吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题辽宁省新民市第一高级中学2021-2022学年高二上学期10月月考化学试题广东省江门市蓬江区棠下中学2022-2023学年高二上学期第一次月考化学试题浙江省玉环市玉城中学2022-2023学年高二上学期第一次月考化学试题 广西钟山县钟山中学2021-2022学年高二上学期第二次月考化学(理科)试题河北省唐山市2022-2023学年高二上学期期末考试化学试题广东省汕尾华大实验学校2022-2023学年高二上学期12月月考化学试题河北省唐山市2022-2023学年高二下学期开学考试化学试题天津市河西区2023-2024学年高二上学期11月期中化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)广东省茂名市化州市第一中学2023-2024学年高二上学期期中测评化学试题天津市耀华中学2023-2024学年高二上学期期末学情调研化学试卷2015-2016学年吉林省松原市油田高中高一下期末化学试卷陕西省西安市第一中学2018届高三上学期第一次考试化学试题云南省西畴县第二中学2020届高三上学期开学考试化学试题云南省开远市实验中学2020届高三上学期开学考试化学试题贵州省荔波高级中学2019-2020学年高三上学期期末考试理综化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)云南省玉溪市民族中学2021-2022年高三下学期适应性考试(七)化学试题云南省曲靖市宣威市第七中学2021-2022学年高三下学期3月考试化学试题云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)湖南省岳阳市岳阳县2021-2022学年高三上学期入学考试化学试题
名校
8 . 在两个固定体积均为 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率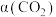 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是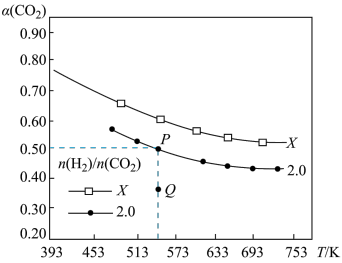
| A.该反应在常温下不可能自发进行 |
B.X的氢碳比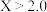 ,在氢碳比为2.0时Q点 ,在氢碳比为2.0时Q点 点 点 |
C.向处于P点状态的容器中,按2∶4∶1∶4的比例再充入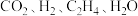 ,再次平衡后 ,再次平衡后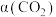 减小 减小 |
D.若起始时 、 、 浓度分别为 浓度分别为 、 、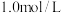 ,则可得P点对应温度的平衡常数的值为512 ,则可得P点对应温度的平衡常数的值为512 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
A.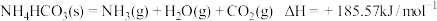 ,在无催化下不加热也能自发进行,原因是反应有自发地向混乱度增加的方向转变的倾向 ,在无催化下不加热也能自发进行,原因是反应有自发地向混乱度增加的方向转变的倾向 |
| B.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| C.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
| D.焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
您最近一年使用:0次
解题方法
10 . 研究化学反应中的能量变化具有重要意义。下列说法正确的是
A.已知: 500° C、30MPa 下,N2(g) +3H2(g)  2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ 2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ |
| B.汽车尾气净化器中的反应为2NO(g) +2CO(g) =N2(g) +2CO2(g) ,该反应在一定条件 下能自发进行,说明该反应的 ΔH>0 |
C.已知反应2NO2(g)  N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 |
| D.C2H5OH(1) 的燃烧热的热化学方程式为2C2H5OH(1) +6O2(g) =4CO2(g) +6H2O(g) ΔH= −1367.0 kJ∙mol−1 |
您最近一年使用:0次



